Исходная гипотеза выглядела так: первым событием в реакции слияния (рис. 21) является взаимодействие двух комплементарных v- и t-SNAREs (находясь на разных мембранах, они образуют так называемый транс-комплекс). Далее этот комплекс рекрутирует из цитоплазмы SNAP, который, в полном соответствии со своим названием, привлекает к месту будущего слияния NSF. Таким образом, между везикулой и мембраной-мишенью образуется мостик, представляющий собой 20S-fusion particle. Слияние происходит за счет гидролиза АТФ на NSF, энергия которого, по мысли авторов, нужна для «активации» (priming) связи t- и v-SNARE. В результате липиды реорганизуются, мембрана везикулы встраивается в мембрану-мишень, а v- и t-SNARE оказываются в общей теперь мембране параллельно друг другу (так называемый цис-комплекс).
 |
Рис. 21. Первоначальная гипотеза регуляции слияния
мембран с помощью NSF-SNAP-SNARE. См. пояснения в тексте
Однако первые восторги по поводу столь простого и изящного механизма несколько остыли по мере получения новых данных. Во-первых, оказалось, что скорость слияния мембран гораздо выше, чем скорость гидролиза АТФ на NSF, следовательно, эта энергия не может быть использована для слияния. Во-вторых, как выяснилось, некоторые стадии обслуживаются более чем 2-мя SNARE, и напротив, некоторые SNARE обеспечивают более чем одну стадию транспортного процесса. Возник закономерный вопрос: каким же образом обеспечивается специфичность слияний и как клетка разбирается во всем многообразии SNAREs? Во-вторых, стало непонятно, как энергетически обеспечивается этот процесс, и какую роль в нем играет NSF.
Ключ к ответу дала информация по структуре большого числа SNARE. Самой характерной чертой этих мембранных белков оказалось наличие длинного суперскрученного линейного участка. Такой участок в рецепторе может быть один, их может быть два, они могут заканчиваться или перемежаться глобулярными доменами. SNARE-комплекс наиболее стабилен, если образован «пучком» из 4 суперскрученных участков таким образом, что против ключевого аргининового остатка (R) лежат три остатка глутамина (3Q). Эта гипотеза получила название Q-R модели.
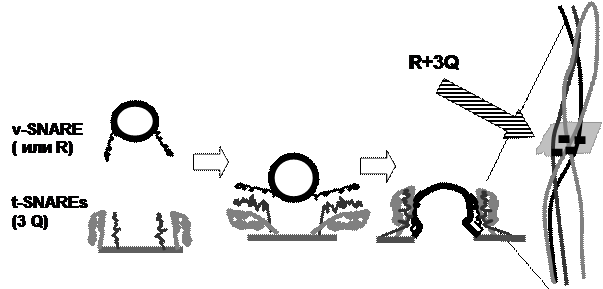 | |||
Рис. 22. Образование комплекса 3Q+R
Оказалось (рис. 22), что в транс-комплексе все SNARE ориентированы также, как и в цис-комплексе, т. е. формируют некое подобие «молнии». Как правило, R – это v-SNARE, а Q - t-SNARE, причем их приблизительно в 3 раза больше, чем R-SNARE. Они делятся на Qa, Qb и Qc. Тем не менее, отношение молекул рецепторов на мембране-мишени к рецепторам на везикуле не всегда соотносится как 3 к 1, поскольку некоторые t-SNARE несут по два участка, формирующих комплекс, таким образом, число молекул рецепторов может быть меньше 4х.
Прояснился и вопрос со специфичностью. Оказалось, что каждой стадии определенного транспортного пути соответствует уникальный комплекс SNARE-рецепторов, конкретные составляющие которого, однако, могут меняться не полностью. Это, в свою очередь, обеспечивает жесткую последовательность отдельных стадий одного пути. Так, например, в дрожжах за слияния сформированных в ЭПР везикул с цис-АГ отвечает комплекс Sec22-Bet1p-Sed5p-Bos1p, за транспорт через цистерны АГ – Sec22-Sed5p-Gos1p, а слияния везикул, сформированных в АГ, с эндосомами – Ykt6p-Sed5-Vti1p. Таким образом, каждый комплекс уникален, но Sed5p, аналог синтаксина5 млекопитающих, присутствует во всех комплексах, «оркеструя» доставку вновь синтезированных белков в эндосомы.
Как правило, очень важные для клетки процессы имеют несколько уровней контроля. Так, способность синтаксинов (t-SNARE) к слиянию в норме подавлена в результате взаимодействия с протекторным белком семейства n-Sec1, который препятствует его спонтаному переходу в «активную» конформацию». позволяя избегать несанкционированных слияний даже при наличии всех компонентов SNARE-комплекса. Протектор n-Sec1 взаимодействует с N-концом синтаксинов и подавляет скорость слияния в 2000 раз.
Таким образом, действующая модель регуляции слияния мембран с помощью SNARE выглядит следующим образом.
При сближении везикулы, несущей v-SNARE, с мембраной-мишенью, имеющей 2–3 t-SNARE, кэпированные протекторным белком, происходит так называемая «нуклеация», в результате которой протектор уходит, и все SNARE выстраиваются в транс-комплекс. На следующем этапе, как правило, необходимо присутствие ионов Са2+ . Предполагали, что кальций требуется для того, чтобы «молния» стабилизировалась, комплекс SNARE реорганизовался в жесткую структуру-шпильку, а мембрана везикулы и мембрана-мишень оказались друг от друга на расстоянии нескольких нанометров. Такая суперпозиция заканчивается реорганизацией билипидных слоев и формированием п о ры слияния, в результате чего мембрана везикулы встраивается в акцепторную мембрану, а все рецепторы оказываются в одной мембране в цис-комплексах.
Именно на этой стадии в дело включается SNAP и NSF, и энергия гидролиза АТФ на NSF тратится на диссоциацию цис-комплекса. Затем v-SNARE рециклируют. Таким образом, NSF работает не в начале процесса слияния, а уже после окончания слияния мембран, обеспечивая возможность рециклирования v-SNARE в мембрану-донор.
Сливающиеся мембраны, как правило, принадлежат объемным структурам с относительно упругой поверхностью. Возникает вопрос: сколько транс-комплексов должно быть образовано между двумя везикулами, чтобы призошло их слияние? Окончательного ответа на этот вопрос нет, но моделирование процесса позволяет предполагать, что таких комплексов должно быть минимум три на одну будущую пору слияния.