Основные понятия и определения
Теплообмен – перенос энергии в виде тепла, происходящие между материальными потоками или телами, имеющими различную температуру.
Теплообмен осуществляется за счет обмена энергией между молекулами, атомами, электронами в результате теплообмена интенсивность движения (колебания) более нагретого тела снижается, а менее нагретого увеличивается.
Теплоносители – это материальные потоки или тела, участвующие в процессе теплообмена.
Теплопередача – передача тепла через теплопередающую (разделяющую) поверхность.
Тепловой поток(Q) – количество тепла, передаваемое в единицу времени от одного материального потока к другому.
[Q] = [Дж/с] = [Вт] = [кал/с]
1 калория = 4,19 Дж
1 Дж = 0,24 кал
Теплообмен подчиняется закону сохранения энергии: «Тепло передается от одной среды к другой без потерь», то есть для процессов теплообмена может быть составлен тепловой баланс. Составлению теплового баланса предшествует составление материального баланса.
Уравнение теплового баланса.
Теплоемкость – это количество тепла, необходимое на нагревание или охлаждение 1 кг, 1 м3 или 1 моль вещества на 10.
Различают удельную, объемную и молярную теплоемкость.
[С]=[кДж/кг*К]
Теплоемкость является справочной величиной и характеризует способность тела аккумулировать в себе тепло.
Для газов различают Сv (при постоянном объеме) и Ср (при постоянном давлении).
Ср – это величина работы, совершенной газом при расширении на 10.
[Ср]=[кДж/кмоль*К]
С = ¦ (t)
Средняя теплоемкость( ) – количество тепла, передаваемое единицей количества вещества при изменении температуры от t1 до t2.
) – количество тепла, передаваемое единицей количества вещества при изменении температуры от t1 до t2.

Энтальпия(теплосодержание) – количество тепла, необходимое для нагревания 1 кг(1 м3 или 1 моль) от 00 до данной температуры.
Для жидкостей энтальпия обозначается i, для газовY.
[ i ] = [кДж/кг] = [кДж/м3] = [кДж/кмоль]

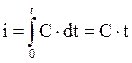
Энтальпия является справочной величиной.
Теплота фазового или химического превращения.
В ходе процесса теплопередачи могут быть фазовые, физические и химические превращения.
Фазовые превращения: испарение, конденсация. При испарении тепло затрачивается, при конденсации тепло выделяется.
Физические превращения: адсорбция, абсорбция, десорбция.
Теплота физического превращения (адсорбция, абсорбция, десорбция).
Теплота химического превращения: выделение тепла – экзотермическая реакция, поглощение тепла – эндотермическая реакция.
Теплота фазового превращения (r) - количество тепла, которое выделяется или поглощается при изменении агрегатного состояния теплоносителя, при осуществлении физического процесса или при осуществлении химического превращения единицы массы вещества.
[ r ] = [Дж/кг]=[Дж/м3]=[Дж/кмоль]
Тепловой баланс может быть составлен двумя способами.
Способы составления теплового баланса:
1) Внутренний метод (с использованием величин теплоемкости).
При составлении теплового баланса по внутреннему методу рассматривается перераспределение тепла между теплообменивающимися средами внутри аппарата. Количество тепла, передаваемого от горячего теплоносителя к холодному называется тепловой нагрузкой аппарата.
А) При отсутствии фазового превращения.


 - тепловая нагрузка аппарата;
- тепловая нагрузка аппарата;
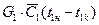 - количество тепла, отданное горячей средой;
- количество тепла, отданное горячей средой;
 - количество тепла, принятое холодной средой;
- количество тепла, принятое холодной средой;
С1,С2 – теплоемкость сред при средней температуре.
Б) Если в процессе теплообмена в одной фазе происходит фазовое превращение.
Пусть в первой среде происходит конденсация.



r- теплота конденсации;
 - охлаждение
- охлаждение 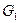 до температуры фазового превращения;
до температуры фазового превращения;
 - теплота фазового превращения;
- теплота фазового превращения;
 - охлаждение остатков
- охлаждение остатков 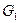 до конечной температуры;
до конечной температуры;
 - охлаждение продуктов фазового превращения до конечной температуры.
- охлаждение продуктов фазового превращения до конечной температуры.
Конденсация и испарение идут при постоянной температуре фазового превращения  .
.
Недостатки внутреннего метода:
1.Необходимо учитывать средние теплоемкости для данного интервала, что сделать по справочным данным не всегда возможно
2.При наличии фазового превращения также сложно определить r.
2) Внешний метод(с использованием величин удельных энтальпий).
В этом случае аппарат представляет собой «черный ящик».
А) При отсутствии фазового превращения.

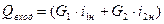

 =
= 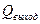
 =
= 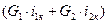

 - тепловая нагрузка аппарата;
- тепловая нагрузка аппарата;
 - разность теплосодержания в начале и в конце процесса для первой среды;
- разность теплосодержания в начале и в конце процесса для первой среды;
 - разность теплосодержания в начале и в конце процесса для второй среды.
- разность теплосодержания в начале и в конце процесса для второй среды.
Б) Если в процессе теплообмена в одной фазе происходит фазовое превращение.
Пусть в первой среде происходит конденсация.


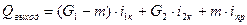
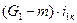 - теплосодержание потока не претерпевшего превращения;
- теплосодержание потока не претерпевшего превращения;
 - теплосодержание второго потока;
- теплосодержание второго потока;
 - теплосодержание продуктов конденсации при температуре
- теплосодержание продуктов конденсации при температуре  .
.
r0 – теплота фазового превращения при температуре t =00 для данной среды;
 - энтальпия продуктов превращения при температуре на выходе из аппарата.
- энтальпия продуктов превращения при температуре на выходе из аппарата.
 =
=