A. Канареечно-желтого цвета;
Б. Белого цвета;
B. Оранжевого цвета;
Г. Черно-коричневого цвета;
Д. Сиреневого цвета.
178. В результате реакции образовался осадок белого цвета состава Me2[Fe(CN)6], указывающий на наличие в минерализате катиона:
1. Марганца;
2. Цинка;
3. Висмута;
4. Кадмия;
5. Бария.
179. Катион цинка можно доказать реакциями с:
1. Дитизоном;
2. Тиомочевинной;
3. Сульфидом натрия;
4. Перйодатом калия;
5. Тетрароданомеркуратом аммония.
180. С помощью подобного комплекса при рН >7 можно экстрагировать из минерализата катион:
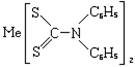
1. Висмута;
2. Кадмия;
3. Сурьмы;
4. Цинка;
5. Меди.
181. Доказательство ртути в деструктате основано на реакции:
A. Зангер-Блека;
Б. Несслера;
B. Полежаева;
Г. Марша;
Д. Гутцайта.
182. Приведенный комплекс образуется при доказательстве катиона:
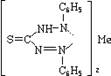
A. Серебра;
Б. Ртути;
B. Свинца;
Г. Цинка;
Д. Таллия.
183. В результате реакции образовался кирпично-красный осадок состава Cu2[MeI4], что свидетельствует о наличии в растворе катиона:
A. Сурьмы;
Б. Свинца;
B. Ртути;
Г. Серебра;
Д. Мышьяка.
УСТАНОВИТЕ СООТВЕТСТВИЕ
Катион Основная реакция с реагентом
184. Сурьмы в А. 8-оксихинолин
185. Висмута а Б. Дитизон
186. Свинца б В. Малахитовый зеленый
Г. Дифенилкарбазид
Д. Тиомочевина
УСТАНОВИТЕ СООТВЕТСТВИЕ
Катион Основная реакция с реагентом
187. Хрома г А. Диэтилдитиокарбаминат натрия
188. Меди в Б. Дитизон
190. Серебра б В. Диэтилдитиокарбаминат свинца
Г. Дифенилкарбазид
Д. Малахитовый зеленый
УСТАНОВИТЕ СООТВЕТСТВИЕ
Катион Реакция с реагентом
191. Висмута бг А. Пиридинродановый реактив
192. Цинка в Б. Тиомочевина
193. Меди а В. Сульфид натрия
Г. 8-оксихинолин
Д. Йодат калия
194. Катион свинца количественно можно определить методами:
1. Комплексонометрическим (обратное титрование);
2. Комплексонометрическим (прямое титрование);
3. Экстракционно-фотометрическим по дитизонату;
4. Экстракционно-фотометрическим по диэтилдитиокарбаминату;
5. Дихроматно-йодометрическим.
195. Катион марганца количественно определяют методами:
1. Экстракционно-фотометрическим по дитизонату;
2. Фотоэлектроколориметрическим по перманганат-иону;
3. Комплексонометрическим (прямое титрование);
4. Сравнительного титрования;
5. Гравиметрическим.
196. Катион хрома количественно определяют фотоэлектроколориметрическим методом по реакции с:
A. Дитизоном;
Б. Диэтилдитиокарбаминатом натрия;
B. Дифенилкарбазидом;
Г. Малахитовым зеленым;
Д. Пиридинродановым реактивом.
197. Катион меди количественно определяют экстракционно-фотометрическим методом по реакции с:
A. Диэтилдитиокарбаминатом натрия;
Б. Диэтилдитиокарбаминатом свинца;
B. Дитизоном;
Г. Малахитовым зеленым;
Д. 8-Оксихинолином.
198. Катион сурьмы количественно определяют методом:
1. Гравиметрическим;
2. Роданометрическим;
3. Экстракционно-фотометрическим по комплексу с малахитовым зеленым;
4. Комплексонометрическим;
5. Фотометрическим по ацидокомплексу гексахлорсурмиата.
199. Катион таллия количественно определяют экстракционно-фотометрически методом по реакции с:
1. 8-Оксихинолином;
2. Малахитовым зеленым;
3. Дитизоном;
4. Диэтилдитиокарбаминатом натрия;
5. Пиридинродановым реактивом.
200. Мышьяк количественно можно определить методами:
1. Визуально-колориметрическим по реакции Зангер-Блека;
2. Нитритометрическим;
3. Комплексонометрическим;
4. Аргентометрическим;
5. Фотоколориметрическим по реакции Зангер-Блека.
201. Катион висмута количественно определяют фотоколориметрическим методом по реакции с:
A. Тиомочевиной;
Б. 8-Оксихинолином;
B. Бруцином;
Г. Пиридинродановым реактивом;
Д. Дифенилкарбазидом.
202. Катион кадмия количественно определяют методами:
1. Гравиметрическим;
2. Экстракционно-фотометрическим;
3. Комплексонометрическим;
4. Роданометрическим;
5. Визуально-колориметрическим по сульфиду кадмия.
203. Катион цинка количественно определяют экстракционно-фотометрическим методом по реакции с:
A. Дитизоном;
Б. Малахитовым зеленым;
B. Диэтилдитиокарбаминатом натрия;
Г. 8-Оксихинолином;
Д. Пиридинродановым реактивом.
204. Катион ртути количественно определяют методами:
1. Фотометрическим по тетрайодо(II)меркурату меди(I);
2. Визуально-колориметрическим по тетрайодо(II)меркурату меди(I);
3. Комплексонометрическим;
4. Экстракционно-фотометрическим по дитизонату;
5. Гравиметрическим.
205. Характерные симптомы отравления мышьяком:
А. Расстройства органов ЖКТ;
Б. Неврит с параличами;
В. Темная кайма десен;
Г. Лихорадка;
Д. Деформация костей.
206. В каком случае можно дать заключение о том, что отравление произошло фосфидом цинка?
А. Если после минерализации реакции с дитизоном положительна и подтверждающие реакции также положительны;
Б. Если после перегонки с водяным паром в листилляте и предварительной реакцией с дитизоном и основным исследованием найден цинк;
В. Если в минерализате обнаружена фосфорная кислота по реакции с молибдатом аммония и с магнезиальной смесью;
Г. Если после перегонки с водяным паром в дистилляте обнаружена фосфорная кислота, а в минерализате после «мокрого озоления» найден цинк;
Д. Если после определения цинка в минерализате, его количество превышает естественное содержание.
207. При отравлении солями ртути преимущественно поражаются:
А. Печень, мышцы;
Б. Почки, толстый кишечник;
В. Мозг;
Г. Тонкий кишечник, кости;
Д. Легкие, поджелудочная железа.
208. Пестициды из группы галогенпроизводных можно изолировать из биологического объекта:
1. Минерализацией;
2. Экстракцией органическим растворителем;
3. Перегонкой;
4. Диализом;
5. Деструкцией.
209. Источниками отравления пестицидами могут быть:
1. Сами ядохимикаты;
2. Вода;
3. Пищевые продукты;
4. Сельскохозяйственные растения;
5. Домашние животные.
210. Пестициды классифицируют на отдельные группы в зависимости от:
1. Химического строения;
2. Назначения;
3. Путей проникновения в организм;
4. Токсичности;
5. Степени летучести.
211. Для предохранения неметаллических материалов от разрушения микроорганизмами используют:
A. Фунгициды;
Б. Антисептики;
B. Альгициды;
Г. Гербициды;
Д. Инсектициды.
212. Для подсушивания растений перед уборкой используют:
A. Нематоциды;
Б. Десиканты;
B. Дефолианты;
Г. Альгициды;
Д. Аттрактанты.
213. Отличительными особенностями группы галогенпроизводных являются:
1. Быстрый метаболизм;
2. Способность к кумуляции;
3. Способность проникать через неповрежденную кожу;
4. Длительная сохраняемость в объектах окружающей среды;
5. Быстрое разложение в объектах окружающей среды.
214. Анализ на содержание ФОС надо проводить:
A. Не позднее 2-х часов после взятия крови;
Б. В течение суток после взятия крови;
B. Время проведения анализа значения не имеет.
215. Холинэстеразная проба основана:
A. На свойстве галогенорганических пестицидов отщеплять атомы хлора;
Б. На способности пестицидов из класса фенолов окисляться;
B. На способности фосфорорганических пестицидов снижать активность ферментов;
Г. На способности фосфорорганических пестицидов повышать активность ферментов;
Д. На свойстве галогенорганических пестицидов накапливаться в организме.
216. Переход окраски индикатора бромтимолового синего в ходе холинэстеразной пробы в норме длится:
А. 30 минут;
Б. 10 – 15 минут;
В. 1 час;
Г. 3 – 5 минут;
Д. 2 часа.
Холинэстеразная проба
A. Имеет положительное судебно-химическое значение;
Б. Имеет отрицательное судебно-химическое значение;
B. Применяется как предварительный, ориентировочный тест;
Г. Является специфической реакцией на органические пестициды.
218. К фосфорорганическим пестицидам относятся:
1. Карбофос;
2. Фосфид цинка;
3. Октаметил;
4. Швейнфуртская зелень;
5. Хлорофос.
219. Для хроматографического скрининга ФОС используют хроматографические системы:
1. гексан - ацетон (2: 1);
2. хлороформ - ацетон (9: 1);
3. гексан - ацетон (4: 1);
4. хлорофом - метанол (9: 1);
5. бензол.