Понятие об энтропии
В термодинамике есть еще одна очень важная функция состояния газа - энтропия (S). Математически прирост энтропии dS определяется выражением

| (3.19) |
где dq - полное количество тепла, подводимое к газу как извне, так и изнутри за счет сил трения;
Т - абсолютная температура.
Если в формуле (2.9) вместо dq подставить его выражение согласно первому закону термодинамики

и произвести ряд преобразований, то можно получить

| (3.20) |
Согласно (2.10) в идеальном адиабатическом процессе, который является обратимым, изменение энтропии равно нулю, так как в этом случае

и изменение энтропии не происходит. В реальном адиабатическом процессе за счет трения выделяется тепло (dqтр>0) и процесс протекает в таком направлении, что энтропия возрастает S2-S1>0.
Таким образом, численное значение S2-S1, может служить мерой потерь механической энергии на преодоление сил трения. Если известны параметры состояния газа в точках 1 и 2, то изменение энтропии в процессе 1 - 2 определяется по формуле (3.20).

Рис. 3.4. Процесс расширения газов
В термодинамике процессы принято представлять в Р - V и Т - S координатах (рис. 3.4).
На рис. 3.4, а представлен процесс расширения газа в турбине. Заштрихованная площадь характеризует техническую работу, которая может быть получена на валу турбины. На рис. 3.4, б тот же процесс представлен в координатах Т - S. Здесь заштрихованная площадь характеризует количество тепла, выделившееся в результате работы, затраченной на преодоление сил трения. Если бы процесс был идеальным, т.е. шел без потерь энергии на трение, то он изображался бы вертикальным отрезком 1 - 2 ад. Соответственно площадь под отрезком 1 - 2 ад равна нулю. Таким образом, использование энтропии позволяет количественно оценить потери механической энергии на трение.
Частные случаи уравнения энергии
Запишем еще раз уравнение энергии

| (3.21) |
При отсутствии технической работы (отсутствует турбина или компрессор в потоке газа) и теплообмена с окружающей средой имеем

Из этого уравнения следует, что изменение скорости в энергетически изолированном потоке газа (q=0, L = 0) однозначно связано с изменением температуры. Если скорость газа не изменяется, то остается постоянной и температура независимо от того, есть трение или нет. Процесс расширения газа в канале от давления Р1 до давления Р2 можно представить на диаграмме в Т - S координатах (рис. 3.5).

Рис. 3.5. Процесс расширения газа: а - идеальная адиабата; в - расширение газа с трением; с - адиабатическое дросселирование
Расширение газа от давления Р1 до давления Р2 может идти различными способами. Процесс расширения а соответствует идеальной адиабате. Потерь на трение нет. Увеличение скорости на участке канала 1- 2 максимальное; уменьшение температуры также максимальное. Уравнение энергии для случая а

Другой случай- с. Вся потенциальная энергия газа переходит в тепло. Скорость не увеличивается, температура не изменяется. Количество тепла, выделившееся в результате работы сил трения, соответствует площади треугольника 1 2 g d е. Уравнение энергии для случая с

откуда w2=w1 и T1=T2д.
Случай в соответствует течению газа по сужающемуся каналу с трением. Скорость увеличивается. Тепло, выделившееся в результате работы сил трения, соответствует площади 1 2 р f е. Уравнение энергии для случая в

Уравнение энергии (3.21) можно записать в виде

| (3.22) |
т.е. суммы энтальпии и кинетической энергии газа для энергетически изолированного потока газа в сечениях 1 и 2 равны между собой. Это соотношение можно записать и для любых других сечений. Поэтому уравнение (3.22) записывается без индексов в виде

Отсюда видно, что если поток газа затормозить полностью (w=0), то энтальпия достигнет максимально возможного значения

Получающееся при этом значение энтальпии i* будем называть полной энтальпией, а соответствующую ей абсолютную температуру

температурой торможения.
В дальнейшем всем параметрам, определенным для заторможенного потока газа будет, присваиваться верхний индекс *.
С помощью (3.23) из уравнения энергии можно исключить скорости, и тогда уравнение энергии записывается в виде
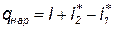
| (3.24) |
Теплоемкость Ср не является строго постоянной величиной, а изменяется в зависимости от температуры, но незначительно. Пользуясь средним значением теплоемкости, можно вычислить температуру торможения по следующей формуле

| (3.25) |
Для воздуха Ср = 1005 Дж/кг К и, следовательно,

В воздушном потоке с нормальной температурой воздуха 300 К при скорости движения w=100; 350; 1000 м/с получается соответственно температура торможения Т*=305, 360,800 К.
Итак, температура торможения за входным устройством самолета (перед компрессором) может быть определена по формуле (3.25).
Для расчета компрессора или турбины обычно пользуются уравнением энергии в форме (3.24). Так как принято, что работа турбины положительна IK>0, а работа компрессора 1К<0, то для турбины имеем
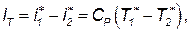
| (3.26) |
а для компрессора

| (3.27) |
Здесь принято, что сечение 1 на входе в компрессор, турбину, а сечение 2 на выходе из компрессора, турбины. По (3.26) можно определить температуру на выходе из турбины T2*, если известны температура на входе Т1* и работа на валу турбины IT По (3.27) можно определить температуру на выходе из компрессора Т2*, если известны температура на входе Т1* и работа, подводимая к валу компрессора IK.
В формулах (3.26) и (3.27) потери на трение в подшипниках, трение дисков о газ или воздух, перетекание через радиальный зазор в лопаточных машинах не учитываются. Применительно к камере сгорания I = 0 уравнение энергии (3.24) будут иметь вид

| (3.28) |
где gT - количество топлива, приходящееся на 1 кг воздуха;
Нu - теплотворная способность топлива т.е. количество тепла, выделяющееся при сгорании 1 кг топлива, кДж/кг;
СP2 - теплоемкость продуктов сгорания, кДж/кг К;
СP1 - теплоемкость воздуха, кДж/кг К;
Т2 * - температура продуктов сгорания, К;
Т1* - температура воздуха на входе в камеру сгорания, К.
Уравнение (3.28) записано для 1 кг воздуха. Расход продуктов сгорания больше расхода воздуха на величину gТ, поэтому в правой части уравнения (3.28) появился сомножитель (1+gT). Уравнение (3.28) дает возможность определить расход топлива для получения необходимой температуры Т2*.