
Дальнейшем пируват, а также жирные кислоты и некоторые аминокислоты окисляются до ацетильного остатка, связанного с коэнзимом А (ацетил-КоА). Эти реакции протекают уже в митохондриях клетки. Пируват и ацетил-КоА, находящиеся на пересечении нескольких метаболических путей, можно отнести к ключевым или узловым метаболитам.
39. Цикл трикарбоновых кислот: последовательность реакций, характеристика ферментов. Амфиболическая функция цитратного цикла. Связь с обменом углеводов, жиров и белков.
Реакции цикла Кребса относятся к третьей стадии катаболизма питательных веществ и происходят в митохондриях клетки. Эти реакции относятся к общему пути катаболизма и характерны для распада всех классов питательных веществ (белков, липидов и углеводов).
Главной функцией цикла является окисление ацетильного остатка с образованием четырёх молекул восстановленных коферментов (трёх молекул НАДН и одной молекулы ФАДН2), а также образование молекулы ГТФ путём субстратного фосфорилирования. Атомы углерода ацетильного остатка выделяются в виде двух молекул СО2.
13.4.2. Цикл Кребса включает 8 последовательных стадий, обращая особое внимание на реакции дегидрирования субстратов:

Рисунок 13.6. Реакции цикла Кребса, включая образование α-кетоглутарата
а) конденсация ацетил-КоА с оксалоацетатом, в результате которой образуется цитрат (рис.13.6, реакция 1); поэтому цикл Кребса называют также цитратным циклом. В этой реакции метильный углерод ацетильной группы взаимодействует с кетогруппой оксалоацетата; одновременно происходит расщепление тиоэфирной связи. В реакции освобождается КоА-SH, который может принять участие в окислительном декарбоксилировании следующей молекулы пирувата. Реакцию катализирует цитратсинтаза, это – регуляторный фермент, он ингибируется высокими концентрациями НАДН, сукцинил-КоА, цитрата.
б) превращение цитрата в изоцитрат через промежуточное образование цис-аконитата. Образующийся в первой реакции цикла цитрат содержит третичную гидроксильную группу и не способен окисляться в условиях клетки. Под действием фермента аконитазы идёт отщепление молекулы воды (дегидратация), а затем её присоединение (гидратация), но другим способом (рис.13.6, реакции 2-3). В результате данных превращений гидроксильная группа перемещается в положение, благоприятствующее её последующему окислению.
в) дегидрирование изоцитрата с последующим выделением молекулы СО2 (декарбоксилированием) и образованием α-кетоглутарата (рис. 13.6, реакция 4). Это – первая окислительно-восстановительная реакция в цикле Кребса, в результате которой образуется НАДН. Изоцитратдегидрогеназа, катализирующая реакцию, - регуляторный фермент, активируется АДФ. Избыток НАДН ингибирует фермент.
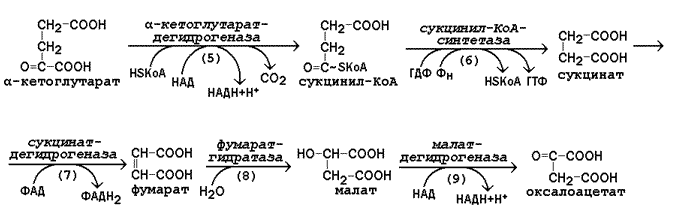
Рисунок 13.7. Реакции цикла Кребса, начиная с α-кетоглутарата.
г) окислительное декарбоксилирование α-кетоглутарата, катализируется мультиферментным комплексом (рис. 13.7, реакция 5), сопровождается выделением СО2 и образованием второй молекулы НАДН. Эта реакция аналогична пируватдегидрогеназной реакции. Ингибитором служит продукт реакции – сукцинил-КоА.
д) субстратное фосфорилирование на уровне сукцинил-КоА, в ходе которого энергия, освобождающаяся при гидролизе тиоэфирной связи, запасается в форме молекулы ГТФ. В отличие от окислительного фосфорилирования, этот процесс протекает без образования электрохимического потенциала митохондриальной мембраны (рис. 13.7, реакция 6).
е) дегидрирование сукцината с образованием фумарата и молекулы ФАДН2 (рис. 13.7, реакция 7). Фермент сукцинатдегидрогеназа прочно связан с внутренней мембраной митохондрии.
ж) гидратация фумарата, в результате чего в молекуле продукта реакции появляется легко окисляемая гидроксильная группа (рис. 13.7, реакция 8).
з) дегидрирование малата, приводящее к образованию оксалоацетата и третьей молекулы НАДН (рис.13.7, реакция 9). Образующийся в реакции оксалоацетат может вновь использоваться в реакции конденсации с очередной молекулой ацетил-КоА (рис. 13.6, реакция 1). Поэтому данный процесс носит циклический характер.
13.4.3. Таким образом, в результате описанных реакций подвергается полному окислению ацетильный остаток СН3-СО-. Количество молекул ацетил-КоА, превращаемых в митохондриях в единицу времени, зависит от концентрации оксалоацетата. Основные пути увеличения концентрации оксалоацетата в митохондриях (соответствующие реакции будут рассмотрены позднее):
а) карбоксилирование пирувата – присоединение к пирувату молекулы СО2 с затратой энергии АТФ;
б) дезаминирование или трансаминирование аспартата – отщепление аминогруппы с образованием на её месте кетогруппы.
13.4.4. Некоторые метаболиты цикла Кребса могут использоваться для синтеза структурных блоков для построения сложных молекул. Так, оксалоацетат может превращаться в аминокислоту аспартат, а α–кетоглутарат – в аминокислоту глутамат. Сукцинил-КоА принимает участие в синтезе гема – простетической группы гемоглобина. Таким образом, реакции цикла Кребса могут участвовать как в процессах катаболизма, так и анаболизма, то есть цикл Кребса выполняет амфиболическую функцию (см. 13.1).
40. Окисление НАДН2 и ФАДН2 в митохондриях. Характеристика основных компонентов дыхательной цепи. Ферментные комплексы. Дегидрирование субстратов и окисление водорода как источник энергии для синтеза АТФ. Роль АТФ в организме.
В пируватдегидрогеназной реакции и в цикле Кребса происходит дегидрирование (окисление) субстратов (пируват, изоцитрат, α-кетоглутарат, сукцинат, малат). В результате этих реакций образуются НАДН и ФАДН2. Эти восстановленные формы коферментов окисляются в митохондриальной дыхательной цепи. Окисление НАДН и ФАДН2, протекающее сопряжённо с синтезом АТФ из АДФ и Н3РО4 называется окислительным фосфорилированием.
Схема строения митохондрии показана на рисунке 14.1. Митохондрии представляют собой внутриклеточные органеллы, имеющие две мембраны: наружную (1) и внутреннюю (2). Внутренняя митохондриальная мембрана образует многочисленные складки – кристы (3). Пространство, ограниченное внутренней митохондриальной мембраной, носит название матрикс (4), пространство, ограниченное наружной и внутренней мембранами, - межмембранное пространство
Дыхательная цепь – последовательная цепь ферментов, осуществляющая перенос ионов водорода и электронов от окисляемых субстратов к молекулярному кислороду – конечному акцептору водорода. В ходе этих реакций выделение энергии происходит постепенно, небольшими порциями, и она может быть аккумулирована в форме АТФ. Локализация ферментов дыхательной цепи – внутренняя митохондриальная мембрана.
Дыхательная цепь включает четыре мультиферментных комплекса
I. НАДН-KoQ-редуктаза (содержит промежуточные акцепторы водорода: флавинмононуклеотид и железосерные белки).
II. Сукцинат-KoQ-редуктаза (содержит промежуточные акцепторы водорода: ФАД и железосерные белки).
III. KoQН2-цитохром с-редуктаза (содержит акцепторы электронов: цитохромы b и с1, железосерные белки).
IV. Цитохром с-оксидаза (содержит акцепторы электронов: цитохромы а и а3, ионы меди Cu2+).
14.1.3. В качестве промежуточных переносчиков электронов выступают убихинон (коэнзим Q) и цитохром с.
Убихинон (KoQ) – жирорастворимое витаминоподобное вещество, способен легко диффундировать в гидрофобной фазе внутренней мембраны митохондрий. Биологическая роль коэнзима Q – перенос электронов в дыхательной цепи от флавопротеинов (комплексы I и II) к цитохромам (комплекс III).
Цитохром с – сложный белок, хромопротеин, простетическая группа которого – гем – содержит железо с переменной валентностью (Fe3+ в окисленной форме и Fe2+ в восстановленной форме). Цитохром с является водорастворимым соединением и располагается на периферии внутренней митохондриальной мембраны в гидрофильной фазе. Биологическая роль цитохрома с – перенос электронов в дыхательной цепи от комплекса III к комплексу IV.
14.1.4. Промежуточные переносчики электронов в дыхательной цепи расположены в соответствии с их окислительно-восстановительными потенциалами. В этой последовательности способность отдавать электроны (окисляться) убывает, а способность присоединять электроны (восстанавливаться) возрастает. Наибольшей способности отдавать электроны обладает НАДН, наибольшей способностью присоединять электроны – молекулярный кислород.
Механизм синтеза АТФ описывает хемиосмотическая теория (автор - П. Митчелл). Согласно этой теории, компоненты дыхательной цепи, расположенные во внутренней митохондриальной мембране, в ходе переноса электронов могут «захватывать» протоны из матрикса митохондрий и передавать их в межмембранное пространство. При этом наружная поверхность внутренней мембраны приобретает положительный заряд, а внутренняя – отрицательный, т.е. создаётся градиент концентрации протонов с более кислым значением рН снаружи. Так возникает трансмембранный потенциал (ΔµН+). Существует три участка дыхательной цепи, на которых он образуется. Эти участки соответствуют I, III и IV комплексам цепи переноса электронов.
Энергия, аккумулированная в форме АТФ, используется в организме для обеспечения разнообразных биохимических и физиологических процессов. Запомните основные примеры использования энергии АТФ:
1) синтез сложных химических веществ из более простых (реакции анаболизма);
2) сокращение мышц (механическая работа);
3) образование трансмембранных биопотенциалов;
4) активный транспорт веществ через биологические мембраны.
Ответы 41-60
41. Сопряжение окисления с фосфорилированием в дыхательной цепи. Н+-АТФсинтетаза мембран митохондрий. Коэффициент Р/О. Разобщение дыхания и фосфорилирования. Гипоэнергетические состояния.
Степень сопряжённости окисления и фосфорилирования в митохондриях характеризует коэффициент фосфорилирования (Р/О). Он равен отношению количества молекул неорганического фосфата (Н3 Р О4), перешедшего в АТФ, к количеству атомов потреблённого кислорода (О 2).
Например, если донором водорода для дыхательной цепи является молекула НАДН, то электроны от донора (НАДН) к акцептору (кислород) проходят 3 участка сопряжения окисления и фосфорилирования (I, III и IV ферментные комплексы дыхательной цепи). Таким образом, максимально может образоваться 3 молекулы АТФ (3 АДФ + 3 Н3РО4 → 3 АТФ). Затрачивается 1 атом кислорода (2 Н + О → Н2О). Значение коэффициента Р/О = 3/1 = 3.
Если донором водорода будет молекула ФАДН2, то электроны в дыхательной цепи проходят 2 участка сопряжения окисления и фосфорилирования (III и IV ферментные комплексы дыхательной цепи). Таким образом, максимально может образоваться 2 молекулы АТФ (2 АДФ + 2 Н3РО4 → 2 АТФ). Затрачивается, как и в предыдущем случае, 1 атом кислорода (2 Н + О → Н2О). Значение коэффициента Р/О = 2/1 = 2.
14.2.2. Более сложный пример расчёта коэффициента фосфорилирования – при окислении пирувата до конечных продуктов - показан на рисунке 14.5. В этом метаболическом пути происходит дегидрирование 4 субстратов (пирувата, изоцитрата, α-кетоглутарата и малата) с образованием НАДН и одного субстрата (сукцината) с образованием ФАДН2. Восстановленные коферменты окисляются в дыхательной цепи, и в сопряжённых реакциях фосфорилирования образуется (4×3 АТФ + 1×2 АТФ)=14 молекул АТФ. Ещё 1 молекула АТФ (ГТФ) образуется в реакции субстратного фосфорилирования на уровне сукцинил-КоА. Таким образом, при полном окислении 1 молекулы пирувата образуется 15 молекул АТФ (из них 14 - путём окислительного фосфорилирования).
Чтобы рассчитать количество потреблённого кислорода, нужно знать число реакций дегидрирования на данном участке метаболического пути. Для окисления каждой восстановленной формы кофермента необходим 1 атом кислорода (см. выше). Следовательно, в нашем примере потребляется 5 атомов кислорода. Значение коэффициента Р/О будет равно 14/5 = 2,8.

Рисунок 14.5. Расчёт энергетического баланса реакций окислительного декарбоксилирования пирувата и цикла Кребса.
Перенос электронов в дыхательной цепи не во всех случаях протекает сопряжённо с фосфорилированием АДФ. Состояние, при котором окисление субстратов в дыхательной цепи происходит, но АТФ при этом не образуется, называется свободным (нефосфорилирующим) окислением. Энергия, выделяемая при окислении, рассеивается в виде теплоты.
В физиологических условиях свободное окисление может служить одним из механизмов терморегуляции. В организме человека и некоторых животных имеется особая ткань – бурый жир, содержащий митохондрии, приспособленные для выработки теплоты. Много бурого жира у новорождённых, в последующие периоды жизни его количество уменьшается. В митохондриях бурого жира содержание дыхательных ферментов значительно выше, чем ферментов, осуществляющих фосфорилирование АДФ, поэтому в них преобладают процессы свободного окисления.
Разобщение процессов окисления и фосфорилирования в митохондриях может иметь место при некоторых патологических состояниях. Основными симптомами таких состояний могут быть быстрая утомляемость, повышенная температура тела, снижение массы тела, несмотря на повышенный аппетит, учащение дыхания и сердцебиения.
14.3.2. Разобщение процессов окисления и фосфорилирования может быть вызвано действием ряда веществ, как природных, так и синтетических. Механизм действия этих веществ заключается в том, что они являются переносчиками протонов через мембрану. Вещества, разобщающие окисление и фосфорилирование, можно разделить на протонофоры и ионофоры.
Протонофоры представляют собой слабые гидрофобные органические кислоты, которые в форме аниона (R-COO-) связывают протоны в межмембранном пространстве, диффундируют через мембрану и диссоциируют в матриксе с образованием протонов. К этой группе относятся, например, свободные жирные кислоты, гормоны щитовидной железы, салицилаты, дикумарол, 2,4-динитрофенол (см. рисунок 14.6).

Рисунок 14.6. Механизм действия 2,4-динитрофенола.
Ионофоры (валиномицин, нигерицин, грамицидин) способны встраиваться в мембрану, образуя канал, по которому могут перемещаться протоны и другие одновалентные катионы - Na+ или K+(рисунок 14.7). В результате снимается протонный потенциал и нарушается синтез АТФ.

Рисунок 14.7. Валиномицин облегчает проникновение в клетку ионов Н+.
Образование и пути использования глюкозо-6-фосфата в организме. Особенности обмена глюкозо-6-фосфата в различных тканях, обусловленные функциональными различиями этих тканей.
Источниками глюкозо-6-фосфата служат 2 процесса: мобилизация гликогена и глюконеогенез.
1. Мобилизация гликогена. В состоянии гипогликемии в крови повышается уровень гормона глюкагона, вырабатываемого а-клетками поджелудочной железы. Подобно адреналину он запускает каскад реакций, приводящих к фосфорилированию внутриклеточных ферментов печени. В том числе, ключевого фермента распада гликогена - гликогенфосфорилазы, что приводит к повышению его активности. Мобилизация гликогена обеспечивает потребности организма человека в глюкозе на протяжении первых 12-24 часов голодания.
2. В более поздние сроки голодания основным источником глюкозы становится глюконеогенез - биосинтез глюкозы из неуглеводных источников.
Основными субстратами для глюконеогенеза при голодании служат глицерол и аминокислоты (за исключением лейцина).
Повышение уровня этих субстратов в крови обеспечивается тем же глюкагоном, за счет распада триацилглицеролов в клеткаж жировой ткани и гормонами коркового вещества надпочечников – глюкокортикоидами, которые стимулируют процессы катаболизма белков во внепеченочных тканях. Кроме того, эти гормоны,индуцируют синтез и повышают активность регуляторных ферментов глюконеогенеза – пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы и фруктозо-1,6-дифосфатазы.
Начальной реакцией превращения глюкозы в клетке является её фосфорилирование в результате взаимодействия с АТФ (рисунок 15.1, реакция 1). Эта реакция в условиях клетки протекает только в одном направлении. Биологическая роль реакции фосфорилирования глюкозы заключается в том, что глюкозо-6-фосфат, в отличие от свободной глюкозы, не может проникать через плазматическую мембрану обратно в кровь и оказывается «запертой» в клетке. Таким образом, глюкозо-6-фосфат является ключевым метаболитом углеводного обмена, на уровне которого осуществляется интеграция различных путей превращения глюкозы в клетке.
В большинстве тканей реакцию фосфорилирования глюкозы катализирует фермент гексокиназа, которая обладает высоким сродством к глюкозе, способна также фосфорилировать фруктозу и маннозу и аллостерически ингибируется избытком глюкозо-6-фосфата. В клетках печени, кроме того, есть фермент глюкокиназа, которая имеет низкое сродство к глюкозе, не ингибируется глюкозо-6-фосфатом и не участвует в фосфорилировании других моносахаридов. Глюкокиназа эффективно функционирует только при высокой концентрации глюкозы в крови. Это способствует усвоению большого количества углеводов, поступающих в печень из кишечника в активную фазу пищеварения.
В следующей реакции глюкозо-6-фосфат изомеризуется во фруктозо-6-фосфат.
43. Гликолиз - локализация в клетке и тканях, последовательность реакций, биологическая роль, энергетический баланс. Утилизация молочной кислоты в организме человека. Интенсивность гликолиза в тканях в период внутриутробного развития плода и после рождения.
Гликолиз – это ферментативный распад глюкозы в аэробных условиях до двух молекул пировиноградной кислоты (аэробный гликолиз), а в анаэробных условиях – до двух молекул молочной кислоты (анаэробный гликолиз). В анаэробных условиях гликолиз протекает в тканях без потребления кислорода и является единственным процессом, поставляющим АТФ, так как окислительное фосфорилирование в этих условиях не функционирует. Анаэробный гликолиз происходит во всех тканях, функционирующих в условиях гипоксии, прежде всего в скелетных мышцах. Гликолиз в эритроцитах даже в присутствии кислорода завершается образованием лактата, поскольку в этих клетках отсутствуют митохондрии.
Гликолиз протекает в цитозоле клеток организма. Этот процесс катализируется одиннадцатью ферментами, которые выделены в высокоочищенном состоянии и хорошо изучены. Условно можно разделить гликолиз на две стадии.
15.2.2. Первая стадия гликолиза является подготовительной и включает реакции превращения молекулы глюкозы в две молекулы фосфотриоз. Эта стадия сопровождается затратой молекул АТФ.
Начальной реакцией превращения глюкозы в клетке является её фосфорилирование в результате взаимодействия с АТФ (рисунок 15.1, реакция 1). Эта реакция в условиях клетки протекает только в одном направлении. Биологическая роль реакции фосфорилирования глюкозы заключается в том, что глюкозо-6-фосфат, в отличие от свободной глюкозы, не может проникать через плазматическую мембрану обратно в кровь и оказывается «запертой» в клетке. Таким образом, глюкозо-6-фосфат является ключевым метаболитом углеводного обмена, на уровне которого осуществляется интеграция различных путей превращения глюкозы в клетке.
В большинстве тканей реакцию фосфорилирования глюкозы катализирует фермент гексокиназа, которая обладает высоким сродством к глюкозе, способна также фосфорилировать фруктозу и маннозу и аллостерически ингибируется избытком глюкозо-6-фосфата. В клетках печени, кроме того, есть фермент глюкокиназа, которая имеет низкое сродство к глюкозе, не ингибируется глюкозо-6-фосфатом и не участвует в фосфорилировании других моносахаридов. Глюкокиназа эффективно функционирует только при высокой концентрации глюкозы в крови. Это способствует усвоению большого количества углеводов, поступающих в печень из кишечника в активную фазу пищеварения.
В следующей реакции глюкозо-6-фосфат изомеризуется во фруктозо-6-фосфат (рисунок 15.1, реакция 2).
Продукт реакции изомеризации подвергается повторному фосфорилированию за счёт АТФ (рисунок 15.1, реакция 3). Эта реакция – наиболее медленно протекающая реакция гликолиза и, подобно фосфорилированию глюкозы, необратима. Фермент – фосфофруктокиназа – является аллостерическим, активируется АДФ, АМФ, и фруктозо-2,6-бисфосфатом, а ингибируется цитратом и высокой концентрацией АТФ.
На следующем этапе фруктозо-1,6-дифосфат подвергается расщеплению на две фосфотриозы (рисунок 15.1, реакция 4). Таким образом, химическое соединение, содержащее 6 углеродных атомов, превращается в два, содержащих по 3 атома углерода. Поэтому гликолиз называют дихотомическим путём превращения глюкозы (от слова «дихотомия» – рассечение на две части).
Далее происходит изомеризация триозофосфатов (рисунок 15.1, реакция 5). В этой реакции диоксиацетонфосфат переходит в глицеральдегид-3-фосфат. Таким образом, в первой стадии гликолиза молекула глюкозы превращается в две молекулы глицеральдегид-3-фосфата. Поэтому в реакциях второй стадии глюкозы будет участвовать по две молекулы каждого субстрата, что необходимо учитывать при расчёте энергетического баланса данного метаболического пути.
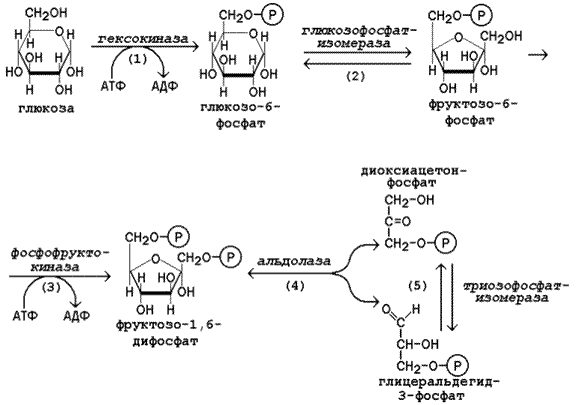
Рисунок 15.1. Реакции первой стадии гликолиза.
15.2.3. Вторая стадия гликолиза включает реакции превращения двух молекул глицеральдегид-3-фосфата в две молекулы лактата. На этой стадии гликолиза происходит синтез молекул АТФ.
Глицеральдегид-3-фосфат подвергается дегидрированию при участии НАД-зависимой дегидрогеназы. В этой реакции происходит потребление неорганического фосфата, который включается в состав продукта реакции, содержащего макроэргическую фосфатную связь (рисунок 15.2, реакция 6), а промежуточным донором водорода служит SH-группа в активном центре фермента, которая потом регенерирует.
1,3-Дифосфоглицерат вступает в реакцию первого субстратного фосфорилирования, т.е. не сопряжённого с переносом электронов в дыхательной цепи. В этой реакции осуществляется синтез молекулы АТФ в результате переноса фосфатной группы вместе с макроэргической связью на молекулу АДФ (рисунок 15.2, реакция 7).
В следующей реакции происходит внутримолекулярное перемещение фосфатной группы 3-фосфоглицерата ко 2-му углеродному атому (рисунок 15.2, реакция 8). Тем самым облегчается последующее отщепление молекулы воды, которое приводит к появлению в продукте реакции макроэргической фосфатной связи (рисунок 15.2, реакция 9).
Фосфоенолпируват (ФЕП) вступает в реакцию второго субстратного фосфорилирования, в ходе которого образуется молекула АТФ. В отличие от первого субстратного фосфорилирования, данная реакция является необратимой в условиях клетки (рисунок 15.2, реакция 10). Фермент пируваткиназа существует в двух изоферментных формах. Изофермент, присутствующий в печёночных клетках, аллостерически ингибируется АТФ и активируется фруктозо-1,6-дифосфатом. Изофермент, присутствующий в головном мозге, мышцах и других тканях, не является аллостерическим и не принимает участия в регуляции гликолиза.
В заключительной реакции гликолиза происходит использование НАДН, образовавшегося при дегидрировании глицеральдегид-3-фосфата (см. реакцию 6). При участии НАД-зависимой лактатдегидрогеназы пируват восстанавливается в молочную кислоту (рисунок 15.2, реакция 11). Фермент существует в пяти изоферментных формах, отличающихся сродством к субстрату и распределением в тканях.

Рисунок 15.2. Реакции второй стадии гликолиза.
Таким образом, в процессе образования лактата из глюкозы в клетке не накапливается НАДН. Это значит, что данный процесс является анаэробным и может протекать без участия кислорода (который является конечным акцептором электронов, передаваемых НАДН в дыхательную цепь). В тканях, функционирующих в условиях гипоксии,
При подсчёте энергетического баланса гликолиза следует учитывать, что каждая из реакций второй стадии этого метаболического пути повторяется дважды. Таким образом, в первой стадии было затрачено 2 молекулы АТФ, а во второй стадии путём субстратного фосфорилирования образовалось 2х2 = 4 молекулы АТФ; следовательно при окислении одной молекулы глюкозы в клетке накапливается 2 молекулы АТФ.
44. Дихотомический аэробный распад глюкозы: схема последовательности реакций, значение. Энергетический баланс аэробного окисления глюкозы.
Аэробным называется окисление биологических субстратов с выделением энергии, протекающее при использовании кислорода в качестве конечного акцептора водорода в дыхательной цепи. В качестве доноров водорода выступают восстановленные формы коферментов (НАДН, ФАДН2 и НАДФН), образующиеся в промежуточных реакциях окисления субстратов.
Аэробное дихотомическое окисление глюкозы является основным путём катаболизма глюкозы в организме человека и может происходить во всех органах и тканях. В результате этих реакций глюкоза расщепляется до СО2 и Н2О, а выделяющаяся энергия аккумулируется в АТФ. В этом процессе можно условно выделить три стадии:
1. превращение глюкозы в 2 молекулы пирувата в цитоплазме клеток (специфический путь распада глюкозы);
2. окислительное декарбоксилирование пирувата с образованием ацетил-КоА в митохондриях;
3. окисление ацетил-КоА в цикле Кребса в митохондриях.
15.3.2. На каждом этапе процесса происходит образование восстановленных форм коферментов, которые окисляются ферментными комплексами дыхательной цепи с образованием АТФ путём окислительного фосфорилирования. Коферменты, образующиеся на второй и третьей стадиях аэробного окисления глюкозы, подвергаются непосредственному окислению в митохондриях. В то же время НАДН, образующийся в цитоплазме в реакциях первой стадии аэробного окисления, не способен проникать через митохондриальную мембрану. Перенос водорода с цитоплазматического НАДН в митохондрии происходит при помощи специальных челночных циклов, основным из которых является малат-аспартатный челночный механизм. Цитоплазматический НАДН восстанавливает оксалоацетат в малат, который проникает в митохондрию, где окисляется, восстанавливая митохондриальный НАД; в цитоплазму оксалоацетат возвращается в виде аспартата (рисунок 15.3).

Рисунок 15.3. Малат-аспартатный челночный механизм.
Продукция АТФ в реакциях аэробного дихотомического окисления происходит также в трёх реакциях субстратного фосфорилирования – две из них в гликолизе, третья в цикле Кребса на уровне сукцинил-КоА. Полный энергетический баланс аэробного окисления глюкозы представлен на рисунке 15.4.

Рисунок 15.3. Энергетический баланс аэробного окисления глюкозы.
45. Пентозофосфатный путь превращений глюкозы. Реакции окислительного этапа. Роль пентозофосфатного пути в различных тканях.
Пентозофосфатный путь представляет собой прямое окисление глюкозы и протекает в цитоплазме клеток. Наибольшая активность ферментов пентозофосфатного пути обнаружена в клетках печени, жировой ткани, коры надпочечников, молочной железы в период лактации, зрелых эритроцитах. Низкий уровень этого процесса выявлен в скелетных и сердечной мышцах, мозге, щитовидной железе, легких.
Пентозофосфатный путь называют также апотомическим путём, так как в его реакциях происходит укорочение углеродной цепи гексозы на один атом, который включается в молекулу СО2.
16.1.2. Пентозофосфатный путь выполняет в организме две важнейшие метаболические функции:
· он является главным источником НАДФН для синтеза жирных кислот, холестерола, стероидных гормонов, микросомального окисления; в эритроцитах НАДФН используется для восстановления глутатиона – вещества, препятствующего пероксидному гемолизу;
· он является главным источником пентоз для синтеза нуклеотидов, нуклеиновых кислот, коферментов (АТФ, НАД, НАДФ, КоА-SН и др.).
16.1.3. В пентозофосфатном пути можно выделить две фазы - окислительную и неокислительную.
Исходным субстратом окислительной фазы является глюкозо-6-фосфат, который непосредственно подвергается дегидрированию с участием НАДФ-зависимой дегидрогеназы (рисунок 16.1, реакция 1). Продукт реакции гидролизуется (реакция 2), а образующийся 6-фосфоглюконат дегидрируется и декарбоксилируется (реакция 3). Таким образом, происходит укорочение углеродной цепи моносахарида на один углеродный атом («апотомия»), и образуется рибулозо-5-фосфат.

Рисунок 16.1. Реакции окислительной фазы пентозофосфатного пути.
16.1.4. Неокислительная фаза пентозофосфатного пути начинается с реакций изомеризации. В ходе этих реакций одна часть рибулозо-5-фосфата изомеризуется в рибозо-5-фосфат, другая - в ксилулозо-5-фосфат (рисунок 16.2, реакции 4 и 5).

Рисунок 16.2. Реакции изомеризации рибулозо-5-фосфата.
Следуюшая реакция протекает при участии фермента транскетолазы, коферментом которой является тиаминдифосфат (производное витамина B1). В этой реакции происходит перенос двухуглеродного фрагмента с ксилулозо-5-фосфата на рибозо-5-фосфат:

Образовавшиеся продукты взаимодействуют между собой в реакции, которая катализируется трансальдолазой и заключается а переносе остатка дигидроксиацетона на глицеральдегид-3-фосфат.
 Продукт этой реакции эритрозо-4-фосфат участвует во второй транскетолазной реакции вместе со следующей молекулой ксилулозо-5-фосфата:
Продукт этой реакции эритрозо-4-фосфат участвует во второй транскетолазной реакции вместе со следующей молекулой ксилулозо-5-фосфата:
 Таким образом, три молекулы пентозофосфатов в результате реакций неокислительной стадии превращаются в две молекулы фруктозо-6-фосфата и одну молекулу глицеральдегид-3-фосфата. Фруктозо-6-фосфат может изомеризоваться в глюкозо-6-фосфат, а глицеральдегид-3-фосфат может подвергаться окислению в гликолизе или изомеризоваться в дигидроксиацетонфосфат. Последний вместе с другой молекулой глицеральдегид-3-фосфата может образовывать фруктозо-1,6-дифосфат, который также способен переходить в глюкозо-6-фосфат.
Таким образом, три молекулы пентозофосфатов в результате реакций неокислительной стадии превращаются в две молекулы фруктозо-6-фосфата и одну молекулу глицеральдегид-3-фосфата. Фруктозо-6-фосфат может изомеризоваться в глюкозо-6-фосфат, а глицеральдегид-3-фосфат может подвергаться окислению в гликолизе или изомеризоваться в дигидроксиацетонфосфат. Последний вместе с другой молекулой глицеральдегид-3-фосфата может образовывать фруктозо-1,6-дифосфат, который также способен переходить в глюкозо-6-фосфат.
16.1.5. Посредством пентозофосфатного пути может происходить полное окисление глюкозо-6-фосфата до шести молекул СО2. Все эти молекулы образуются из С-1-атомов шести молекул глюкозо-6-фосфата, а из образовавшихся при этом шести молекул рибулозо-5-фосфата снова регенерируются пять молекул глюкозо-6-фосфата:

Если упростить представленную схему, то получится:
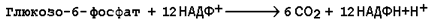
Таким образом, полное окисление 1 молекулы глюкозы в пентозофосфатном пути сопровождается восстановлением 12 молекул НАДФ.
46. Обмен гликогена. Регуляция синтеза и распада гликогена. Мобилизация гликогена печени: последовательность реакций, каскадный механизм активации фосфорилазы. Нарушения обмена гликогена. Гликогенозы.
Гликоген – биополимер, состоящий из остатков глюкозы, он является компонентом всех тканей животных и человека (см. рисунок 15.1). Этот полисахарид служит основным источником энергии и резервом углеводов в организме.
Содержание гликогена в различных органах зависит от физиологического состояния организма. Наиболее высокое содержание гликогена обнаруживается в печени (от 2 до 6% от массы органа). Хотя концентрация гликогена в мышцах значительно ниже (от 0,5 до 1,5%), однако в норме его количество в мышцах составляет 2/3 от общего его содержания в организме.
Гликоген отличается значительным разнообразием по структуре и по относительной молекулярной массе. Молекулы его ветвисты. Глюкозные остатки образуют цепи, в которых они связаны между собой α-1,4-гликозидными связями. Разветвления образуются при помощи α-1,6-гликозидных связей.
Большая часть глюкозы, поступающей в организм с пищей, превращается в клетках печени в гликоген. Это связано с тем, что накопление легко растворимой глюкозы в клетках привело бы к резкому увеличению осмотического давления и разрушению клеточной мембраны.
16.3.2. Молекула глюкозы фосфорилируется при участии фермента глюкокиназы (в гепатоцитах) или гексокиназы (в других клетках) с образованием глюкозо-6-фосфата. Этот метаболит под влиянием фосфоглюкомутазы превращается в глюкозо-1-фосфат (рисунок 16.7, реакция 1).
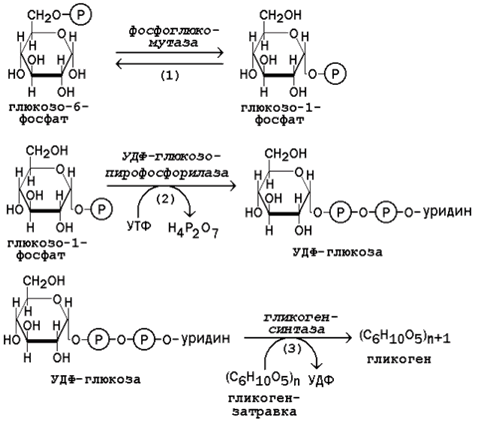
Рисунок 16.7. Реакции биосинтеза гликогена.
Глюкозо-1-фосфат взаимодействует с уридинтрифосфатом (УТФ) в присутствии фермента УДФ-глюкозо-пирофосфорилазы с образованием УДФ-глюкозы – ключевого метаболита углеводного обмена (рисунок 16.7, реакция 2).
Перенос глюкозного остатка с УДФ-глюкозы на затравочную полисахаридную цепь осуществляет гликогенсинтаза – регуляторный фермент данного метаболического пути (рисунок 16.7, реакция 3). Гликогенсинтаза существует в двух формах: гликогенсинтаза b (неактивная) и гликогенсинтаза а (активная). Превращение формы а в форму b катализируется цАМФ-зависимой протеинкиназой, обратный процесс – протеинфосфатазой.
Образование α-1,6-гликозидных связей в молекуле гликогена катализирует ветвящий фермент или трансглюкозидаза (рисунок 16.8).

Рисунок 16.8. Образование α-1,6-гликозидных связей в молекуле гликогена.
Мобилизация, или распад гликогена – процесс превращения гликогена в глюкозу, происходящий в печени. Таким образом, распад гликогена в печени наряду с глюконеогенезом принимает участие в поддержании уровня глюкозы в крови.

Рисунок 16.9. Реакции мобилизации гликогена.
Первую реакцию внутриклеточного расщепления гликогена катализирует фермент фосфорилаза гликогена (рисунок 16.9, реакция 1). Простетической группой его является пиридоксальфосфат (производное витамина В6).
Фосфорилаза гликогена – регуляторный фермент, он существует в двух формах: фосфорилаза а (активная) и фосфорилаза b (неактивная). Переход фосфорилазы b в фосфорилазу а катализирует киназа фосфорилазы, которая фосфорилирует неактивный фермент. Превращение фосфорилазы а в фосфорилазу b катализирует протеинфосфатаза, которая осуществляет дефосфорилирование активного фермента. Следует отметить, что ускорение процессов мобилизации гликогена происходит одновременно с торможением его биосинтеза, и наоборот. Активацию фосфорилазы гликогена вызывают гормоны адреналин
Поделиться:
Поиск по сайту
Все права принадлежать их авторам. Данный сайт не претендует на авторства, а предоставляет бесплатное использование.
Дата создания страницы: 2016-07-22
Нарушение авторских прав и Нарушение персональных данных