Лабораторная работа № 104.
Цель работы: изучение тепловых процессов в идеальном газе, ознакомление с методом Клемана-Дезорма и экспериментальное определение отношения молярных теплоемкостей воздуха при постоянном давлении и постоянном объеме.
Описание установки и метода изучения процесса.

Рис. 1.
Внешний вид рабочей панели и принципиальная схема экспериментальной установки ФПТ1-6н представлена на рис. 1: 1 – включатель «СЕТЬ» для питания установки; 2 – включатель «Компрессор» для нагнетания воздуха в рабочий сосуд (емкость объемом V = 3500 см3), расположенный в полости корпуса; 3 – кран К1, необходимый для предотвращения сброса давления из рабочего сосуда после остановки компрессора; 4 – пневмотумблер «Атмосфера», позволяющий на короткое время соединять рабочий сосуд с атмосферой; 5 – измеритель давления с помощью датчика давления в рабочем сосуде; 6 – двухканальный измеритель температуры, позволяющий измерить температуру внутри окружающей среды и температуру внутри рабочего сосуда.
Состояние некоторой массы газа определяется тремя термодинамическими параметрами: давлением р, объемом V и температурой Т. Уравнение, устанавливающее связь между этими параметрами, называется уравнением состояния. Для идеальных газов таким уравнением является уравнение Клапейрона-Менделеева:
 , (1)
, (1)
где m – масса газа; µ – молярная масса, R = 8,31 Дж/моль·К – универсальная газовая постоянная.
Любое изменение состояния термодинамической системы, связанное с уменьшением или увеличением хотя бы одного из параметров р, V, Т, называется термодинамическим процессом.
Изопроцессы – это процессы, протекающие при одном постоянном параметре:
изобарический – при р = const;
изохорический – при V = const;
изотермический – при Т = const.
Адиабатический процесс совершается без теплообмена с окружающей средой, поэтому для его осуществления систему теплоизолируют или ведут процесс так быстро, чтобы теплообмен не успел произойти. При адиабатическом процессе изменяются все три параметра р, V, Т.
При адиабатическом сжатии идеального газа температура его повышается, а при расширении понижается. На рис. 2 в системе координат р и V изображены изотерма (рV =const) и адиабата (рV γ=const). Из рисунка видно, что адиабата проходит круче изотермы. Объясняется это тем, что при адиабатическом сжатии увеличение давления газа происходит не только из–за уменьшения его объема, как при изотермическом сжатии, но и за счет повышения температуры.

Рис. 2
Теплоемкостью вещества (тела) называется величина, равная количеству теплоты, необходимому для нагревания его на один Кельвин.
Она зависит от массы тела, его химического состава и вида процесса теплоты. Теплоемкость одного моля вещества называется молярной теплоемкостью С µ.
Согласно первому началу термодинамики количество теплоты dQ, сообщенное системе, расходуется на увеличение внутренней энергии dU системы и совершение системой работы dA против внешних сил:
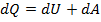 . (2)
. (2)
Используя первое начало термодинамики (2) и уравнение Клапейрона-Менделеева (1), можно вывести уравнение, описывающее адиабатический процесс, - уравнение Пуассона:
 ,
,
или в других параметрах:
TVγ-1=const,
Tγp1-γ=const.
В этих уравнениях γ -показатель адиабаты:
 ,
,
где С V и С p – молярные теплоемкости при постоянном объеме и давлении соответственно.
Для идеального газа расчет теплоемкостей С V и С p можно провести теоретически. При нагревании газа при постоянном объеме (изохорический процесс) работа газа dA = рdV равна нулю, поэтому молярная теплоемкость:
 , (3)
, (3)
где i – число степеней свободы – количество независимых координат, с помощью которых однозначно можно задать положение молекулы; индекс V означает изохорический процесс.
При изобарном нагревании (p =const) количества теплоты, подведенное к газу, расходуется на увеличение внутренней энергии и на совершение работы расширения газа dA=pdV=m/μ RdT. Теплоемкость моля газа при этом равна
 , (4)
, (4)
т.е.
 . (5)
. (5)
Уравнение (5) называется уравнением Майера. Следовательно, разность молярных теплоемкостей С р – С V = R численно равна работе расширения одного моля идеального газа при нагревании его на один Кельвин при постоянном давлении. В этом заключается физический смысл универсальной газовой постоянной R.
Для идеальных газов отношение  зависит только от числа степеней свободы молекул газа, которое, в свою очередь, определяется структурой молекулы, т.е. количеством атомов, из которых состоит молекула. Одноатомная молекула имеет 3 степени свободы (инертные газы). Если молекула состоит из двух атомов, то число степеней свободы складывается из числа степеней свободы поступательного движения (i пост = 3) центра масс и вращательного (i вр = 2) движения системы вокруг двух осей, перпендикулярных к оси молекулы, т.е. равно 5. Для трех- и многоатомных молекул i = 6 (три поступательные и три вращательные степени свободы).
зависит только от числа степеней свободы молекул газа, которое, в свою очередь, определяется структурой молекулы, т.е. количеством атомов, из которых состоит молекула. Одноатомная молекула имеет 3 степени свободы (инертные газы). Если молекула состоит из двух атомов, то число степеней свободы складывается из числа степеней свободы поступательного движения (i пост = 3) центра масс и вращательного (i вр = 2) движения системы вокруг двух осей, перпендикулярных к оси молекулы, т.е. равно 5. Для трех- и многоатомных молекул i = 6 (три поступательные и три вращательные степени свободы).
В данной работе коэффициент γ для воздуха определяется опытным путем.
Если при помощи насоса в сосуд накачать некоторое количество воздуха, то давление и температура воздуха внутри сосуда повысятся. Вследствие теплообмена воздуха с окружающей средой через некоторое время температура воздуха, находящегося в сосуде, сравняется с температурой T0 внешней среды.
Давление, установившееся в сосуде, равно р 1= р 0 + р ′, где р 0 – атмосферное давление, р ′ – добавочное давление. Таким образом, воздух внутри сосуда характеризуется параметрами (р 0 + р ′), V 0, Т 0, а уравнение состояния имеет вид:
 . (6)
. (6)
Если на короткое время (~3с) открыть тумблер «АТМОСФЕРА», то воздух в сосуде будет расширяться. Этот процесс расширения можно рассматривать как подключение к сосуду дополнительного объема V ′. Давление в сосуде станет равным атмосферному Р 0, температура понизится до Т 1, а объем будет равен V 0 + V ′. Следовательно, в конце процесса уравнение состояния будет иметь вид:
 . (7)
. (7)
Разделив выражение (7) на выражение (6), получим:
 . (8)
. (8)
Расширение происходит без теплообмена с внешней средой, т.е. процесс является адиабатическим, поэтому для начального и конечного состояний системы справедливо соотношение
 . (9)
. (9)
Охладившийся при расширении воздух через некоторое время, вследствие теплообмена с внешней средой, нагреется до комнатной температуры Т 0 (изохорический процесс). Давление возрастет до некоторой величины р 2 = р 0 + р ′′, где р ′′ – новое добавочное давление. Для воздуха массой m ′, оставшегося в сосуде, уравнение состояния в начале нагрева:
 , (10)
, (10)
а в конце нагрева до комнатной температуры Т 0:
 . (11)
. (11)
Разделив (10) на (11), получим:
 . (12)
. (12)
Правые части выражений (8) и (12) одинаковы, следовательно, левые части также равны:
 . (13)
. (13)
Возведя левую и правую часть (13) в степень γ, запишем:
 . (14)
. (14)
Заменим правую часть (14) с учетом (9):
 ;
;
откуда
 . (15)
. (15)
Поскольку р ′<< р 0; р ′′<< р 0, то, ограничиваясь первым членом разложения в ряд бинома (1+х) γ =1+ γх и пренебрегая членами второго порядка малости, получим для показателя адиабаты γ:
 ;
;
 . (16)
. (16)
Предварительное задание.
Изучив материал по [1], [2] каждый студент должен:
1) ознакомиться с методом Клемана-Дезорма;
2) получить уравнение Майера для молярных теплоемкостей и вывести уравнение для показателя адиабаты (16).
Рабочее задание.
Определить отношение молярных теплоемкостей воздуха при постоянном давлении и постоянном объеме.
Порядок выполнения работы.
1. Подать на установку питание, включив переключатель «СЕТЬ». При этом переключатель подсвечен.
2. Включить подачу воздуха в рабочий сосуд переключателем «КОМПРЕССОР». При этом слышен шум работающего компрессора и подсвечивается корпус переключателя.
3. По измерителю давления контролировать рост давления в рабочем сосуде. После достижения необходимого уровня рабочего давления отключить компрессор. Закрыть кран К1. Отключить компрессор. (Р тах =6 кПа)
4. После стабилизации давления и температуры в рабочем сосуде снять показания измерителя давления (р ′).
5. На короткое время соединить рабочий сосуд с атмосферой, повернув пневмоклапан «АТМОСФЕРА» по часовой стрелке до щелчка.
6. После стабилизации процесса снять показания измерителя давления (р ′′).
7. Повторить эксперимент п. 3-6 пять раз при различных начальных давлениях воздуха в сосуде (р ′).
Таблица 4.1
| № опыта | р ′, кПа | р ′′, кПа | γ |
| Средние значения |
Указания по обработке результатов измерений.
1) Подставить в формулу (16) полученные значения р ′ и р ′′, взятые из каждого отдельного опыта, вычислить γ 1, γ 2 и т.д. Результаты занести в таблицу.
2) Определить среднее значение γ ср, среднюю абсолютную ошибку Δ γ ср вычислить по формуле:
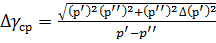 ,
,
где р ′ и р ′′ рассчитать по алгоритму, изложенному в [3].
3) Вычислить относительную погрешность ε γ [3].
4) Представить результат эксперимента в виде:
γ = γ ± Δγср, ε γ=
Контрольные вопросы.
1. Какие виды теплоемкости Вам известны?
2. От чего зависит теплоемкость газов? Почему С р > С V?
3. Каков физический смысл универсальной газовой постоянной R?
4. Объясните изменение температуры газа в процессе опыта.
5. Объясните, почему адиабата при расширении газа спадает круче, чем изотерма?
6. Что называется числом степеней свободы? Как зависят от числа степеней свободы СV и γ? Зная γ (из опыта), рассчитайте число степеней свободы молекулы воздуха.
Литература.
1. Савельев И.В. Курс общей физики. Т. 1. – М.: Наука, 1989. (Для изучения – с. 234 – 241).
2. Трофимова Т.И. Курс физики. – М.: Высш. школа, 1990. (Для изучения - с. 88, 91).
3. Петрунин В.И., Серебренникова Т.А. Обработка результатов измерений физических величин. – М.: Изд-во МЭИ, 1992.