ЛАБОРАТОРНАЯ РАБОТА № 1
ОПРЕДЕЛЕНИЕ СОСТАВА И ТЕПЛОФИЗИЧЕСКИХ ПАРАМЕТРОВ ПРОДУКТОВ СГОРАНИЯ АВИАЦИОННОГО КЕРОСИНА
Цель работы
Целью работы является освоение методики расчёта теплофизических параметров и состава многокомпонентной газовой смеси на примере продуктов сгорания авиационного керосина, а также исследование зависимости удельной теплоёмкости продуктов сгорания от их температуры и состава.
Основные теоретические положения
Взаимосвязь между термическими параметрами рабочего тела устанавливается уравнением состояния [1,2]
f (p, v, Т) = 0. (1.1)
Во многих случаях достаточно точной для описания состояния газообразных рабочих тел и его изменения в различных процессах, происходящих в тепловых машинах, является модель идеального газа. Уравнение состояния для идеального газа имеет вид
pv = RT. (1.2)
В качестве рабочих тел в тепловых машинах и других технических устройствах для взаимного преобразования различных видов энергии используются различные газы, жидкости и (или) их пары.
Воздух и продукты сгорания углеводородных топлив, используемые в качестве рабочих тел в большинстве тепловых двигателей, работающих в атмосфере, являются многокомпонентными газами. Установлено, что смесь идеальных газов обладает свойствами идеального газа и для нее справедливо уравнение состояния (1.2). Однако при проведении расчётов возникает необходимость определения ряда параметров газовой смеси: молярной массы m, газовой постоянной R, удельной изобарной теплоёмкости сp, плотности r и др.
Они могут быть установлены достаточно просто при известном составе газовой смеси, который может быть выражен через массовые доли компонентов (число компонентов п)
 ; (1.3)
; (1.3)
объёмные доли компонентов
 (1.4)
(1.4)
или мольные доли
 ,(1.5)
,(1.5)
где величины с индексом i относятся к отдельным компонентам смеси. Здесь Vi – парциальный объём компонента, находящегося в смеси при парциальном давлении (такой объём компонент занимал бы при температуре Т и давлении p смеси).
Взаимосвязь массовых и объемных долей компонентов смеси идеальных газов выражается соотношениями
 . (1.6)
. (1.6)
Уравнения для расчета параметров смеси идеальных газов при известных параметрах для отдельных компонентов имеют вид:
– молярная масса смеси
 , кг/кмоль,(1.7)
, кг/кмоль,(1.7)
– удельные газовые постоянные компонентов смеси
 , кДж/(кг·К),(1.8)
, кДж/(кг·К),(1.8)
где  кДж/(кмоль·К) – универсальная газовая постоянная;
кДж/(кмоль·К) – универсальная газовая постоянная;
– удельная газовая постоянная смеси
 , кДж/(кг·К),(1.9)
, кДж/(кг·К),(1.9)
– удельная массовая теплоёмкость при постоянном давлении
 , кДж/(кг·К),(1.10)
, кДж/(кг·К),(1.10)
– удельная массовая теплоёмкость при постоянном объёме по уравнению Майера
 кДж/(кг·К),(1.11)
кДж/(кг·К),(1.11)
– удельная мольная теплоёмкость
 , кДж/(кмоль·К),(1.12)
, кДж/(кмоль·К),(1.12)
 , кДж/(кмоль·К), (1.13)
, кДж/(кмоль·К), (1.13)
– удельная объёмная теплоёмкость
 , кДж/(нм3·К),(1.14)
, кДж/(нм3·К),(1.14)
 , кДж/(нм3·К).(1.15)
, кДж/(нм3·К).(1.15)
 – объём 1 киломоля газа при нормальных физических условиях (t 0 =0 oС, р 0 = 101325 Па),
– объём 1 киломоля газа при нормальных физических условиях (t 0 =0 oС, р 0 = 101325 Па),
– показатель адиабаты
 , (1.16)
, (1.16)
– парциальные давления компонентов
 , Па. (1.17)
, Па. (1.17)
Значения истинных теплоёмкостей в уравнениях (1.10)…(1.15) для отдельных компонентов зависят, главным образом, от температуры и задаются в табличной форме (табл. 1.6) или уравнениями вида сi = f (Т). Поэтому соответствующие параметры газовой смеси будут также являться функциями температуры.
В состав сухого воздуха входят следующие компоненты:
азот N2 ( = 0,7803), кислород О2 (
= 0,7803), кислород О2 ( = 0,2099), аргон Аr (
= 0,2099), аргон Аr ( = 0,0094), водород Н2 (
= 0,0094), водород Н2 ( = 0,0001), диоксид углерода СО2 (
= 0,0001), диоксид углерода СО2 ( = 0,0003) и некоторые другие примеси.
= 0,0003) и некоторые другие примеси.
В практических расчётах обычно принимают воздух состоящим из кислорода и атмосферного азота, относя к азоту все примеси. При этом объёмные доли компонентов принимают равными:  = 0,21,
= 0,21,  = 0,79, а массовые доли–
= 0,79, а массовые доли–  =0,232,
=0,232,  =0,768.
=0,768.
Зависимости истинных теплоёмкостей cр = f (Т) для компонентов воздуха и продуктов сгорания углеводородных топлив в диапазоне температур Т = 600…1300 К могут быть аппроксимированы полиномами вида
 , кДж/(кг·К).(1.18)
, кДж/(кг·К).(1.18)
Значения mi, Ri и коэффициенты полинома (1.18) даны в табл. 1.1.
Таблица 1.1
Значения mi, Ri и коэффициенты полинома (1.18)
| Газ | m i, | Ri, | Коэффициенты полинома | ||

| 
| а 0 | а 1 | а 2 | |
| Атмосферный азот N2атм | 28,15 | 0,2954 | 0,87455 | 0,36339 | -0,0811 |
| Кислород О2 | 0,2598 | 0,77723 | 0,47505 | -0,16188 | |
| Диоксид углерода СО2 | 0,1889 | 0,67209 | 0,84759 | -0,28332 | |
| Водяной пар Н2О | 0,4615 | 1,60160 | 0,68262 | 0,00771 | |
| Оксид углерода CO | 0,2968 | 0,86421 | 0,43879 | -0,11824 |
Помимо истинных теплоемкостей в расчетах могут применяться также их средние для интервала температур значения. За начальную температуру при вычислении средней теплоемкости газа может приниматься t 0 = 0 оС или T 0 = -273,15 оС (0 K).
В первом случае средняя теплоемкость определяется по формуле
 , (1.19)
, (1.19)
 . (1.20)
. (1.20)
Соответственно энтальпии могут вычисляться по формулам
 ,(1.21)
,(1.21)
 . (1.22)
. (1.22)
При этом будут соблюдаться условия:  ,
,  , а
, а  , т.е.
, т.е.  .
.
Использование средних теплоемкостей  , отсчитанных от 0оС, практически является неудобным, так как в расчетные термодинамические формулы входит абсолютная температура, поэтому в большинстве случаев используются величины
, отсчитанных от 0оС, практически является неудобным, так как в расчетные термодинамические формулы входит абсолютная температура, поэтому в большинстве случаев используются величины  .
.
В термодинамических процессах с изменением температуры T  [ Т 1; Т 2] средняя для процесса удельная теплоемкость может быть определена по формуле
[ Т 1; Т 2] средняя для процесса удельная теплоемкость может быть определена по формуле
 . (1.23)
. (1.23)
Элементарный химический состав углеводородного топлива с условной формулой С х Н у может быть определен с учетом соотношений
 ,(1.24)
,(1.24)
 ,(1.25)
,(1.25)
где  12,01,
12,01,  1,008 – условные атомные массы, а
1,008 – условные атомные массы, а  ,
,  – массовые доли углерода и водорода в топливе.
– массовые доли углерода и водорода в топливе.
Расчётный состав продуктов сгорания определяется в первом приближении по основным компонентам – СО2,СО, Н2О, N2атм, О2 в пренебрежении диссоциацией компонентов вследствие относительно низких температур газа.
Если пренебречь наличием в продуктах сгорания весьма незначительных концентраций несгоревших углеводородовС х Н у и частиц углерода (дыма), то всю невыделившуюся теплоту сгорания топлива Q неп.сгор. можно отнести к незавершенности реакции СО®СО2
СО +0,5О2 = СО2 + Q(СО ® СО2),
где Q (СО ® СО2) = 285500 кДж/кмоль – экзотермический тепловой эффект этой реакции.
Тогда из уравнения
 неп.сгор. =
неп.сгор. = 
можно определить массовый секундный расход оксида углерода СО за камерой сгорания двигателя
 , кг/с. (1.26)
, кг/с. (1.26)
Здесь  (кг/с) – секундный расход топлива,
(кг/с) – секундный расход топлива,  (кДж/кг) – низшая теплотворная способность топлива (без конденсации водяных паров),
(кДж/кг) – низшая теплотворная способность топлива (без конденсации водяных паров),  – коэффициент полноты сгорания топлива.
– коэффициент полноты сгорания топлива.
Массовый расход элементов, участвующих в реакциях горения, и полученных компонентов газовой смеси можно определить из приводимых ниже стехиометрических уравнений горения элементов топлива.
1. Реакция неполного сгорания углерода такова
С + 0,5О2 = СО + Q( С ® СО ) .
1 кмоль 0,5кмоль 1кмоль
12 кг 16 кг 28 кг
Количество углерода, окисленного в его оксид СО
 , кг/с.(1.27)
, кг/с.(1.27)
Количество прореагировавшего при этом кислорода определяется как
 , кг/с.(1.28)
, кг/с.(1.28)
Количество углерода в топливе, не участвующего в реакции
С ® СО, равно
 , кг/с. (1.29)
, кг/с. (1.29)
2. Реакция окисления углерода в его диоксид СО2 такова
С+ О2 = СО2 + Q (С ® СО2 ) .
1 кмоль 1 кмоль 1кмоль
12 кг 32 кг 44 кг
Количество образовавшегося СО2 равно
 , кг/с. (1.30)
, кг/с. (1.30)
Количество прореагировавшего при этом кислорода определяется как
 , кг/с. (1.31)
, кг/с. (1.31)
3. Реакция окисления водорода в воду Н2О такова
Н2 + 0,5 О2 = Н2О + Q (Н 2® Н2О).
1 кмоль 0,5 кмоль 1кмоль
2 кг 16 кг 18 кг
Количество образовавшейся воды Н2О равно
 , кг/с.(1.32)
, кг/с.(1.32)
Количество прореагировавшего при этом кислорода определяется как
 , кг/с.(1.33)
, кг/с.(1.33)
4. Общее количество кислорода, участвовавшего в реакциях горения, равно
 , кг/с. (1.34)
, кг/с. (1.34)
5. Количество остаточного кислорода в продуктах горения составляет
 , кг/с. (1.35)
, кг/с. (1.35)
Здесь  (кг/с) – массовый расход воздуха на входе в двигатель.
(кг/с) – массовый расход воздуха на входе в двигатель.
3. Описание экспериментальной установки
В качестве исследуемой многокомпонентной газовой смеси выступают продукты сгорания авиационного керосина ТС-1. Регулирование их состава в экспериментах осуществляется за счет различного соотношения массовых расходов сжигаемого топлива  и воздуха
и воздуха  в камере сгорания. Состав топливовоздушной смеси обычно характеризуют коэффициентом избытка воздуха a, определяемым по формуле:
в камере сгорания. Состав топливовоздушной смеси обычно характеризуют коэффициентом избытка воздуха a, определяемым по формуле:
 , (1.36)
, (1.36)
где  , кгвозд/кгтопл – количество воздуха, теоретически необходимого для сгорания 1 кг топлива. Сжигание керосина осуществляется в камере сгорания малоразмерного турбореактивного двигателя (ТРД) ТС-20, схема которого показана на рис. 1.1.
, кгвозд/кгтопл – количество воздуха, теоретически необходимого для сгорания 1 кг топлива. Сжигание керосина осуществляется в камере сгорания малоразмерного турбореактивного двигателя (ТРД) ТС-20, схема которого показана на рис. 1.1.
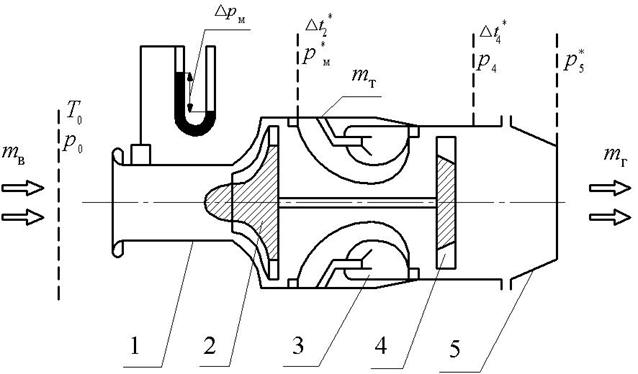
Рис. 1.1. Схема ТРД ТС-20 с контрольными сечениями:
1 – входное устройство с мерным участком, 2 – компрессор,
3 – камера сгорания, 4 – турбина, 5 – реактивное сопло
Последующее расширение газа в турбине и реактивном сопле с понижением температуры газа позволяет провести исследование зависимости удельной теплоемкости и показателя адиабаты продуктов сгорания различного состава от температуры: c = f (Т), k = f (Т).
При проведении эксперимента устанавливаются следующие параметры:
1. Давление р 0 в окружающей среде, измеряется барометром в мм рт.ст.
2. Температура окружающей среды t 0, измеряется спиртовым термометром в градусах Цельсия.
3. Перепад давления D р м в мерном участке входного устройства, измеряется водяным пьезометром в мм вод.ст.
4. Полное давление  за компрессором, измеряется по избыточному давлению с помощью образцового манометра (100 делений шкалы соответствуют избыточному давлению
за компрессором, измеряется по избыточному давлению с помощью образцового манометра (100 делений шкалы соответствуют избыточному давлению  изб.= 2,5 кг/см2 = 245250 Па).
изб.= 2,5 кг/см2 = 245250 Па).
5. Полная температура  за компрессором, измеряется хромель-копелевой (ХК) термопарой с регистрацией величины термоэлектродвижущей силы милливольтметром, шкала которого проградуирована в градусах Цельсия (D t 2* =
за компрессором, измеряется хромель-копелевой (ХК) термопарой с регистрацией величины термоэлектродвижущей силы милливольтметром, шкала которого проградуирована в градусах Цельсия (D t 2* =  - t х.сп., где t х.сп – контролируемая в ходе опытов температура холодного спая термопары, служащая точкой отсчёта при измерениях).
- t х.сп., где t х.сп – контролируемая в ходе опытов температура холодного спая термопары, служащая точкой отсчёта при измерениях).
6. Статическое давление р 4 за турбиной, измеряется по избыточному давлению с помощью образцового манометра (100 делений шкалы соответствуют избыточному давлению  изб. = 1,6 кг/см2 =156960 Па).
изб. = 1,6 кг/см2 =156960 Па).
7. Полная температура  за турбиной, измеряется хромель-алюмелевой (ХА) термопарой с регистрацией величины термоэлектродвижущей силы милливольтметром, шкала которого проградуирована в градусах Цельсия (D t 4* =
за турбиной, измеряется хромель-алюмелевой (ХА) термопарой с регистрацией величины термоэлектродвижущей силы милливольтметром, шкала которого проградуирована в градусах Цельсия (D t 4* =  - t х.сп.).
- t х.сп.).
8. Полное давление р 5* на срезе сопла, измеряется по избыточному давлению с помощью образцового манометра (100 делений шкалы соответствуют избыточному давлению  изб.= 1,6 кг/см2 = 156960 Па).
изб.= 1,6 кг/см2 = 156960 Па).
9. Объемный расход топлива  , измеряется с помощью расходомера ТРД-4, установленного в системе топливопитания двигателя, и электронноцифрового частотомера ЧЗ-24 (fV).
, измеряется с помощью расходомера ТРД-4, установленного в системе топливопитания двигателя, и электронноцифрового частотомера ЧЗ-24 (fV).
10. Частота вращения ротора турбокомпрессора п, измеряется с помощью тахометра ДТЭ-2 и частотомера ИЧ-6 (fп).
При выполнении лабораторной работы проводятся три эксперимента при различных режимах работы двигателя, отличающихся расходом топлива и числом оборотов ротора.
Результаты экспериментов вносятся в таблицу опытных данных (табл. 1.2).
Таблица 1.2
Опытные данные
| Режим | f п | р 0 | t 0 | D р м | 
| D 
| р 4 | D 
| р 5* | fV |
| Гц | мм рт.ст. | оC | мм вод.ст. | делен. | oC | делен. | oC | делен. | Гц | |
| 1. | ||||||||||
| 2. | ||||||||||
| 3. |
4. Обработка результатов эксперимента
1. Прежде всего, необходимо перевести результаты измерений в единицы измерения системы СИ. Для этого используются следующие соотношения для единиц давлений:
1 мм рт.ст.=1 торр=133,6 Па; 1 мм вод.ст.=9,81 Па;
1 кг/см2 = 9,81×104 Па.
Абсолютные давления по сечениям двигателя определяются с привлечением измеренных избыточных давлений
р абс. = р изб. + р 0, Па.
Температуры по сечениям двигателя определяются по формуле
Т = D t + t х.сп.+273,15, К.
Здесь температура холодного спая принимается t х.сп.= t 0, где t 0 – температура воздуха в лаборатории.
Частота вращения ротора турбокомпрессора п равна
п = 3 × fп, об/мин. (1.37)
Объёмный расход топлива определяется по формуле
 , л/с. (1.38)
, л/с. (1.38)
Данные первичной обработки результатов экспериментов вносятся в табл. 1.3.
Таблица 1.3
Данные первичной обработки результатов эксперимента
| Режим | f п | р 0 | Т 0 | D р м |  абс. абс.
| 
| р 4 абс. | 
| р 5*абс. | 
|

| Па | К | Па | Па | К | Па | К | Па | 
| |
| 1. | ||||||||||
| 2. | ||||||||||
| 3. |
2. Необходимыми данными для обработки результатов опытов являются:
а) характеристики керосина ТС-1:
– условная формула С7,2 Н14;
– низшая теплотворная способность Ни = 42914 кДж/кг;
– стехиометрический коэффициент топлива  =14,9 кгвозд/кгтопл;
=14,9 кгвозд/кгтопл;
– плотность топлива rТ = 0,775 ×103 кг/м3 =0,775 кг/л;
б) технические характеристики двигателя ТС-20:
– площадь входного устройства в мерном сечении F м = 109,4×10-4 м2;
– коэффициент полноты сгорания в камере hГ =0,97;
– коэффициент потерь полного давления в камере сгорания sк.с.= 0,92.
3. Расход воздуха находится по формуле
 , кг/с, (1.39)
, кг/с, (1.39)
где удельный объем воздуха  в мерном сечении находится из уравнения состояния
в мерном сечении находится из уравнения состояния
 , м3/кг. (1.40)
, м3/кг. (1.40)
Здесь R в = 287 Дж/(кг×K) – газовая постоянная воздуха.
Учитывая, что  , для более точного расчёта можно воспользоваться формулами
, для более точного расчёта можно воспользоваться формулами
 , Па, (1.41)
, Па, (1.41)
 , К. (1.42)
, К. (1.42)
Здесь  1005 Дж/(кг·К) – удельная теплоемкость воздуха.
1005 Дж/(кг·К) – удельная теплоемкость воздуха.
Скорость воздуха в мерном сечении определяется как
 , м/с. (1.43)
, м/с. (1.43)
Здесь  (м3 /кг) – первоначально найденное приближенное значение удельного объема в мерном сечении.
(м3 /кг) – первоначально найденное приближенное значение удельного объема в мерном сечении.
4. Массовый расход топлива равен
 , кг/с. (1.44)
, кг/с. (1.44)
5. Расход газа
 , кг/с. (1.45)
, кг/с. (1.45)
6. Коэффициент избытка воздуха в камере сгорания
 . (1.46)
. (1.46)
7. Относительный расход топлива
 , кгтопл/кгвозд (1.47)
, кгтопл/кгвозд (1.47)
8. Среднемассовая температура газа  перед турбиной может быть найдена из приближенного уравнения теплового баланса при горении топлива
перед турбиной может быть найдена из приближенного уравнения теплового баланса при горении топлива
 . (1.48)
. (1.48)
В (1.48)  – условная средняя теплоемкость при подводе теплоты в камере сгорания. Отсюда вместо (1.48) имеем:
– условная средняя теплоемкость при подводе теплоты в камере сгорания. Отсюда вместо (1.48) имеем:
 . (1.49)
. (1.49)
Хорошее совпадение с результатами точного расчета величины  получается при
получается при  р =1,1242 кДж/(кг·К). В связи с относительно небольшими скоростями газа в камере сгорания и за турбиной можно приближенно принять равенство статических и температур торможения
р =1,1242 кДж/(кг·К). В связи с относительно небольшими скоростями газа в камере сгорания и за турбиной можно приближенно принять равенство статических и температур торможения  и
и  .
.
9. Считая в первом приближении изменение параметров газа в реактивном сопле, протекающим по обратимой адиабате, принимаем 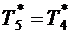 . Тогда статическая температура газа на срезе сопла
. Тогда статическая температура газа на срезе сопла  может быть найдена из уравнения изоэнтропического торможения газа в выходном сечении сопла:
может быть найдена из уравнения изоэнтропического торможения газа в выходном сечении сопла:
 , К. (1.50)
, К. (1.50)
Здесь принимается, что  1,33 и при полном расширении газа в реактивном сопле имеем p 5 = p 0.
1,33 и при полном расширении газа в реактивном сопле имеем p 5 = p 0.
10. Массовый состав продуктов горения определяется как
 , (1.51)
, (1.51)
где значения  ,
,  ,
,  ,
,  определяются по формулам (1.26), (1.30), (1.32), (1.35) соответственно, а
определяются по формулам (1.26), (1.30), (1.32), (1.35) соответственно, а  .
.
Контрольная проверка расчётов исходит из их удовлетворения формуле  .
.
11. Объёмные доли компонентов газовой смеси ri определяются по формуле (1.6), а контрольная проверка расчетов основывается на формуле  .
.
12. Удельная истинная теплоемкость при постоянном давлении для компонентов газовой смеси cрi при температурах Т 3, Т 4, Т 5 определяется по формуле (1.18) или по данным таблицы 1.6 методом интерполяции.
Полученные данные для каждого режима работы двигателя вносятся в табл. 1.4.
Таблица 1.4
Расчётные данные для каждого режима
| Газ | g i | r i | T 3 =, K | T 4 =, K | T 5 =, K |
| cp, кДж/(кг·К) | cp, кДж/(кг·К) | cp, кДж/(кг·К) | |||
| N2 атм | |||||
| О2 | |||||
| СО2 | |||||
| Н2О | |||||
| СО |
13. Удельная газовая постоянная газовой смеси R – по формуле (1.9).
14. Молярная масса газовой смеси m – по формуле (1.7).
15. Удельная истинная теплоемкость при постоянном давлении cр для газовой смеси – по формуле (1.10).
16. Удельная истинная теплоемкость при постоянном объеме cV для газовой смеси – по формуле (1.11).
17. Показатель адиабаты газовой смеси k – по формуле (1.16).
Полученные данные для трёх режимов сводятся в табл. 1.5.
Таблица 1.5
Результаты расчёта для трех режимов работы ТРД
| Режим | aк.с. | m, кг/кмоль | R, кДж/ (кг·К) | T 3, K | cp 3, кДж/ (кг·К) | cv 3, кДж/ (кг·К) | k 3 |
Продолжение табл. 1.5
| Режим | T 4, K | cp 4, кДж/ (кг·К) | cv 4, кДж/ (кг·К) | k 4 | T 5, K | cp 5, кДж/ (кг·К) | cv 5, кДж/ (кг·К) | k 5 |
По результатам расчетов строятся графики зависимостей удельной теплоемкости и показателя адиабаты для продуктов сгорания в виде:
cр = f (Т, a), cv = f (Т, a), k = f (Т, a).
5. Требования к отчёту
Отчёт по лабораторной работе должен включать краткую информацию по теоретической части, схему экспериментальной установки с указанием контрольных сечений проточной части ТРД, таблицы результатов 3-х экспериментов и результатов проведённых расчётов, графики зависимостей
cр = f (Т, a), cv = f (Т, a), k = f (Т, a)
и выводы по работе. В них следует резюмировать полученные данные о массовом и объёмном составе продуктов горения керосина и проанализировать характер протекания зависимостей
cр = f (Т, a), cv = f (Т, a), k = f (Т, a).
При оформлении отчёта следует придерживаться следующих правил:
1. Результаты промежуточных вычислений фиксируются с точностью до 5 значащих цифр (например, р = 101320 Па, Т = 413,15 К,  = 0,95371 кг/с, q т = 0,020351, cp = 1,1242 кДж/кг). Конечные результаты округляются до 4 значащих цифр (cp = 1,124 кДж/кг, k =1,312).
= 0,95371 кг/с, q т = 0,020351, cp = 1,1242 кДж/кг). Конечные результаты округляются до 4 значащих цифр (cp = 1,124 кДж/кг, k =1,312).
2. Вычисления представляются в следующей форме: расчётная формула, числовая подстановка, результат расчёта.
3. У результатов расчёта, представляющих собой размерные величины, обязательно указывается единица измерения.
4. При построении графиков вначале оцениваются диапазоны варьирования параметров и с их учётом наносятся равномерные шкалы, проставляются масштабные числа и с использованием этих масштабов наносятся экспериментальные или расчётные данные. При выборе масштабов должен использоваться предпочтительный ряд чисел: 1; 2; (2,5); 4; 5 и кратные им числа; использование в масштабах чисел 3; 6; 7; 9; 11; 13 и т.д. не допускается.
Истинные массовые теплоёмкости газов в составе продуктов сгорания керосина при постоянном давлении (по спектроскопическим данным [3]) в кДж/(кг×К) представлены в табл. 1.6.
Таблица 1.6
Истинные массовые теплоёмкости газов в составе продуктов сгорания керосина при постоянном давлении (по спектроскопическим данным [3]) в кДж/(кг×К)
| t, oC | T, K | N2 атм | О2 | СО2 | Н2 О | СО | Воздух |
| 573,15 | 1,0605 | 0,9944 | 1,0602 | 1,9994 | 1,0803 | 1,0445 | |
| 623,15 | 1,0709 | 1,0094 | 1,0885 | 2,0315 | 1,0928 | 1,0559 | |
| 673,15 | 1,0822 | 1,0236 | 1,1143 | 2,0646 | 1,1057 | 1,0678 | |
| 723,15 | 1,0940 | 1,0366 | 1,1379 | 2,0984 | 1,1190 | 1,0798 | |
| 773,15 | 1,1061 | 1,0485 | 1,1593 | 2,1329 | 1,1321 | 1,0918 | |
| 823,15 | 1,1181 | 1,0593 | 1,1789 | 2,1677 | 1,1449 | 1,1036 | |
| 873,15 | 1,1298 | 1,0691 | 1,1967 | 2,2030 | 1,1572 | 1,1150 | |
| 923,15 | 1,1412 | 1,0779 | 1,2130 | 2,2383 | 1,1688 | 1,1258 | |
| 973,15 | 1,1520 | 1,0858 | 1,2279 | 2,2738 | 1,1797 | 1,1361 | |
| 1023,15 | 1,1621 | 1,0931 | 1,2416 | 2,3091 | 1,1898 | 1,1457 | |
| 1073,15 | 1,1717 | 1,0998 | 1,2544 | 2,3441 | 1,1992 | 1,1546 | |
| 1123,15 | 1,1807 | 1,1059 | 1,2658 | 2,3788 | 1,2080 | 1,1629 | |
| 1173,15 | 1,1891 | 1,1118 | 1,2766 | 2,4130 | 1,2161 | 1,1707 | |
| 1223,15 | 1,1969 | 1,1172 | 1,2865 | 2,4466 | 1,2236 | 1,1779 | |
| 1273,15 | 1,2043 | 1,1224 | 1,2958 | 2,4793 | 1,2307 | 1,1846 | |
| 1323,15 | 1,2113 | 1,1272 | 1,3044 | 2,5112 | 1,2373 | 1,1909 | |
| 1373,15 | 1,2179 | 1,1319 | 1,3124 | 2,5420 | 1,2435 | 1,1969 |
Значения cр (Т) при температурах T 1< Т < T 2 определяются с помощью линейной интерполяции
 .
.
6. Литература для подготовки и сдачи работы
1. Техническая термодинамика: Учебник для маш. спец. вузов/ В.И. Крутов и др. 3-е изд. М.: Высш. шк., 1991. С. 84-96.
2. Цирельман Н.М. Техническая термодинамика. М.: Машиностроение, 2012. С. 32-35, с. 61-70.
3. Ривкин С.Л. Термодинамические свойства газов: Справочник. 4-е изд., перераб. М.: Энергоатомиздат, 1987. С. 6-10.
ЛАБОРАТОРНАЯ РАБОТА № 4