Причины и механизмы экстрасистолии. Экстрасистолия – преждевременное, внеочередное возбуждение миокарда, часто сопровождающееся преждевременным сокращением всего сердца или отдельных его камер (рис.6). При экстрасистолии свойство генерировать импульс приобретают эктопические центры, и поэтому экстрасистолия относится к категории гетеротопных нарушений ритма.
Классификация экстрасистолии. 1. В зависимости от места образования внеочередного импульса экстрасистолы подразделяются на: наджелудочковые (предсердные, из АВ-узла) и желудочковые. Если регистрируются экстрасистолы из какого-то одного отдела сердца, например, из предсердий, говорят о монотопной экстрасистолии; если обнаруживаются одновременно несколько экстрасистол из разных отделов сердца, говорят о политопной экстрасистолии.
2. Экстрасистолы могут быть одиночными и парными; спорадическими и регулярными. Регулярные экстрасистолы (аллоритмия) появляются с определенной закономерностью: каждое внеочередное сокращение сердца после первого нормального сокращения называют бигеминией (рис. 6, В), каждое внеочередное сокращение после двух нормальных – тригеминией, каждое внеочередное после трех нормальных – квадригеминией.
3. В зависимости от частоты возникновения экстрасистол, их классифицируют как: редкие (менее 5 экстрасистол в минуту); средней частоты (6-15 экстрасистол в минуту); частые (более 15 экстрасистол в минуту).
Рис. 6. А – желудочковая экстрасистола; В – желудочковая экстрасистолия – бигемения
Причины экстрасистолии. К появлению экстрасистолии приводят причины функционального и органического характера, хотя иногда провести точную грань между ними бывает достаточно сложно. Редкая экстрасистолия (до 30 внеочередных сокращений в течение часа) может наблюдаться и у здоровых людей. Описаны «вагусные» причины экстрасистолии, когда появлению внеочередного сокращения предшествует раздражение рефлексогенных зон блуждающего нерва. Так, экстрасистолия может возникнуть после раздражения рецепторов пищевода и желудка (например, после приема пищи), диафрагмы, кишечника, желчного пузыря и др. Экстрасистолия также наблюдается вследствие преобладания тонуса симпатической нервной системы (после употребления крепких кофе, чая, спиртных напитков, психоэмоционального напряжения и др). Изменения нейрогенных влияний с рефлексогенных зон внутренних органов при различных нарушениях осанки также могут приводить к экстрасистолии. Устранение перечисленных выше причин иногда позволяет предупреждать возникновение экстрасистолии. Экстрасистолия часто встречается при различных заболеваниях сердца: острой и хронической ишемической болезни сердца, кардиомиопатиях, миокардиодистрофиях различного происхождения (дисгормонального, алкогольного, тонзиллогенного, токсического и др.), миокардитах, перикардитах, пороках сердца, артериальной гипертензии и др. Нарушения водно-электролитного баланса и кислотно-основного равновесия крови также могут вызывать экстрасистолию.
Механизмы экстрасистолии. В основе развития этого нарушения ритма лежат следующие два механизма: (1) триггерная активность эктопических центров, (2) повторный вход возбуждения (re-entry). При экстрасистолии может нарушаться проводимость внеочередного импульса в антеградном или ретроградном направлении.
Последствия экстрасистолии определяются ее видом и частотой. Редкая экстрасистолия не приводит к каким-либо существенным нарушениям гемодинамики. Частая желудочковая экстрасистолия, как правило, является предвестником более сложных нарушений ритма, например, желудочковой пароксизмальной тахикардии и фибрилляции желудочков. При частой желудочковой экстрасистолии возможно нарушение системной гемодинамики, характеризующееся снижением сердечного выброса до 25% (иногда – до 40%) от исходного и иногда – уменьшением минутного объема крови. При недостаточности сердца, когда сердечный выброс уже снижен, частая желудочковая экстрасистолия способна привести к застойным явлениям в малом круге кровообращения. При частой экстрасистолии коронарный кровоток может уменьшаться на 5-25% от исходного уровня, что может способствовать возникновению ишемии миокарда.
Пароксизмальные тахикардии характеризуются внезапным началом тахикардии.
Классификация пароксизмальных тахикардий. В зависимости от локализации в сердце источника генерации возбуждающих импульсов различают наджелудочковые (суправентрикулярные) и желудочковые пароксизмальные тахикардии. В свою очередь, суправентрикулярные тахикардии подразделяются на предсердные и тахикардии из АВ-соединения. Для пароксизмальных тахикардий характерно увеличение ритма сердечных сокращений свыше 120 в минуту. Частота сердечного ритма может достигать 140-250 сокращений в минуту.
Причины пароксизмальных тахикардий. В подавляющем большинстве случаев желудочковые и наджелудочковые пароксизмальные тахикардии возникают на фоне органического повреждения миокарда (при инфаркте миокарда, кардиомиопатиях, миокардитах, пороках сердца) либо в результате активации дополнительных путей проведения импульса. Реже пароксизмальные суправентрикулярные тахикардии вызывают причины функционального характера (например, поворот головы, сдавление шеи тугим воротничком и др.).
Механизмы возникновения пароксизмальных тахикардий. В основе пароксизмальных тахикардий чаще всего лежат механизмы повторного входа волны возбуждения (re-entry), реже – повышение автоматизма эктопических центров. Стимулом для возникновения пароксизмальной тахикардии является внеочередной импульс – экстрасистола. Сердечный ритм при пароксизмальной тахикардии, как правило, регулярный.
Последствия пароксизмальной тахикардии зависят от ее вида, частоты сокращения камер сердца, а также от характера сопутствующей патологии сердечно-сосудистой системы. Кратковременные эпизоды наджелудочковой пароксизмальной тахикардии с невысокой частотой сердечных сокращений у практически здоровых людей не сопровождаются существенными нарушениями системной гемодинамики и купируются самостоятельно. После окончания пароксизма тахикардии нередко наблюдается учащение мочеиспускания, что объясняется повышенной продукцией натрийуретического пептида в предсердиях желудочков. Частая желудочковая тахикардия, например, на фоне острого инфаркта миокарда, может быть фатальной сама по себе или предвещает фибрилляцию желудочков. Нарушения системной гемодинамики во время пароксизмальной тахикардии обусловлены сочетанием целого ряда механизмов:
1. При увеличении частоты сердечных сокращений укорачивается продолжительность диастолы и уменьшается сила сердечных сокращений, что приводит к уменьшению диастолического наполнения камер сердца и снижению сердечного выброса. Если частота сокращений сердца при наджелудочковой пароксизмальной тахикардии не превышает 140-150 в минуту, то фракция сердечного выброса, приходящаяся на мозг, снижается на 7-12%. При более значительном увеличении числа сердечных сокращений снижение мозгового кровотока может достигать 40%. Поэтому при пароксизмальной тахикардии возможно появление клинических признаков, указывающих на недостаточное кровоснабжение мозга (головокружение, слабость, «пелена» перед глазами, спутанность сознания и др.).
2. Укорочение фазы диастолы приводит к снижению внутриаортального давления и нарушению коронарного кровотока. Изменение градиента трансмиокардиального давления способствует большему нарушению кровотока в субэндокардиальных слоях миокарда. Более того, сама по себе тахикардия увеличивает потребность миокарда в кислороде. Таким образом, создаются условия для возникновения ишемии миокарда, которая усугубляет тяжесть нарушений ритма и проводимости и приводит к дальнейшему падению сердечного выброса (формируется «порочный круг»).
3. Повышение активности симпатической нервной системы, а также изменение характера импульсации от барорецепторов сосудов приводит к увеличению сосудистого периферического сопротивления. Это сопровождается нарушением почечного кровотока, кровотока в органах ЖКТ, мышцах и коже.
4. При снижении сократительной функции миокарда на фоне заболеваний сердца, предшествовавших пароксизму тахикардии, создаются условия для застоя крови в венах малого круга кровообращения и возникновения отека легких.
Мерцательная аритмия. Мерцательная аритмия, включающая в себя мерцание и трепетание предсердий, может быть как пароксизмальной, так и постоянной. Наиболее часто встречается мерцание (фибрилляция) предсердий.
Мерцание предсердий – вид аритмии, характеризующийся нерегулярным, хаотическим возбуждением отдельных мышечных волокон предсердий с частотой 350-700 в минуту, что приводит к нарушению эффективных сокращений предсердий и нерегулярным сокращениям желудочков (рис. 7).

Рис. 7. Фибрилляция предсердий
По частоте встречаемости среди всех нарушений ритма сердца мерцательная аритмия занимает второе место после экстрасистолии. В зависимости от частоты сокращений желудочков выделяют следующие формы мерцательной аритмии:
1. тахисистолическую (частота сокращений желудочков – 90-200 в минуту),
2. нормосистолическую (частота сокращений желудочков – 60-90 в минуту)
3. брадисистолическую (частота сокращений желудочков – менее 60 в минуту).
Причины мерцания предсердий. Мерцательная аритмия в большинстве случаев развивается на фоне имеющихся заболеваний сердца, таких как кардиосклероз, пороки сердца, особенно митральный стеноз, тиротоксикоз, кардиомиопатии, интоксикации, гемохроматоз, перикардит, опухоли сердца и др. Возникновению мерцательной аритмии способствует дилатация предсердий, так как при этом становится возможным образования множества кругов re-entry. Особое значение в инициации пароксизма мерцательной аритмии принадлежит гипокалиемии и гипомагниемии. Повышение тонуса блуждающего нерва в ночные и ранние утренние часы также может провоцировать пароксизм мерцательной аритмии («вагусное мерцание»). Несколько реже встречается «адренергическое мерцание», которое провоцируется повышением тонуса адренергической нервной системы, когда увеличивается частота стимуляции предсердий.
Патогенез. Возникновение мерцания предсердий связано с циркуляцией волн возбуждения по предсердиям. Инициировать механизм повторного входа волны возбуждения может экстрасистола, попавшая в уязвимый период возбудимости миокарда предсердий. Как правило, в предсердиях формируется не менее 4-6 кругов re-entry. Реализации механизмов повторного входа волны возбуждения способствуют укорочение эффективного рефрактерного периода кардиомиоцитов предсердий и замедление движения импульса в предсердиях. При этом кардиомиоциты предсердий характеризуются электрической гетерогенностью, то есть продолжительность эффективного рефрактерного периода различных кардиомиоцитов предсердий варьирует. Поэтому импульс может циркулировать по предсердиям и асинхронно возбуждать отдельные мышечные волокна сколь угодно долго, пока следующий импульс не попадет в «возбудимое окно» и не прервет циркуляцию возбуждения. Асинхронные возбуждения отдельных кардиомиоцитов предсердий нарушают нормальный процесс систолы предсердий. На ЭКГ это проявляется отсутствием зубцов Р, вместо которых регистрируются волны мерцания f (рис. 7). При мерцательной аритмии частота сокращения желудочков все время изменяется, что на ЭКГ проявляется разной величиной интервалов R-R. Аритмичные сокращения желудочков при мерцании предсердий объясняются тем, что часть предсердных хаотических импульсов, поступающих в АВ-соединение, блокируется и не проводится к желудочкам.
Последствия мерцания предсердий. Мерцательная аритмия оказывает неблагоприятное влияние на внутрисердечную и системную гемодинамику. При мерцательной аритмии снижается сердечный выброс. Причем, чем больше частота сокращения предсердий, тем в большей степени уменьшается объем крови, выбрасываемый левым желудочком в аорту. Уменьшение сердечного выброса при тахисистолической форме мерцательной аритмии обусловлено в первую очередь уменьшением диастолического наполнения левого желудочка из-за отсутствия эффективной систолы предсердий и укорочения диастолы желудочков. При мерцательной аритмии величина сердечного выброса может постоянно изменяться. Снижение сердечного выброса особенно выражено у тех пациентов, развитию мерцательной аритмии у которых предшествовали заболевания миокарда со снижением его сократительной функции. В этих условиях пароксизм мерцательной аритмии может сопровождаться застойными явлениями в малом круге кровообращения. Уменьшение и неравномерность сердечного выброса приводят к снижению его фракции, приходящейся на головной мозг. Вследствие этого при мерцательной аритмии могут наблюдаться эпизоды нарушения мозгового кровообращения. Уже доказано, что риск ишемического инсульта у пациентов, страдающих мерцательной аритмией, значительно возрастает. При постоянной форме мерцательной аритмии многократно увеличивается и риск тромбоэмболических осложнений. Высокая вероятность образования тромбов в предсердиях объясняется увеличением в них турбулентности движения крови и «застоем» крови из-за хаотических сокращений отдельных волокон предсердий и отсутствия полноценной систолы предсердий.
Трепетание предсердий. Трепетание предсердий характеризуется регулярными частыми (до 200-400 в минуту)ихсокращениями. Трепетание предсердий может быть пароксизмальным и реже – постоянным. Сокращения предсердий следуют друг за другом практически без диастолической паузы, что на ЭКГ проявляется волнами трепетания F почти одинаковой амплитуды и продолжительности. Регулярность сокращения желудочков при трепетании предсердий зависит от характера функциональной блокады проведения импульса в АВ-узле. Если в АВ-узле блокируется проведение каждого второго импульса из предсердий (блокада 2:1), то на каждые две волны F приходится один желудочковый комплекс. При этом интервалы R-R практически регулярные. Такую форму трепетания предсердий называют регулярной. При нерегулярной форме трепетания предсердий степень АВ-блокады постоянно изменяется, например 2:1, затем 3:1, затем 4:1, затем 3:1 и т.д. При этом на ЭКГ регистрируются интервалы R-R различной продолжительности.
Трепетание предсердий осложняет течение практически тех же заболеваний, что и фибрилляция предсердий. Для объяснения механизма трепетания предсердий предложено две теории. Наиболее доказанной является теория повторного входа волны возбуждения, однако не исключается возможность активации эктопических очагов автоматизма в предсердиях.
Нарушения гемодинамики при трепетании предсердий обусловлены частыми их сокращениями, во время которых к желудочкам поступает меньший объем крови из-за снижения диастолического наполнения предсердий. В то же время, при одинаковой частоте сокращения желудочков снижение сердечного выброса при трепетании предсердий выражено в меньшей степени, чем при мерцании предсердий. Изменения гемодинамики при тахисистолической форме трепетания предсердий практически аналогичны таковым, наблюдающимся при тахисистолической форме мерцания предсердий. Риск тромбоэмболических осложнений при трепетании предсердий, в отличие от мерцания, низкий, что объясняется практически полным регулярным опорожнением предсердий при их трепетании.
Фибрилляция (мерцание) и трепетание желудочков. Фибрилляция желудочков – частые (200-500 в минуту), нерегулярные, хаотические сокращения отдельных мышечных волокон желудочков, приводящие к невозможности осуществления сердцем его насосной функции и клинической смерти. Это тяжелейшее нарушение ритма сердца является частой причиной внезапной коронарной смерти пациентов.
Причины фибрилляции желудочков. Фибрилляция желудочков может развиться при многих заболеваниях сердца: инфаркте миокарда, гипертрофии миокарда и кардиомегалии, кардиомиопатиях, некоторых блокадах сердца, а также при поражении электрическим током, передозировке сердечных гликозидов, антиаритмических препаратов и анестетиков; при хирургических вмешательствах и гипотермии. Терминальные состояния у больных с тяжелыми соматическими заболеваниями и необратимая стадия шока любой этиологии также способны приводить к фибрилляции желудочков. Иногда возникновению фибрилляции желудочков предшествуют различные аритмии: часто повторяющиеся пароксизмы желудочковой тахикардии, в том числе и “torsades de pointes”, частая политопная желудочковая экстрасистолия и др.
Механизмы развития фибрилляции желудочков. Возникновение фибрилляции желудочков объясняется повторной циркуляцией нескольких волн возбуждения по миокарду желудочков. Как правило, в этих условиях формируется нескольких кругов re-entry на фоне электрической гетерогенности миокарда желудочков. Формированию электрической гетерогенности миокарда способствуют: накопление внутри кардиомиоцитов ионизированного кальция; действие высоких концентраций активных форм кислорода и азота; нарушения метаболизма кардиомиоцитов; изменение активности автономной нервной системы, а также электролитные расстройства. При этом процессы реполяризации кардиомиоцитов десинхронизируются во времени, эффективный рефрактерный период кардиомиоцитов существенно различается, и замедлено проведение импульса от волокон Пуркинье к рабочим кардиомиоцитам. Фактически, миокард желудочков представляет собой «мозаику», сложенную из кардиомиоцитов с различными электрофизиологическими характеристиками. Поэтому в таких условиях самопроизвольное прекращение фибрилляции желудочков практически невозможно.
При фибрилляции желудочков на ЭКГ регистрируются нерегулярные волны различной амплитуды и продолжительности (рис. 8). Если реанимационные мероприятия не проводятся, амплитуда волн фибрилляции уменьшается, из крупноволновой она переходит в мелковолновую, вслед за которой возникает асистолия желудочков.
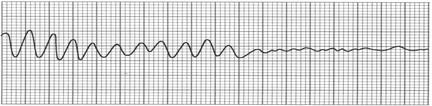
Рис. 8. Желудочковая тахикардия, переходящая в фибрилляцию
желудочков
Последствия фибрилляции желудочков. Клиническая картина фибрилляции желудочков соответствует картине клинической смерти. Отсутствие эффективных сокращений желудочков приводит к прекращению выброса крови в аорту и легочные артерии. Нарушается мозговой кровоток, артериальное давление падает до нуля, и через 6-10 минут при отсутствии или неэффективности реанимационных мероприятий наступает биологическая смерть. Основным методом лечения фибрилляции желудочков является электрическая дефибрилляция сердца. Она позволяет синхронизировать процессы деполяризации «критической массы» миокарда и прервать повторную циркуляцию волн возбуждения по миокарду желудочков.
В отличие от фибрилляции желудочков, при трепетании желудочков частота их сокращений несколько меньше и составляет от 200 до 300 в минуту. На ЭКГ при этом регистрируются ритмичные синусоидальной волны; компоненты желудочкового комплекса не дифференцируются. Причины и механизмы трепетания желудочков сходны с теми же, что и при фибрилляции желудочков. Клиническая смерть при трепетании желудочков обусловлена резким снижением мозгового кровотока в результате неэффективных сокращений левого желудочка и значительного снижения сердечного выброса. Трепетание желудочков самопроизвольно не купируется и может перейти в фибрилляцию желудочков.
Патофизиологическая характеристика наиболее часто встречающихся блокад сердца. Замедления проводимости импульса по различным отделам проводящей системы называются блокадами сердца. В зависимости от локализации нарушения проводимости выделяют следующие разновидности блокад: синоатриальная; атриовентрикулярная и внутрижелудочковые.
При синоатриальной блокаде сердца функционирование синусового узла не нарушено, однако затруднено продвижение волны возбуждения от синусового узла к миокарду предсердий. Часть импульсов из синусового узла не проводится к предсердиям и желудочкам. При этом на ЭКГ отмечается периодическое выпадение зубцов P и желудочковых комплексов. Выпадение отдельных сердечных сокращений могут приводить к синкопальным состояниям в результате нарушения кровообращения мозга. В случае отсутствия нескольких последовательных сокращений предсердий и желудочков могут активироваться латентные пейсмекеры. Это приводит к появлению замещающих ритмов (из эктопических центров автоматизма, расположенных в предсердиях, АВ-соединении, системе Гиса-Пуркинье).
Атриовентрикулярная блокада характеризуется нарушением проведения импульса от синусового узла к АВ-узлу или от АВ-узла к пучкам Гиса. Выделяют три степени АВ-блокады.
При АВ-блокаде I степени замедление проведение импульса наблюдается в самом атриовентрикулярном узле. Все импульсы из синусового узла проводятся к желудочкам, но с некоторым опозданием. Замедление проводимости не сопровождается какими-либо нарушениями системной гемодинамики, и решающим критерием в диагностике АВ-блокады I степени является удлинение интервала PQ свыше 0,20 секунд на ЭКГ. Атриовентрикулярная блокада I степени может наблюдаться при различных заболеваниях сердца, а также у вполне здоровых индивидуумов-ваготоников. С возрастом частота встречаемости этой блокады увеличивается.
АВ-блокада II степени (тип Мобитц I) характеризуется постепенным удлинением интервала P-Q с последующим выпадением желудочкового комплекса. Этот вид блокады вызван замедлением проведения импульса в самом АВ-соединении. Периодические выпадения комплексов QRST называют периодикой Венкенбаха-Самойлова.
Отсутствие единичных сокращений желудочков сопровождается нарушением мозгового кровообращения и проявляется синкопальными состояниями. Кратковременные эпизоды потери сознания на фоне кратковременной асистолии желудочков сердца были описаны еще в XIX в. и получили название в честь охарактеризовавших эти синкопы ученых – приступы Морганьи-Адамса-Стокса. Различают две формы этих приступов – асистолическую и гипердинамическую. Асистолическая форма возникает при синдроме слабости синусового узла и продолжительной асистолии, синоаурикулярной блокаде и АВ-блокаде II степени (типа Мобитц-I), а также полной АВ-блокаде. Гипердинамическая форма приступов Морганьи-Адамса-Стокса наблюдается при фибрилляции или трепетании желудочков, а также при пароксизмальной желудочковой тахикардии. Вызвана она снижением сердечного выброса в результате неэффективной систолы желудочков или уменьшения их диастолического наполнения.
В отличие от АВ-блокады II степени типа Мобитц I, при блокаде II степени типа Мобитц II наблюдается регулярное или лишенное закономерности выпадение желудочковых комплексов без постепенного удлинения интервалов P-Q.
АВ-блокада III степени (полная атриовентрикулярная блокада) вызвана нарушением проведения импульса на уровне проксимальной или дистальной части ветвей пучка Гиса. При этом импульсы из синусового узла не проводятся к желудочкам. Предсердия сокращаются в своем, более частом ритме, а желудочки – в своем ритме, не зависящем от синусового. В этих условиях могут появляться различные замещающие ритмы, чаще исходящие из желудочков. Частота их сокращений при этом обычно не превышает 30-40 в минуту. Если в течение 10-20 секунд замещающий ритм не появился, асистолия желудочков приводит к возникновению приступов Морганьи-Адамса-Стокса.
Наиболее частыми причинами, способными приводить к появлению атриовентрикулярной блокады II и III степени является ишемия миокарда, а также фиброз, кальцификация или инфильтрация воспалительными клетками АВ-узла или пучка Гиса. Механическое повреждение атриовентрикулярного узла в результате хирургических вмешательств на сердце также способно привести к развитию блокад. В последнее время появление дегенеративных изменений в клетках АВ-узла стали связывать с мутацией гена, ответственного за образование и функцию натриевых каналов в клетках проводящей системы.
Внутрижелудочковые блокады. Это собирательное понятие, которое включает в себя блокады различных ветвей и пучков Гиса, а также замедление проводимости на уровне волокон Пуркинье. Различают однопучковые блокады, характеризующиеся нарушением проведения импульса по какому-либо одному из следующих проводящих путей: правой ножке пучка Гиса, левой передней ветви пучка Гиса, левой задней ветви пучка Гиса. При двухпучковых блокадах нарушение проведения импульса происходит на уровне двух из трех вышеуказанных пучков. Нарушение (замедление) проведения импульса по всем трем пучкам Гиса называют трехпучковой блокадой. Если импульс проводится медленнее, либо не проводится по волокнам Пуркинье, говорят об очаговой внутрижелудочковой блокаде. Внутрижелудочковые блокады могут быть полными (если импульс не проводится по какому-то пути системы Гиса-Пуркинье) и частичными, либо неполными (импульс проводится, но медленнее). Внутрижелудочковые блокады могут быть постоянными и преходящими. Электрокардиографические признаки блокад ножек пучка Гиса и волокон Пуркинье подробно описаны в соответствующих руководствах.
В 80% случаев внутрижелудочковые блокады являются следствием различных заболеваний, при которых поражается проводящая система сердца и миокард. Чаще всего к развитию внутрижелудочковых блокад приводит хроническая ишемическая болезнь сердца или острый инфаркт миокарда. Блокады ножек пучка Гиса и их разветвлений встречаются также у 1-2% практически здоровых взрослых людей. Характер влияния внутрижелудочковых блокад на внутрисердечную и системную гемодинамику зависит от вида блокады, характера сократительной функции миокарда и наличия сопутствующих заболеваний сердечно-сосудистой системы. Например, блокада левой ножки пучка Гиса при ишемической болезни сердца усугубляет выраженность нарушений сократительной функции левого желудочка. Это обусловлено асинхронными сокращениями межжелудочковой перегородки вследствие замедления деполяризации левого желудочка и патологического движения межжелудочковой перегородки. В результате может снижаться сердечный выброс. С другой стороны, влияние полной блокады правой ножки пучка Гиса на сократительную функцию неизмененного правого желудочка минимально.