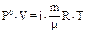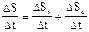| №
| Наименование величины или
физический закон
| Формула
|
|
| Уравнение состояния идеального газа
| 
|
|
| Закон Дальтона
| Р=Р1+Р2+...+Рn
|
|
| Основное уравнение кинетической теории газов
| 
|
|
| Средняя кинетическая энергия молекул (k=1,38×10-23 Дж/К - постоянная Больцмана; i-количество степеней свободы молекулы).
| 
|
|
| Внутренняя энергия вещества
| 
|
|
| Средняя квадратичная скорость
| 
|
|
| Средняя арифметическая скорость
| 
|
|
| Наиболее вероятная скорость
| 
|
|
| Средняя длина свободного пробега молекул (d-эффективный диаметр молекулы)
| 
|
|
| Явления переноса:
|
|
|
| а). уравнение диффузии (закон Фика)
| 
|
|
| б). уравнение теплопроводности (закон Фурье)
| 
|
|
| в). уравнение внутреннего трения (закон Ньютона)
| 
|
|
| Закон Вант-Гоффа для осмоса (Р0-смотическое давление; i - изотонический коэффициент i=1+a, где a-степень диссоциации)
| 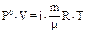
|
|
| Интенсивность потока J:
| |
|
| а). при диффузии
| 
|
|
| б). при теплопроводности
| 
|
|
| в). при осмосе
| Jос.=A×(P10-P20)
|
|
| Уравнение состояния реального газа (уравнение Ван-дер-Ваальса)
| 
|
| №
| Наименование величины или
физический закон
| Формула
|
|
| Критические параметры (параметры, определяющие критическое состояние газа)
| |
|
| а). критический объем газа
| Vк=3×в×n
|
|
| б). критическое давление
| Рк=а / (27×в2)
|
|
| в). критическая температура
| Тк=8×а / (27×R×в)
|
|
| Влажность воздуха
|
|
|
| а). абсолютная влажность
| fа=m / V
|
|
| б). относительная влажность
| 
|
|
| Коэффициент поверхностного натяжения жидкости (F-сила поверхностного натяжения; DЕ - изменение свободной энергии поверхностного слоя)
|

|
|
| Дополнительное давление, вызванное кривизной поверхности жидкости (формула Лапласа)
| 
|
|
| Высота поднятия (опускания) жидкости в капилляре (формула Жюрена-Борелли)
| 
|
|
| Дополнительное давление насыщенного пара над искривленной поверхностью жидкости (r-плотность жидкости, r0-плотность насыщенного пара)
|

|
|
| Количество теплоты, необходимое для нагревания тела
| Q=c×m×DT
|
|
| Теплоемкость одного моля вещества
|
|
|
| а). при постоянном объеме
| 
|
|
| б). при постоянном давлении
| 
|
|
| Уравнение Майера
| Ср- Сv=R; 
|
|
| Первое начало термодинамики
| DQ = DU + DA
|
|
| Применение первого начала термодинамики к газовым процессам:
|
|
|
| а). изохорический процесс
| DА=0; 
|
|
| б). изобарический процесс
| 
|
|
| в). изотермический процесс
| DU = 0; 
|