Оксиды азота относятся к умеренно опасным газам (третий класс опасности). В рабочих зонах ПДК оксидов азота в пересчете на NO2 составляет 2 мг/м3.
Содержание оксидов азота в промышленности после стадии абсорбции значительно превышает санитарные нормы. В промышленной практике применяются методы каталитического восстановления оксидов азота природным газом или аммиаком до молекулярного азота и воды. Условно по температурам восстановления процессы подразделяются на высокотемпературные (более 500°С) и низкотемпературные (менее 500°С).
Высокотемпературная каталитическая очистка.
В промышленности широкое распространение для высокотемпературной каталитической очистки нашел природный газ, при этом содержание серы в нем не должно превышать 20 мг/м3.
В качестве катализаторов применяют металлы платиновой группы, никель, медь, хром, железо, а так же сплавы Ni-Cr, Cu-Cr, Zn-Cr, нанесенные на оксиды алюминия, силикагель, керамику.
Процесс восстановления NOх протекает при 720-770°С, объемной и линейной скоростях газа 15000-25000 ч-1 и 1,0-1,5 м/с. Для достижения остаточной концентрации оксидов азота в пределах 0,002-0,008 об. % используют 10%-ый избыток природного газа от стехиометрии.
Первой стадией процесса является горение и конверсия метана кислородом:
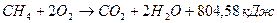 ,
,
 .
.
Выделяемое по реакциям тепло приводит к повышению температуры газа. Адиабатический разогрев газовой смеси при окислении 1% кислорода составляет 160°С. Во избежание перегрева катализатора и одновременно с этим обеспечения температуры его зажигания (450-550°С), содержание кислорода в отходящем газе поддерживают в пределах 3,2%. При восстановлении водородом содержание кислорода составляет 4,4%, так как в этом случае адиабатический разогрев составляет 130-140°С.
В процессе восстановления оксидов азота участвуют водород, СО, метан. Но с большей вероятностью с оксидами азота реагирует на катализаторе водород.
На первой стадии диоксид азота восстанавливается до монооксида азота, а затем до молекулярного азота.
 ,
,
 .
.
Аналогично взаимодействует СО с оксидами азота.
Суммарные реакции взаимодействия природного газа с оксидами азота можно представить в виде:
 ,
,
 .
.
Применение высокотемпературной каталитической очистки позволяет не только организовать замкнутый энерготехнологический цикл, но и выдавать значительное количество пара.
Низкотемпературная каталитическая очистка.
С целью снижения температуры восстановления и уменьшения расхода природного газа в качестве восстановителя предложено использовать аммиак, который при определенных условиях селективно взаимодействует с оксидами азота и не реагирует с кислородом. Восстановление оксидов азота проходит в основном до молекулярного азота:
 ,
,
 .
.
Однако в зависимости от типа катализатора возможно так же восстановление NO2 и NO до оксида азота (I) и окисление аммиака кислородом до N2 и N2O.
 ,
,
 ,
,
 .
.
Сопоставление констант равновесия основных и побочных реакций указывает на предпочтительность реакций восстановления оксидов азота аммиаком по сравнению с реакциями аммиака с кислородом.
Селективное взаимодействие аммиака только с оксидами азота обеспечивает низкотемпературное протекание процесса (200-350°С). Монооксид и диоксид азота реагирует с аммиаком с равной скоростью. Присутствующий кислород оказывает активирующее действие на реакцию образования азота.
В качестве катализаторов селективного восстановления оксидов азота испытаны многие вещества. Каталитическая активность катализаторов процесса при 200-350°С и скорости 10000 ч-1 убывает в последовательности:

К недостаткам данного способа относится трудность точной дозировки небольших количеств аммиака в газ после адсорбционных колонн и равномерного распределения его в газовом потоке.






