ЖК повреждений.
При отборе пациентов для терапии, чтобы уменьшить риск антиагрегантов, необходимо обсудить факторы риска, которые рассмотрены в предыдущем разделе, так же как сопутствующие заболевания. Предложенный подход обрисован в общих чертах в рис. 1. Учитывая относительную безопасность котерапии уменьшения риска, рассмотрение факторов риска, главным образом, относится с условиям
рентабельной помощи.
Уменьшение простагландинов - центральный механизм развития НПВП-язвы, и терапия замены
синтетическим простагландином, misoprostol, уменьшает токсичность НПВП. Небольшие данные определенно обращаются к воздействию misoprostol на AСК-связанное повреждение, хотя надо учитывать, что уменьшенный ульцерогенный эффект низкой дозы АСК сравнивался с полной дозой НПВП. В эндоскопическом исследовании misoprostol в дозе 100 мкг/день значительно уменьшал развитие эрозий у здоровых добровольцев, принимающих АСК 300 мг/день (79). Кроме того, misoprostol, как было показано, превосходил плацебо в предотвращении повторных желудочных язв среди пациентов с анамнезом желудочной язвы, которые получали низкую дозу АСК и другие НПВП (80). Однако, применение misoprostol связано с побочными эффектами, особенно диареей, и это часто приводит к прекращению лечения. Например, в исследование более 8000 пациентов с ревматоидным артритом, 20 % пациентов, получающих misoprostol в течение месяца, выбыли из лечения из-за диареи (81). Хотя это единственный препарат, разрешенный для предотвращения язв и осложнений из-за НПВП U.S. Food and Drug Administration, он редко используется из-за распространенности побочных эффектов: диареи
и спазмы в животе.
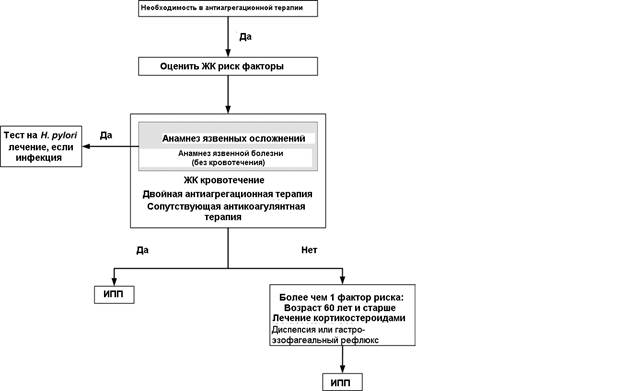
Рис. 1. Алгоритм минимизации желудочнокишечного кровотечения
Терапия ИРР, как полагают, уменьшает риск у всех пациентов; чем больше факторов риска, тем более рентабельная дополнительная терапия, вероятно, становится.
См. текст для дополнительной информации. ЖК обозначает желудочнокишечный; и ИРР, ингибитор протонной помпы.
Sucralfate, основная алюминиевая соль сахарозы octasulfate, формирует язво-заклеивающий комплекс на дуоденальных участках язвы, защищает язву и улучшая заживление; sucralfate может также блокировать активность пепсина в желудочном соке. Sucralfate, как было показано, эффективен в лечении НПВП- ассоциированных дуоденальных язв, особенно когда НПВП отменены, но лечение или предотвращение новых язв неэффективно. Его использование не рекомендуется из-за превосходящих альтернатив.
Уровень уменьшения кислотности, достигаемый традиционной дозой антагонистов H2-рецепторов (H2RAs) не предупреждает большинство НПВП-связанных желудочных язв. Есть немногочисленные данные по их использованию в комбинации с AСК. H2RA ранитидин в дозе 150 мг/день, значительно увеличивает внутрижелудочный pH и уменьшает частоту желудочных кровотечений у лиц, принимающих АСК по 300 мг/день (82). Подобные результаты были получены в 2 последующих исследованиях на добровольцах (83). Несмотря на единственное эндоскопическое исследование, демонстрирующее, что H2RAs в двойной (по отношению к обычной) доза могут быть эффективными по сравнению с плацебо, исследования, сравнивающие высокие дозы блокаторов H2 с misoprostol или ИПП для предотвращения НПВП-язв, не доступны. При дозировании два раза в день терапия ИПП есть рациональная альтернатива H2RAs в этой клинической ситуации. ИПП, как было доказано выше, в предотвращении повторения НПВП-язвы NSAID с постоянным контролем за симптомами, в значительной степени связанным с их способностью уменьшать язвы и улучшать НПВП-связанное расстройство желудка, таким образом воздействовать на качество жизни. Нет доступных рандомизированных контролируемых данных исследований, оценивающих воздействие H2 блокаторов на низкая-доза-AСК-связанное повреждение.
ИПП ингибируют париетальные клетки протонной помпы, таким образом проявляя подавляющий эффект на выделение желудочной кислоты. В эндоскопических исследованиях, включающих здоровых добровольцев, и lansoprazole и omeprazole значительно уменьшали риск гастродуоденальных повреждений у пациентов, принимающих АСК в дозе 300 мг/день (51). Эти результаты были подтверждены эпидемиологическими исследованиями, в которых сопутствующая антисекреторная терапия, особенно терапия ИПП, была связана с существенным сокращением ОР кровотечений ВПЖКТ среди пациентов, получающих низкую дозу AСК (76,84). Эти литературные источники не демонстрируют данных, что назначая дозы большие, чем стандартные один раз в сутки для ИПП терапии, как обозначено для показаний при язвенной болезни, мы получаем боллее высокий уровень подавления кислотности более частым или более высоким ежедневным дозированием. Максимальное подавление кислотности большинства ИПП
достигается, если пища употребляется в течение 30 минут после приема лекарства; это является самым важным для контролирования симптомов гастроэзофагального рефлюкса, но не известно, важно ли это для терапии предотвращения язвы.
Lansoprazole 30 мг/день сравнивался с плацебо для возвратных осложненных язв у пациентов, прнимающих АСК 100 мг/день в течение 12 месяцев после эрадикации H.pylori и заживления язв. Пациенты в группе lansoprazole значительно менее вероятно имели повторнын осложненны язвы,
предполагается, что терапия ИПП плюс эрадикация H.pylori превосходит одно только эрадикацию H.pylori (85). Хотя, у 4 из 9 пациентов в группе плацебо, у которых были повторные кровотечения, была также
неудавшаяся эрадикация или была переинфекция H. pylori, это исследование показывает, что одно только лечение антибиотиками не обеспечивает достаточную защиту для пациентов с высоким рискомЮ принимающих низкую дозу АСК. Chan и др. (86) сообщили, что среди пациентов с инфекцией H.pylori
и анамнезом ВПЖК- кровотечения терапия омепразолом была эквивалентна эрадикации H.pylori в предотвращении повторного кровотечения. Однако, продолжительность этого исследования была относительно короткой (6 месяцев). В наблюдательном исследовании Lanas и др. (87) сообщили о низкой частоте осложнений ВПЖКТ среди пациентов с высоким риском, получающих низкую дозу АСК плюс омепразол.
Как обсуждено в другом месте, преобладающий антиагрегационный эффект АСК провоцирует кровотечение из имеющихся повреждений (включая H.pylori индуцированные язвы) и создает новые язвы.
Основываясь на данных по полнодозовой терапии НПВП, терапия ИПП как полагают, склоняет чашу весов так, чтобы маленькие повреждения не прогрессируют в большие повреждения, которые могут стать симптомными (88). Важны наблюдательные исследования возникающих ЖК кровоизлияний, поскольку их конечные точки могут зарегистрировать изменения в частоте язвенных кровотечений, но они не в состоянии оценить распространенность AСК-связанных язв. Это особенно относится к интерпретации исследований случай-контроль для областей с высокой распространенностью H.pylori, которые, действительно, обеспечивают большую часть данных по этой проблеме, и которые также предполагают возможную роль терапии H2RA. Лечение H2RA, уменьшая тяжесть H. pylori – связанных язв, уменьшает
вероятность ЖК кровотечений, связанных с антиагрегантным действием терапии АСК (76,84).
Комбинация ИПП с клопидогрелем, похоже, приводит к уменьшению ЖК кровотечений (76,89). До настоящего времени, несмотря на некоторые данные in vitro, было относительно немного данных о любом клинически существенном взаимодействии между клопидогрелем и ИПП (90). Продолжающееся исследование COGENT-1(Clopidogrel and the Optimization of Gastrointestinal Events; NCT00557921) рандомизирует пациентов с болезнью коронарной артерии к AСК плюс клопидогрель в комбинации
с омепразолом 20 мг или плацебо, и надо получить новые доказательства, чтобы вернуться к этим проблемам.
7. Роль H.pylory
Рекомендация: Тестирование и эрадикация H. Pylori у пациентах с анамнезом язвенной болезни рекомендуется перед тем, как начать хроническую антиагрегационную терапию.
В отличие от результатов исследований среди не принимающих АСК НПВП, исследования типа "случай-контроль" последовательно показали, что H. Pylori важный фактор риска для язвы и язвенного кровотечения у принимающих низкую дозу АСК (38,91,92). В исследовании типа "случай-контроль" 695 неотобранных
пациентов, принимающих низкую дозу AСК, с ВПЖКТ кровотечением, инфекция H. pylori была идентифицирована как независимый риск-фактор ВПЖКТ кровотечения (ОР 4.7; 95%-ый ДИ: 2.0 - 10.9).
Другими идентифицированными факторами риска были предыдущий анамнез язвы (ОР 15.2; 95%-ый ДИ: 3.8 - 60.1), употребление алкоголя (ОР 4.2; 95% ДИ: 1.7 - 10.4), и использование блокаторов каналов кальция (Ор 2.54; 95%-ый ДИ: 1.25 - 5.14) (91).
Уменьшит ли последующий риск язвы эрадикация инфекции H.pylori у пациентов с анамнезом язвы до старта АСК – вопрос спорный. В 6-месячном рандомизированном исследовании эрадикация H.pylori против
терапии омепразолом у пациентов, принимающих АСК, с инфекцией H. Pylori и недавним анамнезом кровоточащей язвы (n=250), частота повторных язвенных кровотеченийы была сопоставима между 2 группами лечения (1.9% в группе эрадикационной терапии и 0.9% в группе омепразола; 95%-ый ДИ для
различия: -1.9% - 3.9%) (86). В другом рандомизированном испытании все принимающие АСК с инфекцией H.pylori и анамнезом язвенного кровотечения получили курс терапии эрадикации. Пациенты рандомизировались по получению lansoprazole (n=62) или плацебо (n=61) в течение 12 месяцев. Было обнаружено, что 1.6% (95%-ый ДИ: от 0% до 9%) пациентов в группе lansoprazole по сравнению с 14.8 % (95%-ый ДИ: 7% - 26%) в группе плацебо имели возвратную кровоточащую язву (85). В последнем исследовании, однако, две трети пациентов с повторным язвенным кровотечением в группе плацебо у каждого отсутствовала эрадикация H.pylori или использовался сопутствующий НПВП. Таким образом, сомнительно, что одна только эрадикация H.pylori уменьшила бы риск язвенного кровотечения у пациентов с высоким ЖК риском, принимающих АСК. Однако, профилактика ИПП эффективно предотвращает повторное ВПЖКТ кровотечение из-за низкой дозы АСК, несмотря на отсутствие эрадикации H.pylori
и сопутствующий приемиспользование не-АСК НПВП.
Более свежее исследование, и наибольшее до настоящего времени, несколько разъясняет эту проблему. В этом проспективном когортном исследовании частота язвенного кровотечения сравнивалась в 3 различных когортах пациентов, принимающих низкую дозу АСК, а именно, пациенты без предшествующего анамнеза язвы, которые только начали принимать АСК (n=548), принимаюшие АСК с предшествующим язвенным кровотечением и инфекцией H.pylori, у кого была успешная эрадикация H.pylori (n=250), и H.pylori –негативные пациенты, принимающие АСК, которые имели предшествующее язвенное кровотечение (n=118). Все пациенты получали низкую дозу АСК (меньше чем 160 мг ежедневно) без гастропротективных препаратов. После середины исследованияредин (48 месяцев), пересчитанного на год, частота язвенного кровотечения в этих 3 группах была 0.5%, 1.1% и 4.6%, соответственно (93). Таким образом, настоящие данные позволяют предположить, что подтвержденная эрадикация H.pylori у пациентов, принимающих
АСК с предшествующим язвенным кровотечением достоверно и существенно уменьшает риск повторного кровотечения. Выгодна ли эта стратегия в ситуация ОКС неизвестно.
A. Диагностика H.pylori
Недавно изданные руководящие принципы ACG представляют всестороннюю информацию о H.pylori (94). Неинвазивное тестирование H. pylori в настоящее время рекомендуется пациентам не нуждающимся в эндоскопии. Две главные категории неинвазивных тестов сейчас доступны: тесты, которые идентифицируют активную инфекцию, и тесты, которые обнаруживают антитела (контакт). Это
различие важно потому что антитела (то есть, позитивный иммунный ответ), указывают только на присутствие H. pylori в некоторое время. Тесты на антитела не дифференцируют ранее эрадицированные и в настоящее время активные H. pylori. По сравнению с тестами на активную инфекцию, тесты на антитела
более просто осуществляются, обеспечивают более быстрый результат, и менее дороги. Однако, есть большая вероятность, что положительный тест на антитела отражает активное уменьшения инфекции так же как ранее эрадицированные H.pilori. Успешно леченные пациенты включают как пациентов, получающих
антибиотики специально для H.pylori, так и пациентов с недиагностированной инфекцией H. pylori, у которых была эрадицирована H.pylori антибиотиками, назначенными для другой инфекции; более редка спонтанная эрадикация H.pylori.
Cерологические тесты на H. pylori, которые обнаруживают антитела к H.pylori имеют чувствительность и специфичность приблизительно 90%. В популяциях с низкой распространенностью болезни, положительная прогнозирующая ценность теста падает драматически, приводя к ненужному лечению. Сделанные в кабинете серологические тесты менее точны, чем сделанные в лаборатории фермент-зависимыми иммуносорбентами, но имеют преимущество скорости получения результата в пределах 30 минут. Серологические тесты могут использоваться только для первичой диагностики, потому что уровень антител часто остаются поднятым после устранения H.pylori. Серологические тесты не должны использоваться для подтверждения излечения после курса эрадикации H.pylori.
B. Тесты на активные H. pylori
Тесты на активные H. pylori включают фекальный антиген H.pylori и мочевина-дыхательный тест (МДТ). Для МДТ пациент пьет препарат, содержащий 13C или 14C- меченые мочевиной. Бактерии H. pylori в желудке метаболизируют эту мочевину; кровоток адсорбирует углерод, и направляется в легкие, которые выдыхают это как углекислый газ. Изотоп углекислого газа измеряется, чтобы определить присутствие или
отсутствие H.pylori. Этот тест имеет чувствительность и специфичность больше 90% для активной инфекции. Многие препараты могут неблагоприятно повлиять на точность МДТ. Перед любым видом
активного тестирования нужно отменить антибиотики и висмут за, по крайней мере, 4 недели, ИПП надо отменить за 7 дней, и пациент должен не кушать в течение, по крайней мере, 6 часов.
У теста фекального антигена, как сообщают, чувствительность и специфика больше чем 90% у невылеченных пациентов с подозреваемой инфекцией H. pylori. Требуется проба фекалий размера желудя осуществимая любым клиницистом или пациентом. Этот тест должен быть выполнен в лаборатории обучаемым персоналом. Основанный на доступных данных, фекальный тест антигена может быть
используемый попеременно с МДТ, чтобы идентифицировать H.pylori перед лечением антибиотиком.
C. Обработка пилорусов H.
Необходимо выбрать наиболее эффективную терапию и наименьшими побочными эффектами. ИПП в пробирке действуют против H.pylori. ИПП плюс кларитромицин (500 мг) плюс амоксициллин (1 г) или метронидазол (500 мг) назначенные два раза в день продемонстрировали частоту эрадикации около 90%, если используются в течение 10 - 14 дней. Амоксициллин предпочтительнее для пациентов, которые принимали метронидазол ранее. Метонидазол предпочтительнее для пациентов, имеющих аллергию на пенициллин. “Основанная на висмуте тройная терапия” является менее дорогостоящей альтернативой:
(висмута субсалицилат) 2 таблетки ежедневно, метронидазол 250 мг четыре раза ежедневно и тетрациклин 500 мг четыре раза ежедневно в течение 2 недель – наилучшим образом изученная, очень эффективная анти-H.pylori терапия (больше или равно 85%-ой эрадикации). Продолжительность и мультилекарственная суть этого режима назначения уммньшала комплаэнс, приводя к возможной неудачной эрадикации. Из-за сложности тестирования и лечения H. pylori, несмотря на очевидную ценность как единственной терапии, уменьшающей риск, больше поддерживается одна только терапии ИПП из-за ее простоты и эффективности,
даже для H.pylori- зараженных пациентов, как показывает исследование Lai и др. (85).
8. Прекращение антиагрегантной терапии из-за кровотечения
Рекомендация: Решение о прекращении АСК при остром язвенном кровотечении должно быть принято индивидуально, основано на оценке сердечного риска и ЖК риска, чтобы различить возможность тромбического и геморрагического осложнений.
Пациентам, получающим низкую дозу АСК, у которых возникает ВПЖКТ кровотечение, часто советуют прекратить АСК до заживления язв. Специфическая дилемма возникает у пациентов, требующих
непрерывной антиагрегантной терапии (например, с ОКС, острой церебро-васкулярной недостаточностью или недавней чрезкожной реваскуляризацией), и у которых возникает язвенное кровотечение. Может ли быть АСК повторно назначена немедленно после достигнутого эндоскопического гемостаза, при условии, что длительное прекращение АСК увеличивает тромбический риск у пациентов с нестабильной сердечно-сосудистой болезнью?
Гемодинамическая неустойчивость и гемостатические изменения, вызванные острым кровотечением, могут в дальнейшем увеличить риск тромбоза в отсутствии антиагрегационной терапии. С другой стороны, продолжение приема АСК при остановленном остром язвенном кровотечении может вызвать повторное кровотечение. Нет данных, что не-AСК антиагрегантные лекарства, такие как клопидогрель, уменьшат этот риск кровотечения при сохраняющейся острой язве (73). Мета-анализ рандомизированных исследований показал, что внутривенное введение ИПП после эндоскопической терапии язвенного кровотечения уменьшало риск возвратного кровотечения (ОР 0.39; 95%-ый ДИ: 0.18 - 0.87) и потребность в операции (ОР 0.61; 95%-ый ДИ: 0.40 - 0.93) (95). Однако, нет исследований, разрешающих продолжение антиагрегантной терапии во время периода исследования. Исследование in vitro предположило, что гемостаз зависит от pH и стабильности склеивания тромбоцитов (96). Антиагреганты могут негативировать кровоостанавливающий эффект ИПП, ослабляя формирование агреганта тромбоцитов.
До настоящего времени, только 1 небольшое, двойное слепое, рандомизированное исследование оценило эффект раннего повторного назначения АСКу пациентов с сердечно-сосудистыми болезнями, которые сопровождались острым язвенным кровотечением (97). На время промежуточного периода у 113 пациентов, принимающих АСК при церебро-васкулярной или сердечно-сосудистой болезни, развилось кровотечение из гастродуоденальных язв, подтвержденное эндоскопией. После эндоскопического контроля активного кровотечения, они раномизированно принимали AСК 80 мг один раз в день ежедневно или плацебо. Всем пациентам назначалась непрерывная инфузия ИПП в течение 72 часов и затем стандартная доза перорального ИПП течение 8 недель. Конечные точки включали возвратное язвенное кровотечение в течение 30 дней и общую смертности. 2 группы были сопоставимы по возрасту (средний возраст 74 года
против 73 лет), полу (мужчины: 62% против 69%), предшествующему язвенному анамнезу (6.9% против 3.7%), сопутствующему использованию НПВП (12% против 11%), локации(гастродуоденальные язвы: 28 против 32), и диаметру язв (1.13 см против 1.20 см). Возвратное язвенное кровотечение в течение 30 дней возникло у 18.9% пациентов, принимающих AСК, и у 10.9 %, получающие плацебо (p=0.25). В группе AСК 1 пациент (1.7%) умер от повторного сердечно-сосудистого события. В группе плацебо, 8 пациентов (14.5%) умерли (5 повторных сердечно-сосудистых событий, 2 повторных кровотечения, и 1 пневмония; p=0.01 против группы AСК). Эти результаты показали, что прекращение приема АСК было связано с существенным увеличением общей смертности (смертность от всех причин), большинство смертельных случаев произошло из-за повторных сердечно-сосудистых событий. Отмечалась тенденция к более высокой частоте повторных язвенных кровотечений в группе АСК (18.9%), которая предполагает, что дополнительный ИПП после эндоскопической терапии не мог эффективно предотвратить раннее ре-кровотечение, вызванное AСК.
9. Эндоскопия у пациентов с мoно или двойной агрегационной терапией
Рекомендация: Эндоскопическая терапия может быть выполнена у пациентов с высоким сердечно-сосудистым риском на двойной антиагрегантной терапии, и сотрудничество между кардиологом