Вариант 5
1 1 1 1 1 (... 1 - 1_ J_ 1,-1
1 1 1 1
l J!, l--rГL- - r-
' с -r--
1.R1
.,_ r:1I,u!.
| - |
1 ---
-- - - - ' ч!=+-1 1
-- - [ -(-
\) ·q,--
| I |
1 1v - r
| =-=- |
| -: ' 1 |
г
-:=::: L
с
['\. д
'/' tl
1
,.,
1 1 '
| • |
1 .е
!':\
| = |
-
1.:.J 1
3 ' f(r-- с
"
J
' () п 1
1 Х' 1._ с
"' r-
.
·1,1 h
| -:-·- |
| v |
::.
с...1. '1
| ... ". - |
.1 1
| ·'. |
| ) ' w - r |
| ' |
lA л И/ \)
-,1'1 l.(_,t1 1'
r-- \..
\
r--
i--
)
r-- }
| ' |
!---". v
| . |
!---" r, 1' i а
'\I 11
 ..---1-·-
..---1-·-
........' ·· -'
-11 r\
3) Белковые аминокислоты – это α-АК, L-стереохимического ряда и на них есть код. Существует 20 белковых аминокислот. H2N-CH(R)-COOH
Классификация АК по Ленинджеру:
І. АК с неполярными гидрофобными R- группами (R-гр. не содержат никаких ФГ) n=8
Сюда относят: аланин, валин, лейцин, изолейцин, метионин, фенилаланин, триптофан, пролин.
ІІ. АК с полярными гидрофильными R-группами
а) R-группы незаряжены (есть –ОН, -SH, -СОNH2 обладающие слабыми кислотно-основными свойствами) – это глицин +NH3-CH(H)-COO-, серин, треонин
б) R-группы (-) заряжены(есть COOH) – аспартат, глутамат
 в) R-группы (+) заряжены(есть атом N со свободной электронной парой)- этолизин, аргинин, гистидин 4) ß
в) R-группы (+) заряжены(есть атом N со свободной электронной парой)- этолизин, аргинин, гистидин 4) ß
5) Гомополисахариды ~ это полимеры, мономерной единицей которых является один и тот же моносахарид. В природе: Крахмал – синтезируется в растениях Целлюлоза (клетчатка) – тоже, Гликоген – синтезируется в печени и мышцах, а также в других тканях,Декстраны – бактериального происхождения или синтетические,
Фруктаны, маннаны, Пектиновые вещества – пищевые волокна фруктов, овощей
Хитин – роговые оболочки насекомых,
ракообразных, в некоторых грибах.
Отличие крахмала от гликогена:
Крахмал:
Две фракции: (Растворимая амилоза (20 %) Нерастворимый амилопектин (80 %))
Амилоза – линейный гомополисахарид, построенный из D-глюкозы, соединенной α-1,4 гликозидными
связями (как в мальтозе). Вторичная структура – спираль.
Амилопектин – разветвленный гомогликан, состоит из D-глюкозы, соединенной α-1,4 и α-1,6 гликозидными связями
Гидролиз
–Кислотный
–Ферментативный
Продуктом кислотного гидролиза является глюкоза
Ферментативный – идет под действием ферментов класса гликозидаз. Под действием амилазы образуется мальтоза.
Гликоген:
По строению похож на амилопектин. Однако, α-1,6-гликозидные связи встречаются чаще (через 3–5
МС-звеньев) и поэтому молекула имеет еще большую молекулярную массу.
В организме гликоген выполняет роль резервного источника энергии. Основной процесс расщепления –
фосфоролиз под действием фосфорилаз
6) Комплексы жиров с белками (л и попр о теиды) являются важными клеточными компонентами, присутствующими как в клеточной мембране, так и в митохондриях; они также служат средством транспортирования липидов в токе крови. Холестерин входит в состав всех мембран, он регулирует текучесть мембран; На внешней стороне мембраны обычно находятся гликопротеины и гликолипиды, участвующие в молекулярном распознавании; Мембраны асимметричны
Функции мембран:
Электроизоляционная (миелиновая оболочка нервов) Избирательная проницаемость
Активный транспорт
Упорядоченность ферментативных цепей и выработка энергии Передача информации
- рецепторная
- трансдукция и усиление сигнала
- межклеточное взаимодействие и межклеточная сигнализация
Вариант 6

3) Пептиды:
Олигопептиды ( 2 – 10 АК)
АДГ, -окситоцин, либерины, статины, нейропептиды, кинины крови глутатион, Гликопролины
Полипептиды (10 – 50 АК М.м. до 5000)
АКТГ, гастрин, секретин, глюкагон, факторы роста
Белки (> 50 АК. М.м. > 5000)
Простые: Инсулин, СТГ, АХЭ
Сложные: Гликопротеин, Нуклеопротеины, Липопротеины,
Фосфопротеины, Гемпротеины,Металлопротеины
4) Гетерополисахариды - полисахариды, в структуре которых характерно наличие двух или более типов мономерных звеньев. Сюда относятся гиалуроновая кислота(формула на обороте),
Гиалуроновая кислота – вырабатывается фибробластами соединительной ткани и является основным
органическим компонентом межклеточ ного матрикса.
Хондроитинсульфаты (ХИС ы ) – вырабатываются там же, но их больше в твердой ткани (хрящах, костях, зубах).
Гепарин – вырабатывается тучными клетками печени, легких, сосудов.
Свойство и роль:
Гиалуроновая кислота обладает самой высокой молекулярной массой и как самый большой гидрофильный
полимер, хорошо связывает воду, образуя вязкие растворы и упругие гели. Поэтому гиалуронат является: Биологическим депо воды, Биологическим фильтром, Биологическим клеем, цементом, Биологической смазкой
Благодаря множеству карбоксильных групп гиалуронат и ХИСы являются полианионами Как полианионы, они выполняют роль биологических рессор и биологических опор. Так, в хрящах гиалуроновая кислота электростатически комплексируется с белками, к которым ковалентно (О- и N-гликозидными связями) «пришиты» ХИСы, и образуются протеогликановые агрегаты (структура «ерша»)
Роль Хисов: Помимо амортизационной функции ХИСы, будучи более сильными полианионами по сравнению с гиалуроновой кислотой, хорошо связывают катионы металлов Ca2+, Na+ и являются депо этих катионов в хрящах, костях и зубах. Из этих депо Cа2+ идет на минерализацию твердых тканей.
Роль Гепарина: его деятельность связана с процессами узнавания.
Гепарин вырабатывается тучными клетками печени, легких, сосудистой стенки, матки, в органах ЖКТ, молочной железе, миндалинах. Он обнаруживается на поверхности многих клеток, в крови, в лимфе, а также внутри тучных клеток, где связывает гистамин. Снижает вязкость крови.
5) Нуклеозиды – это β-N-гликозиды, у которых в качестве сахарной части выступает пентоза (обычно рибоза илѝ 2′-дезокси рибоза), а в качестве несахарной части (т.е. агликона) – азотистое основание гетероциклического ряда (чаще пуриновое или пиримидиновое).
Нуклеотиды – это фосфорные эфиры нуклеозидов
Нуклеотиды делятся на МОНОНУКЛЕОТИДЫ (Нуклеозид монофосфаты, Нуклеозид дифосфаты Нуклеозид трифосфаты, Цикло нуклеотиды, Флавин мононуклеотиды)
ДИНУКЛЕОТИДЫ(НАД НАДФ ФАД),
ПОЛИНУКЛЕОТИДЫ(ДНК, РНК)
Роль: Все мононуклеотиды, кроме ФМН, могут выполнять регуляторную роль
Кроме того, нуклеозидтрифосфаты являются макроэргами и субстратами для биосинтеза нуклеиновых кислот; Макроэргами являются и нуклеозиддифосфаты; Циклонуклеотиды являются внутриклеточными усилителями и посредниками (мессенджерами) действия многих гормонов.
6) Представление о желчных кислотах и их функциях:
Желчные кислоты эмульгируют жиры в кишечнике, активируют панкреатическую липазу, способствуют всасыванию длинноцепочечных жирных кислот в тонком кишечнике. В печеночных протоках желчные кислоты вместе с другими поверхностно-активными веществами (ПАВ) – фосфолипидами – солюбилизируют труднорастворимые соединения в мицеллы и способствуют их выведению из организма, тем самым, препятствуя образованию камней.
Вариант 7

3) Енольную форму пептидной группы обнаруживает биуретовая реакция, которая проводится с CuSO4
+ NaOH. При этом р-р окрашивается в интенсивный фиолетовый цвет благодаря образованию комплексного соед.
Биуретовая реакция — качественная на все без исключения белки, а также продукты их неполного гидролиза,
которые содержат не менее двух пептидных связей. Биуретовая реакция обусловлена присутствием в белках пептидных связей, которые в щелочной среде образуют с сульфатом меди (ІІ) окрашенные медные солеобразные комплексы. Биуретовую реакцию дают также некоторые небелковые вещества,
например биурет (NH2-CO-NH-CO-NH2), оксамид (NH2CO-CO-NH2), ряд аминокислот (гистидин, серин, треонин, аспарагин).
 4) В хрящах гиалуроновая кислота электростатически комплексируется с белками, к которым ковалентно (О- и N-гликозидными связями) «пришиты» ХИСы, и образуются протеогликановые агрегаты (структура
4) В хрящах гиалуроновая кислота электростатически комплексируется с белками, к которым ковалентно (О- и N-гликозидными связями) «пришиты» ХИСы, и образуются протеогликановые агрегаты (структура
«ерша»)
5)
Расположение четырех типов нуклеотидов в цепях ДНК несет важную информацию. Набор белков (ферментов, гормонов и др.) определяет свойства клетки и организма. Молекулы ДНК хранят сведения об этих свойствах и передают их в поколения потомков. Другими словами, ДНК является носителем наследственной информации, обеспечивает хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. Основная роль ДНК в клетках — долговременное хранение информации о структуре РНК и белков.
6) Гликопротеины и гликолипиды- 1) Они находятся на внешней поверхности всех клеток (в том числе эритроцитов, лейкоцитов и тромбоцитов) 2) Они растворены в плазме крови.–Это компоненты свертывающей системы крови, все транспортные белки (кроме альбуминов) 3) Они растворены в других биолог. жидкостях: в слезах, в слюне 4) В слезистых секретах 5) В матриксе соед ткани 6) РНК вирусы
У-цепи ГП и ГЛ содержат до 20-25 МС-звеньев
–Разветвленные (на концах или в начале)
–Нерегулярно построены (нет закономерности в построении)
–На концах обычно сиаловые кислоты или L-фукоза (6-дезокси-L-галактоза)
–Внутри цепи – гексозамины, N-ацетилгексозамины, манноза, галактоза Связи с белком или керамидом – О- или N-гликозидные.
Вариант 8

3) Роль пептидов в организме:
Межклеточные регуляторы; участвуют в окислительно-восстановительнывх реакциях (глутатион); осуществляют транспорт аминокислот через стенку кишечника(н-глутамильный цикл с участием глетаниона); поддерживают рН мышечных клеток; антибиотики с различным механизмом действий(каналообразователи, ионофоры, связываются с ДНК-изменение геноме-нарушение синтеза белка); обладают вкусовыми качествами; пептиды-яды, токсины змей, рыб, скорпионов, пчел, грибов; особая регуляторная активность обнаружена в семействе глипролинов(состоящие из гли п про).
4) Физико-хим свойства НК:
Поглощают свет в УФ-области; Как полимеры они подвергаются денатурации в щелочной, кислой среде и при повышении температуры; Уже слабое нагревание приводит к разрушению водородных связей и гидрофобных взаимодействий. При 95°С две цепи ДНК расходятся, что говорит о процессе плавления; Денатурация приводит к повышению вязкости растворов; Денатурированная ДНК легко подвергается гидролизу (кислотному, щелочному, ферментативному); ДНК легче гидролизуется, чем РНК; НК легко связываются с катионами металлов, образуя хелаты; Не содержат склонных к окислению группировок и в мягких условиях не окисляются; Окислительной модификации подвергаются НК и в присутствии свободных радикалов (ȮН, ȮR, ȮОН, О2), а также пероксинитрита ONO2 и хлорноватистой кислоты; Свободнорадикальному окислению ДНК отводится ведущая роль в процессах старения, канцерогенеза, ауто- и иммуногенеза,а также в возникновении инсулинустойчивого (инсулинонезависимого) сахарного диабета. Кроме окислительной модификации оснований существуют и другие типы повреждений ДНК (разрывы нитей, межнитевые сшивки ДНК-ДНК, сшивки ДНК-белок, образование участков, лишенных оснований).
Летальное и мутагенное действие на организм оказывает УФ-излучение, т.к.
–запускает процесс свободно-радикального окисления, может приводить к образованию циклобутановых структур между двумя пиримидиновыми азотистыми основаниями (Т, Ц). Циклобутановые структуры блокируют процесс репликации ДНК.
Структура НК
Первичная – последовательность нуклеотидов в полинуклеотидной цепи, организованная с помощью 3ꞌ,5ꞌ-ФЭС
Вторичная – у ДНК – двойная спираль, (закрученная вокруг общей оси) с антипараллельными, но не
идентичными полинуклеотидными цепями. Стабилизируется водородными связями между комплементарными азотистыми основаниями, а также стэкинг взаимод-ми между плоскими циклами азот.оснований.
Третичная структура имеет место только у ДНК – это сверхскрученная упаковка двойной спирали
вокруг белков гистонов. Комплексируясь со щелочными белками гистонами, ДНК формирует метафазную хромосому.
5) Неомыляемые липиды- группа, включает предельные углеводороды и каротиноиды, а также спирты. Они делятся на СТЕРОИДЫ (содержат стеран)- стерины (С27),желчные кислоты (С24) Гормоны(кортикостероиды (С21), гистогены (С21), андрогены (С19),эстрогены (С18)),сердечные гликозиды. Изопреноиды (содержат изопреновые звенья)-содержатся в витаминах А, Е, К, Q, в терпенах и терпеноидах. Эйкозаноиды (производные эйкозантетраеновой кислоты – арахидоновой к- ты)- содержатся в простаноиды (простагландины, тромбоксаны), лейкотриены, липоксины. Неомыляемые липиды не подвергаются гидролизу.
Роль холестерина: Входит в состав всех мембран клеток и внутриклеточных структур
Является источником для синтеза: витамина D, стероидных гормонов, желчных кислот в печени, является структурным компонентом сердечных гликозидов.
6) Роль липидов в медицине: входят в состав таких лекарственных форм, как кремы, эмульсии,
некоторые средства личной гигиены; Знание биохимии липидов необходимо для понимания многих областей современной медицины, например проблем ож ир ения, ат ерос к ле роза. Важное значение имеет также понимание роли различных полиненасыщенных жирных кислот в рац иона льн ом п итан ии и для поддержания здоровья, как носители лекарств липосомы наиболее широкое применение получили в экспериментальной онкологии; Комплексы жиров с белками (л ипопр о теиды) являются важными клеточными компонентами, присутствующими как в клеточной мембране, так и в митохондриях; они также служат средством транспортирования липидов в токе крови.
Вариант 9
3) Структурная организация белковой молекулы
1. Первичная структура
Это последовательность (порядок чередования) аминокислот в полипептидной цепи
Связи, стабилизирующие эту структуру – пептидные
Форма – зигзагообразная цепь
2. Вторичная структура
Это регулярное (закономерное) расположение полипептидной цепи в пространстве
Связи, стабилизирующие эту структуру – водородные между пептидными группами
Форма: α-спираль или β-складчатый лист или спираль коллагена
3. Тетичная структура
Это дальнейший специфический способ укладки полипептидной цепи в пространстве
Связи, стабилизирующие эту структуру – водородные между боковыми R-группами аминокислот (это отличает третичную структуру от вторичной)
–Ионные
–Гидрофобные взаимодействия
–Дисульфидные (наиболее прочные)
Форма – клубок (глобула) или нить (фибрилла).
4. Четвертичная структура
Некоторые белки собираются в олигомерный комплекс из нескольких субъединиц (протомеров) с помощью
нековалентных связей.
Пространственное расположение субъединиц в олигомерном белке – это и есть 4-ая структура. Субъединичная (или четвертичная) структура очень важна для аллостерической регуляции ферментов, а также регуляции экспрессии генов.
Конформация – это форма молекулы, определяемая ее вторичной и третичной структурой. Не является жесткой и зависит от наличия кофакторов в окруж. среде.
Домен – фрагмент ПП-цепи, сходный по своим свойствам с самостоятельным глобулярным белком. Домен автономен, но вместе с другими доменами в данном белке нацелен на
выполнение одной задачи.
HO * H O
O CH
H
H * OH
O H
фуранозный цикл
H OH
O
HO H
*
O H * OH
4) пиранозный цикл
5) Мальтоза относится к дисахаридам типа гликозидо-глюкоз и составлена из двух остатков а-D- глюкопиранозы, соединенных гликозидной связью в положениях 1,4. Связь такого типа называют а-1,4- гликозидной связью. Мальтозу получают при гидролитическом расщеплении крахмала с помощью специфического фермента, которым очень богаты прорастающие зерна ячменя
6) Липиды – это гидрофобные органические соединения природного происхождения, не растворяются в воде, но растворяются в органических растворителях (спирт, эфир, бензол, толуол и т.д.).
Биологическая классификация(основана на функциях липидов):
Липиды делятся на: жиры (энергетическая ф-ция), липоиды (мембранная), биологически активные вещества
(регуляторная).
Липиды делятся на:
Омыляемые (содержат сложно-эфирную связь): они в свою очередь делятся на простые и сложные
Простые (два компонента)- жиры, стериды, воски, твины
Сложные (более двух компонентов) – фосфодипиды (содержат ФК) и гликолипиды (не содержат ФК, но содержат У).
Неомыляемые (не содержат сложно-эфирную связь).
Билет 10

3) Ф изи ко -х имич ес кие с во йст ва бел ко в
Набухаемость (ограниченная и неограниченная)
Растворимость в воде (касается только тех белков, у которых на поверхность выступают гидрофильные группы)
Осаждаемость (или коагуляция) Электрофоретическая подвижность Буферное действие
Лиофилизация Изоэлектрическая точка
Оса ждение бел ко в
Высаливание – осаждение без нарушения структуры белка: путём отнятия гидратной оболочки и
 нейтрализации заряда на поверхности с помощью солей щелочных и щелочно-земельных металлов, а также сернокислого аммония
нейтрализации заряда на поверхности с помощью солей щелочных и щелочно-земельных металлов, а также сернокислого аммония
Денатурация – разрушение всех структур белка, кроме первичной.
Денатурирующие факторы:
- высокие температуры
- УФ и ионизирующее излучение
- встряска
- кислоты и щелочи
- соли тяжелых металлов
- спирт, ацетон при длительном воздействии
4) à
5)  ß
ß
6) Роль белков в организме
Ферментативная
Рецепторная (рецепторы для гормонов и факторhов роста); Регуляторная Структурно-образовательная (построении
мембран клеток и межклеточного матрикса) Опорная (коллаген и неколлагеновые фосфопротеины служат матрицами для минерализации кости); Защитная (участие в иммунных реакциях, в свертывании крови) Энергетическая
2) при взаимодействии хлорангидридов кислот с
концентрированным водным раствором аммиака:
3)  И зо эл ект р ич ес ка я т о ч ка бел ко в
И зо эл ект р ич ес ка я т о ч ка бел ко в
Взаим бенз к-ты и ра-р аммиака

 Значение рН среды, при котором суммарный заряд на поверхности белка равен нулю, называется изоэлектрической точкой - pI
Значение рН среды, при котором суммарный заряд на поверхности белка равен нулю, называется изоэлектрической точкой - pI
При рН < pI, молекула белка будет заряжена положительно
При рН > pI, заряд молекулы белка будет отрицателен
5) ß

6) О тл и чи я ДНК и РНК
ДНК: сахар – д-рибоза; азотистое основание: А, Г, Ц, Т; длина молекулы – 3-5 см; молярная масса – 10 в 11 степени; вторичная структура – двойная спираль; локализация – в ядре (немного в митохондриях);
функция – хранение и передача наследственной информации.
РНК: сахар – рибоза; азотистое основание: А, Г, Ц, У; длина молекулы- до 0,01 см; молярная масса – 10 в 4- 10 в 6 степени; вторичная структура – одна цепь, где чередуются спиральные и неспиральные участки;
Локализация – в цитозоле (немного в митохондриях); функция – реализация наследственной информации.




 2)
2)
3) Белки также, как и аминокислоты можно
◆ фосфорилировать,
◆ ацетилировать
◆ ацилировать
◆ гликозилировать
◆ комплексировать с катионами металлов и т.д.
•Реакции гидролиза
• Цветные реакции (биуретовыя, нингидриновая, ксантопротеиновая, нитропруссидная и др.)
5)
6)
 1) CH3CHO --(H2,Kat)--> C2H5OH --(сжигание)--> CO2 + H2O (этаналь. Этанол, углекислый газ)
1) CH3CHO --(H2,Kat)--> C2H5OH --(сжигание)--> CO2 + H2O (этаналь. Этанол, углекислый газ)
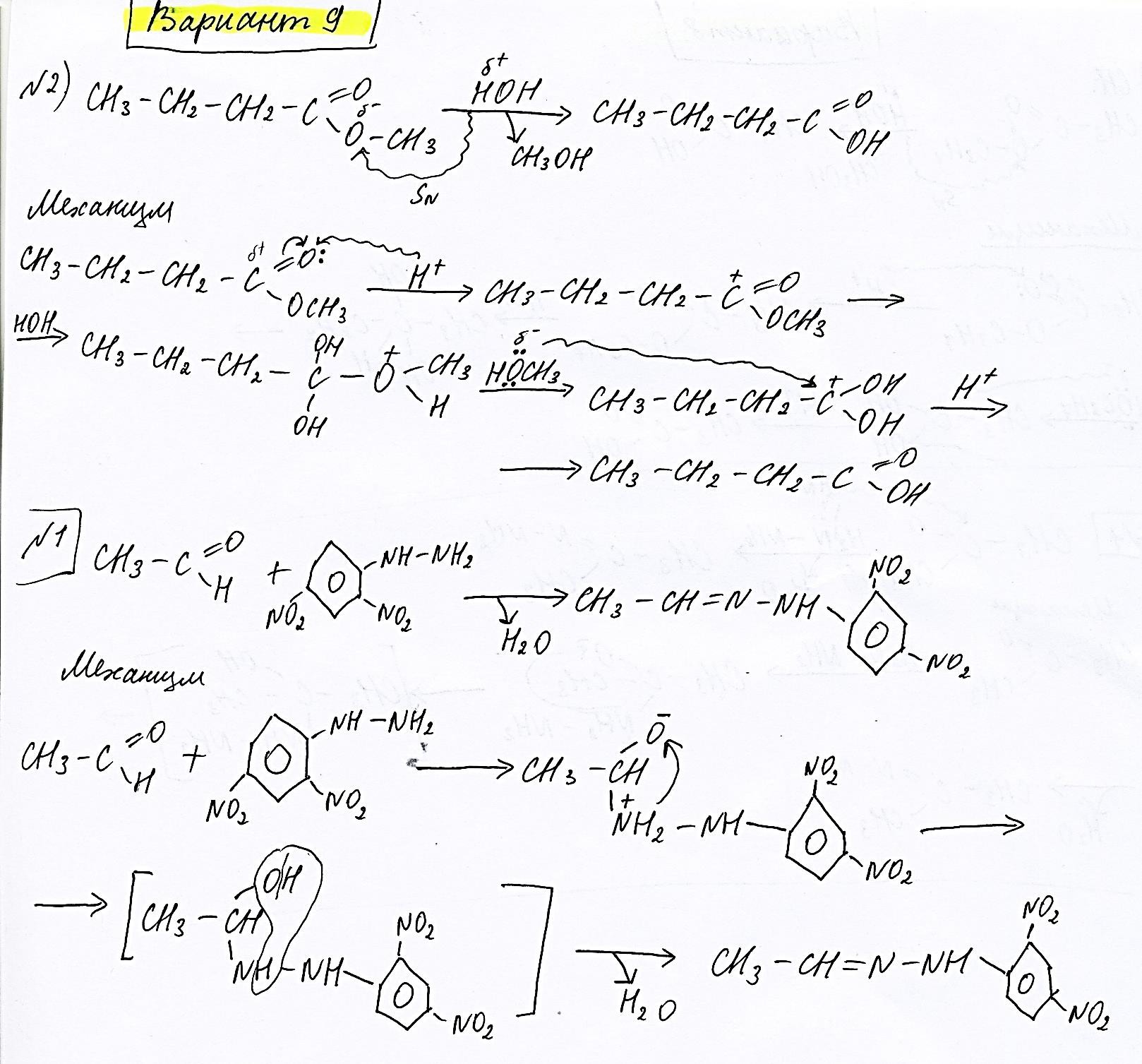
 5) Формула АТФ
5) Формула АТФ
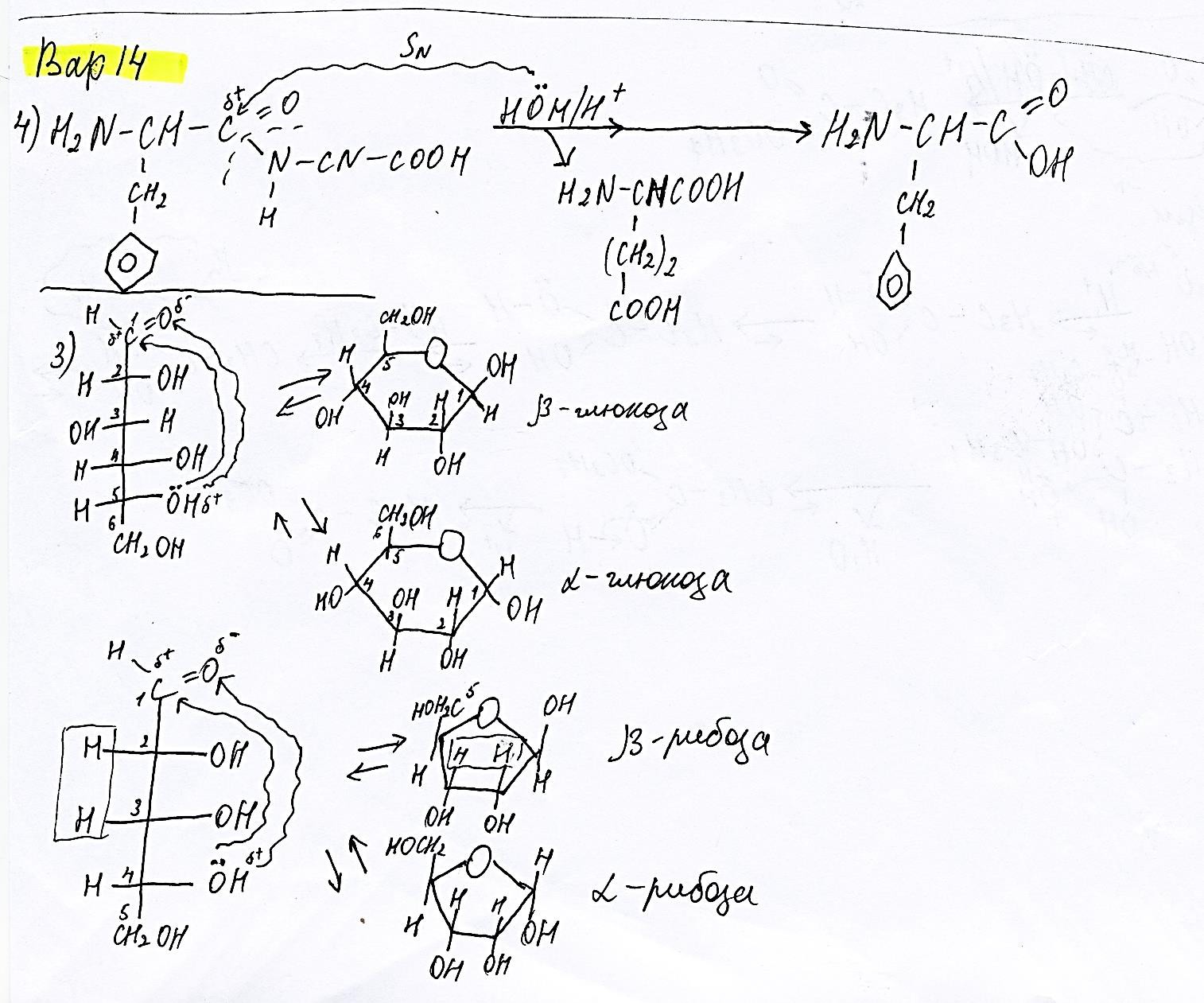
3) Кольчато-цепная таутомерия моносахаридов заключается в существовании кольчатых (циклических) форм и цепной (т. е. с открытой углеродной цепью) формы моносахарида, находящихся в динамическом равновесии.
6) Сфингофосфолипиды (сфингомиелина) состоят из церамида, содержащая один остаток длинноцепочечных аминоспирты сфингозина и один остаток жирной кислоты и гирофильного радикала, присоединенного к сфингозина фо сфо ди ест ер ним связь ю. В качестве гирофильного радикала часто выступает холин или этаноламин.
Сфингомиелин встречаются в мембранах различных клеток, но богатый
на них нервная ткань, особенно высокое содержание этих веществ в миелиновой оболочке аксонов, откуда и происходит их название.
2) Гидролиз никотинамида
Чем меньше основность уходящей группы, тем более лучшей уходящей группой она является. Хлорид-ион является слабым основанием по сравнению с амид- ионом (NH2-) или гидроксид-ионом (OH-), поэтому хлорид-ион является гораздо более лучшей уходящей группой по сравнению с амид-ионом или гидроксид- ионом. Поэтому хлорангидриды обладают большей реакционной способностью, чем амиды и кислоты в реакциях SN у Сsp2