С)от давления в системе
D)от концентрации реагирующих веществ
Е)от давления и температуры
$$$ 363
Укажите вещество электролит
A)Cu
B)CuO
C)O2
D)CuSO4
E)NO
$$$ 364
Сколько катионов образуется при диссоциации сульфида аммония 3
$$$ 365
Укажите вещество неэлектролит:
А)ZnCI2
B)Na2SO4
C)CrCI3
D)MnO
E)Cu(NO3) 3
$$$ 366
В каких единицах изменяется ЭДС(Е) гальванического элемента?
А)кулонах
В)градусах Кельвина
С)калориях
D)вольтах
Е)амперах
$$$ 367
Какой из металлов может вытеснить водород из воды?
А)калий 1
В)медь
С)серебро
D)золото
Е)платина
$$$ 368
Квантовое число, определяющее форму электронного облака в пространстве называется:
А)главным
В)спиновым
С)магнитным
D) орбитальным
Е)не знаю
$$$ 369
Используя закон действия масс определите скорость реакции 2A + B® C:
А) v = k [A] [B];
В) v = k [C];
С) v = k [A];
D) v = k [A]2 [B];
Е) v = k [B].
$$$ 370
Какая из ниже перечисленных реакций относится к окислительно-восстановительным реакциям:
А) CaO + H2O ® Ca(OH)2;
В) SO2 + H2O ®H2SO3;
С) CaCO3 ® CaO + CO2;
D) 2KMnO4 + 16 HCl ® 2MnCl2 + 5Cl2 + 8H2O + 2KCl;
Е) H2SiO3 ® H2O + SiO2
$$$ 371
Чему равен рН раствора, если концентрация (OH-) -ионов равна 10-12 моль/л? 2
$$$ 372
Чему равен рН, если концентрация (OH- ) ионов равна 10-13 моль/л1? 1
$$$ 373
При каком соотношении ИП и ПР раствор будет пересыщенным:
А) ИП > ПР;
В) ИП= 0;
С) ПР= 0;
D) ИП=ПР;
Е) ИП< ПР.
$$$ 374
Используя закон действия масс определите скорость реакции 2A+3E ® F:
А) v = k [E]3;
В) v = k [A]2 [E]3;
С) v = k [F];
D) v = k [A]2;
Е) v = k [A] [E].
$$$ 375
Из ниже перечисленных солей гидролизу не подвергается:
А) CH3COOK;
В) (NH4)2SO4;
С) CH3COONa;
D) K2SO4;
Е) AlCl3.
$$$ 376
Определите pH раствора, если концентрация H+ ионов равна 10-3 моль/л?3
$$$ 377
Используя закон действия масс, определите уравнение скорости реакции
3E + C® 2D:
А) v = k [D]2;
В) v = k [E]3 [C];
С) v = k [E]3;
D) v = k [C];
Е) v = k [E] [C].
$$$ 378
Какая из ниже перечисленных реакции относится к окислительно-восстановительным:
А) CuSO4 + Zn ® ZnSO4 + Cu;
В) SO2 + H2O ® H2SO3;
С) AgNO3 + KCl ® AgCl + KNO3;
D) CrCl3 + 3H2O ® Cr(OH)3 + 3HCl;
Е) H2SiO3 ® H2O + SiO2.
$$$ 379
Определите pH раствора, если концентрация OH- ионов равна 10-11 моль/л-1 : 3
$$$ 380
Определите pH, если концентрация H+ ионов равна 10-5: 5
$$$ 381
Из ниже перечисленных реакций к окислительно-восстановительным относится:
А) AlCl3 + H2O ® Al(OH)3 + 3HCl;
В) CaCl2 + H2SO4 ®CaSO4 + 2HCl;
С) 5Na2SO3+ 2KMnO4 + 3H2SO4 ®5Na2SO4 + K2SO4 + 2MnSO4 +3H2O;
D) (NH4)2CO3 ® 2NH3 + H2O + CO2;
Е) H2SiO3 ® H2O + SiO2
$$$ 382
Используя закон действия масс определите скорость реакции A +2B ® 3C:
А) v = k [C]3;
В) v = k [A] [B]2;
С) v = k [A];
D) v = [A] [B];
Е) v = k [B].
$$$ 383
Из ниже перечисленных солей гидролизу не подвергается:
А) K2SO4;
В) CrCl3;
С) Na3PO4;
D) Al2S3;
Е) Fe2(SO3)3.
$$$ 384
Какая соль подвергается гидролизу?
А) NaCI;
B) K2SO4;
C) (NH4 )2S;
D) NaNO3;
Е) KCI.
$$$ 385
Определите рН раствора, если концентрация Н+ ионов равна 10-4 моль/л? 4
$$$ 386
Используя закон действия масс определите скорость реакции A +3D ® 2C:
А) v = k[C];
В) v = k[A];
С) v = k [D];
D) v = k [A] [D]3;
Е) v = k [C]2 .
$$$ 387
Для какого электролита можно выразить константу диссоциации?
А) NH4 OH;
В) HCl;
С) КОН;
D) H2SO4;
Е) NaCI.
$$$ 388
Какой электролит подвергается ступенчатой диссоциации:
A)H2SО4;
B) HCI;
C) KCI;
D) NaOH;
E) CH3COOH.
$$$ 389
Чему равно ионное произведение для Mg(OH)2?
A) [Mg2+][OH-];
B) [Mg2+][OH-]2;
C) [Mg2+]2[OH-];
D) [Mg2+]+[OH-];
E) [Mg2+]+[OH-]2;
$$$ 390
В приведенной реакции 5Na2SO3 + 2KMnO4 + 3H2SO4 ® 5Na2SO4 + K2SO4+ + 3H2O + 2MnSO4 определите окислитель:
A) KMnO4;
B) H2SO4;
C) Na2SO3;
D) K2SO4;
E) Na2SO4.
$$$ 391
Чему равно ионное произведение воды?
А)  ;
;
В)  ;
;
С) 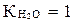 ;
;
D)  ;
;
Е) 
$$$ 392
Выразите константу равновесия для реакции: 2Н2 + СО  СН3ОН
СН3ОН
А)  ;
;
В)  ;
;
С)  ;
;
D) 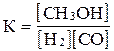
Е) 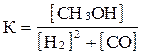 .
.
$$$ 393
Для какой реакции используют электронный баланс?
А) гидролиза;
В) обменный;
С) нейтрализация;
D) дегидратация;