Тестирование во внеучебное время с использованием технологии внешних средств оценки знаний (проект НИИ мониторинга качества образования г. Йошкар-Ола «Интернет – тренажеры в сфере образования»). Для прохождения тестирования необходимо получить у преподавателя логин и пароль.
Темы:
1. термодинамика;
2. кинетика;
3. химическое равновесие;
Ориентировочная основа действия (ООД) для СРС
1. Привести примеры наиболее важныхмакроэргов.
2. Дать определение сопряженных реакций. Показать принцип энергетического сопряжения на конкретном примере.
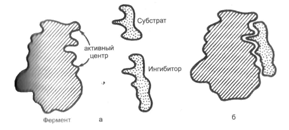
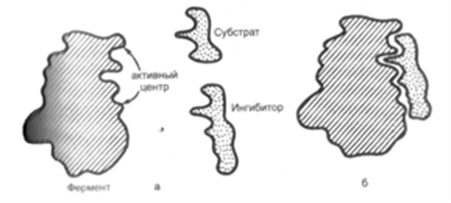
3.Объяснить процессы, происходящие на рисунке. Указать вид ингибирования фермента.
| 
|
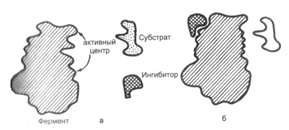
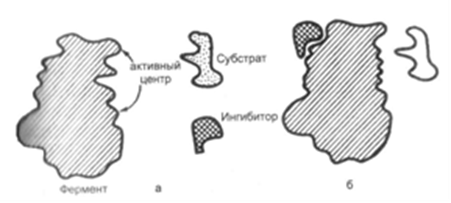
4. Объяснить процессы, происходящие на рисунке. Указать вид ингибирования фермента.
| 
| 
|
Источники информации
8.1.Обязательная литература
1. Попков В.А., Пузаков С.А. Общая химия. - М.: ГЭОТАР-МЕДИА, 2007, с.150-189, с.200-229.
2.Жолнин А.В. Общая химия. Под.ред. Попкова В.А., Жолнина А.В., учебник - М.:ГЭОТАР-Медиа, 2014. с. 19-36., с. 37-58.
3. Пузаков С.А., Попков В.А., Филиппова А.А. Сборник задач и упражнений по общей химии. Учеб.пособие для вузов, 5-е изд.-М.:Юрайт, 2014. с. 22-35, с.44-66.
|
|
8.2.Дополнительная литература
1. Бабков А.В., Барабанова Т.И., Попков В.А. Общая и неорганическая химия, учебник - М.: ГЭОТАР-Медиа, 2014. 384 с.
2. Тюрина Е.Ф., Иванова Н.С. и др. Общая химия. Вопросы и ответы. Владивосток, Медицина ДВ, 2008. 170 с.
3. ЭБС «Консультант студента» https://Studmedlib.ru
4. ЭБС «Университетская библиотека online» https://www. biblioclub.ru
Эталоны ответов к заданиям для самоконтроля
Приведены в:
1. ссылке 3 обязательной литературы,
2. ссылке 2 дополнительной литературы.
Результаты самостоятельной работы контролируются преподавателем при выполнении письменной работы – отчёта по модулю №2 «Элементы химической термодинамики. Элементы химической кинетики».
Приложение
Термодинамические свойства некоторых элементов, неорганических и органических соединений в стандартных условиях
| соединение | состояние | ΔΗ0обр, кДж/моль | ΔG0, кДж/моль | S0, Дж/моль·К | ΔΗ0сгор, кДж/моль |
| Н2О2 | жидкое | -188,0 | -121,0 | 110,0 | |
| С2Н5ОН | жидкое | -278,0 | -175,0 | 161,0 | -1368 |
| СН3СОН | газообраз. | -166,0 | -129,0 | 250,0 | -1192 |
| Н2О | жидкое | -286,0 | -237,0 | 70,0 | |
| Н2О | газообраз. | -242,0 | -229,0 | 189,0 | |
| СО | газообраз. | -111,0 | -137,0 | 198,0 | |
| СО2 | газообраз. | -393,5 | -394,4 | 214,0 | |
| С6H5NO2 | жидкое | 16,0 | 146,0 | 224,0 | -3093 |
| С6H5NН2 | жидкое | 31,0 | 149,0 | 191,0 | -3396 |
| Н2 | газообраз. | -286,0 | |||
| СН4 | газообраз. | -74,8 | -50,7 | 186,0 | -890 |
| СН3Cl | газообраз. | -82,0 | -59,0 | 234,0 | |
| СН2Cl2 | газообраз. | -88,0 | -59,0 | 271,0 | |
| СНCl3 | газообраз. | -100,0 | -67,0 | 296,0 | |
| СCl4 | газообраз. | -107,0 | -64,0 | 309,0 | |
| НCl | газообраз. | -92,3 | -95,3 | 186,7 |