НОВОТРОИЦКИЙ ФИЛИАЛ
Кафедра металлургических технологий и оборудования
Контрольная работа
по дисциплине «Теплотехника»
Вариант № 0
Выполнил: студент гр. ТМиОз-14-34
Проверил: Куницина Н.Г.
Новотроицк, 2017
Для случая сжигания смешанного газа с теплотой сгорания 12 МДж/м3 определить расход воздуха, состав и количество продуктов сгорания, калориметрическую температуру горения при коэффициенте расхода (избытка) воздуха n=1,09. Температура подогрева воздуха 340 ˚С. Температура подогрева топлива 250 ˚С. Составить материальный баланс процесса горения.
Состав топлива А, %: СО2=5,5, О2=0,4, СО=27,5, Н2=13,5, СН4=0,5, N2=52,6. Влажность топлива А WА=24 г/м3.
Состав топлива Б, %: СО2=2,9, О2=0,5, СО=7, Н2=58, СН4=26,7, С3Н8=2,4, N2=2,5. Влажность топлива Б WБ=30 г/м3.
Выполним пересчет каждого топлива с сухой массы на влажную, используя формулы:
 ;
;
 ,
,
где  – содержание компонента топлива соответственно во влажной и сухой массе, %;
– содержание компонента топлива соответственно во влажной и сухой массе, %;
W – влажность топлива, г/м3;
H2О – количество воды во влажной массе топлива, %.
Для топлива А:
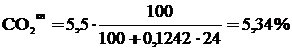 ;
;
 ;
;
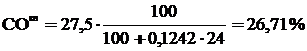 ;
;
 ;
;
 ;
;
 ;
;
 .
.
Проверяем правильность расчета, складывая все компоненты топлива А:
 =5,34 +0,39 +26,71 +13,11 +0,49+51,08+2,88= 100 %.
=5,34 +0,39 +26,71 +13,11 +0,49+51,08+2,88= 100 %.
Для топлива Б:
 ;
;
 ;
;
 ;
;
 ;
;
 ;
;
 ;
;
 ;
;
 .
.
Проверяем правильность расчета, складывая все компоненты топлива Б:
 =2,80 +0,48 +6,75 +55,92 +25,74+2,31+2,41+3,59= 100 %.
=2,80 +0,48 +6,75 +55,92 +25,74+2,31+2,41+3,59= 100 %.
Определяем теплоту сгорания каждого топлива по формуле:
Qрн = 127.СО+108.Н2+358.СН4+590.С2Н4+555.С2Н2+635.С2Н6+913.С3Н8+
+1185.С4Н10+1465.С5Н12+234.Н2S,
где Qрн – низшая теплота сгорания топлива, кДж/м3.
Теплота сгорания топлива А:
Qрн(А) = 127·26,71+108·13,11+358·0,49 = 4983,47 кДж/м3.
Теплота сгорания топлива Б:
Qрн(Б) = 127.6,75+ 108·55,92+358.25,74+913.2,31 =18220,56 кДж/м3.
Определяем состав смеси двух топлив.
Для этого необходимо определить долю топлива А в смеси топлив из выражения:
 ,
,
где а – доля топлива А в смеси двух топлив;
Qрн(А), Qрн(Б) – теплота сгорания соответственно топлива Б и топлива А, кДж/м3;
Qрн(см) – теплота сгорания смеси топлив, кДж/м3,
 .
.
Состав смеси определяется по формуле:
Хвл(см) = Хвл(А).а + Хвл(Б).(1-а),
где Хвл(см), Хвл(А), Хвл(Б) – содержание компонента в смеси топлив и в топливах А и Б соответственно, %.
Тогда с учетом формулы состав смеси топлив будет следующий:
СО2см =5,34.0,47+2,8.0,53 = 3,99 %;
СОсм =26,71· 0,47+6,75.0,53 = 16,13 %;
Н2см = 13,11.0,47+55,92.0,53 = 35,80 %;
О2см = 0,39.0,47+0,48.0,53 = 0,44 %;
СН4см =0,49.0,47+25,74.0,53 = 13,87 %;
С3Н8см=0+2,31.0,53 = 1,22 %;
N2cм =51,08· 0,47+2,41.0,53 = 25,28 %;
Н2Осм =2,88· 0,47+3,59· 0,35 = 3,27 %.
Проверяем правильность расчета, складывая все компоненты смеси топлив:
 =3,99 +16,13 +35,80 +0,44 +13,87+1,22+25,28+3,27=100 %.
=3,99 +16,13 +35,80 +0,44 +13,87+1,22+25,28+3,27=100 %.
Определяем расход воздуха, состав и количество продуктов сгорания. Расчет ведём на 100 м3 смеси топлив.
Составляем реакции горения горючих компонентов смеси топлив и на их основе определяем количество требуемого для горения кислорода, а также количество образующихся продуктов сгорания.
а) СО + 1/2 02 = С02
1 м3СО - 0,5 м3 02
16,13 м3 СО - 8,07 м3 02 ;
1 м3СО - 1 м3 С02
16,13 м3 СО- 16,13 м3 С02.
б) Н2 + 1/202 = Н20
1 м3Н2 - 0,5 м3 02
35,8 м3 Н2 - 17,9 м3 02 ;
1 м3 Н2 - 1 м3 Н20
35,8 м3 Н2 – 35,8 м3Н20.
в) СН4 + 202 = С02 + 2Н20
1 м3 СН4 -2м3 02
13,87 м3 СН4 - 27,74 м3 02 ;
1 м3 СН4 - 1 м3 С02 и 2 м3 Н20
13,87 м3 СН4 – 13,87 м3 С02 и 27,74 м3Н20.
г) С3Н8 + 502 = 3С02 + 4Н20
1 м3 С2Н4 - 5 м3 02
1,22 м3 С2Н4 - 6,1 м3 02 ;
1 м3 С2Н4 - 3 м3 С02 и 4 м3 Н20
1,22 м3 С2Н4 - 3,66 м3 С02 и 4,88 м3 Н20.
Полученные данные заносим в таблицу 1.
Для определения количества воздуха с учетом коэффициента избытка воздуха, необходимо воспользоваться выражением:
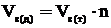 ,
,
где  – действительный объем воздуха, м3;
– действительный объем воздуха, м3;
 – теоретический объем воздуха, м3;
– теоретический объем воздуха, м3;
n – коэффициент избытка воздуха.
Таблица 1 – Результаты расчета расхода воздуха, состава и количества продуктов сгорания
| Участвуют в горении | Образуется продуктов сгорания, м3 | ||||||||
| Топливо, м3 | Воздух, м3 | ||||||||
| Составля-ющая | Содержание, м3 | О2 | N2 | всего | СО2 | Н2О | О2 | N2 | всего |
| СО2 СО Н2 О2 СН4 С3Н8 N2 Н2О | 3,99 16,13 35,80 0,44 13,87 1,22 25,28 3,27 | - 8,07 17,90 -0,44 27,74 6,10 - - | 59,37.3,762=223,35 | 59,37+223,35=282,72 | 3,99 16,13 - - 13,87 3,66 - - | - - 35,80 - 27,74 4,88 - 3,27 | 25,28+223,35=248,63 | ||
| n = 1 | 59,37 (21 %) | 223,35 (79 %) | 282,72 (100 %) | 37,65 (10,5 %) | 71,69 (20,0 %) | - | 248,63 (69,5 %) | 357,97 (100 %) | |
| n = 1,09 | 64,71 (21 %) | 243,45 (79 %) | 308,16 (100 %) | 37,65 (9,8 %) | 71,69 (18,7 %) | 5,34 (1,4 %) | 268,73 (70,1 %) | 383,41 (100 %) |
Для определения состава продуктов сгорания, воспользуемся формулой:
 ,
,
где  – содержание i-того компонента в продуктах сгорания, %
– содержание i-того компонента в продуктах сгорания, %
 – объем i-того компонента в продуктах сгорания, м3;
– объем i-того компонента в продуктах сгорания, м3;
 – общий объем продуктов сгорания, м3.
– общий объем продуктов сгорания, м3.
Таким образом, состав продуктов сгорания с учетом данных таблицы 1:
 ;
;
 ;
;
 ;
;
 .
.
Для проверки правильности расчета составляется материальный баланс. Материальный баланс представлен в таблице 2.
Таблица 2 – Материальный баланс горения смеси двух топлив
| Поступило, кг | Получено, кг |
| Топливо: СО2 = 3,99·44/22,4 = 7,84 СО = 16,13·28/22,4 = 20,16 О2 = 0,44.32/22,4 = 0,63 Н2О = 3,27.18/22,4 = 2,63 Н2 = 35,80·2/22,4 = 3,20 СН4 = 13,87·16/22,4 = 9,91 N2 = 25,28·28/22,4 = 31,60 C3Н8 = 1,22·44/22,4 = 2,40 Воздух: О2 = 64,71.32/22,4 = 92,44 N2 = 243,45.28/22,4 = 304,31 Итого: 475,12 кг. | Продукты сгорания: СО2 = 37,65·44/22,4 = 73,96 Н2О = 71,69.18/22,4 = 57,61 N2 = 268,73·28/22,4 = 335,91 О2 = 5,34.32/22,4 = 7,29 Итого: 474,77 кг. |
Рассчитываем погрешность вычислений  .
.
Т.к. погрешность менее 0,5 %, следовательно, расчет проведен правильно.
Из таблицы 1 следует, что для сжигания 100 м3 смеси топлив необходимо затратить 308,16 м3 воздуха при указанной величине коэффициента избытка воздуха, равной 1,09. При этом образуется продуктов сгорания 383,41 м3. Т.е. для сжигания 1 м3 смеси топлив необходимо затратить 3,082 м3 воздуха и образуется продуктов сгорания 3,834 м3.
Определяем калориметрическую температуру горения. Для этого необходимо найти начальную энтальпию (теплосодержание) 1м3 продуктов сгорания:
I = Io + Iв + Iг,
где I – энтальпия продуктов сгорания, кДж/м3;
Io, Iв, Iг – соответственно количества тепла, получаемые от сжигания топлива и вносимые подогретым воздухом и топливом, кДж/м3.
Так как топливо не подогревается предварительно, то Iг=0.
Количество тепла, получаемое от сжигания топлива в расчете на единицу объема продуктов сгорания, определим из выражения:
 ,
,
 кДж/м3.
кДж/м3.
Количество тепла, вносимое подогретым воздухом, может быть определено следующим образом:
 ,
,
где tв – температура подогрева воздуха, 0С;
св – теплоемкость воздуха при 340 оС, кДж/(м3.оС);
Vв – объем воздуха, вносимого в печь, м3.
Теплоемкость воздуха определяем методом интерполяции:
 кДж/(м3.оС).
кДж/(м3.оС).
Тогда количество тепла, вносимое подогретым воздухом:
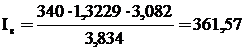 кДж/м3.
кДж/м3.
Количество тепла, вносимое подогретым топливом, определяем по формуле:
 ,
,
где tт – температура подогрева топлива, оС;
ст – теплоемкость топлива при 250 оС, кДж/(м3.оС);
Vт – объем топлива, вносимого в печь, м3.
Теплоемкость топлива, состоящего из многих компонентов, определяется из выражения:
 ,
,
где сi – теплоемкость i-того компонента топлива при указанной температуре, кДж/(м3.оС);
 – доля i-того компонента топлива в смеси.
– доля i-того компонента топлива в смеси.
Определяем теплоемкость всех компонентов топлива при температуре 250 оС методом интерполяции:
 кДж/(м3.оС);
кДж/(м3.оС);
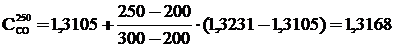 кДж/(м3.оС);
кДж/(м3.оС);
 кДж/(м3.оС);
кДж/(м3.оС);
 кДж/(м3.оС);
кДж/(м3.оС);
 кДж/(м3.оС);
кДж/(м3.оС);
 кДж/(м3.оС);
кДж/(м3.оС);
 кДж/(м3.оС);
кДж/(м3.оС);
 кДж/(м3.оС).
кДж/(м3.оС).
Теплоемкость топлива:
Ст = 1,8444.0,0399+1,3168.0,1613+1,3476.0,0044+1,3000.0,3580+1,8297.0,1387+
+2,4285.0,0122+1,3055.0,2528+1,5277.0,0327=1,4207 кДж/(м3.оС).
Количество тепла, вносимое подогретым топливом:
 кДж/м3.
кДж/м3.
Таким образом, энтальпия продуктов сгорания составит:
 кДж/м3.
кДж/м3.
Далее искомую температуру находим методом подбора. Для этого задаемся возможной температурой горения, например, равной 2100 ˚С, и определяем при этой температуре энтальпию продуктов сгорания с учетом табличных данных и состава продуктов сгорания:
СО2....................... 0,098 ∙ 5186,81 = 508,3
Н2О....................... 0,187∙ 4121,79 = 770,8
О2.........................0,014 ∙ 3314,85 = 46,4
N2.........................0,701 ∙ 3131,96 = 2195,5
––––––––––––––––––––––––––––––––––––––––––––––––
Итого...................................... 3521,0 кДж/м3.
Сравниваем полученную энтальпию с действительной энтальпией продуктов сгорания. Поскольку I>I2100 , следовательно, искомая температура горения больше, чем 2100 оС.
Задаемся температурой горения, равной 2200 0С. Энтальпия продуктов сгорания при этой температуре:
СО2....................... 0,098 ∙ 5464,20 = 535,5
Н2О....................... 0,187∙ 4358,83 = 815,1
О2.........................0,014 ∙ 3487,44 = 48,8
N2.........................0,701 ∙ 3295,84 = 2310,4
––––––––––––––––––––––––––––––––––––––––––––––––
Итого...................................... 3709,8 кДж/м3.
Т.к. I2200>I, то действительная калориметрическая температура горения лежит в пределах 2100 – 2200 оС.
Окончательно калориметрическую температуру горения определяем интерполяцией по формуле:
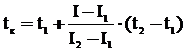 ,
,
где  – калориметрическая температура горения, оС,
– калориметрическая температура горения, оС,
 оС.
оС.
Список использованных источников
1 Куницина Н.Г. Расчет горения топлива. Методические указания для выполнения домашних заданий и контрольных работ по дисциплинам «Теплотехника», «Металлургическая теплотехника», Новотроицк: НФ НИТУ «МИСиС», 2015. – 31 с.