Сплавы с неограниченной растворимостью компонентов в твердом состоянии.Компоненты этих сплавов имеют одинаковые по типу и близкие по параметрам кристаллические решетки (например, Fe—Ni, Fe—Co, Fe—V, Cu—Ni, Au—Ag и др.). В общей кристаллической решетке основного компонента (растворителя) атомы второго компонента могут располагаться по типу внедрения или замещения. При этом следует иметь в виду, что замещение или внедрение атома с иными размерами, чем атомы растворителя, приводит к искажению кристаллической решетки.
Твердые растворы обозначают следующим образом: слева пишется компонент-растворитель, справа, в скобках, — растворенный компонент: А (В). Например: Fe(Ni) — атомы никеля растворены в решетке железа.
В процессе кристаллизации таких сплавов из жидкого раствора выделяются кристаллы твердого раствора. После полного затвердевания структура сплава будет однофазной. Следовательно, на кривых охлаждения нет так называемых остановок (горизонтальных площадок), а на диаграмме состояния нет линий, параллельных оси «Концентрация» (рис. 1.8, а). На диаграмме состояния можно выделить три зоны:
- зона 1 — выше линии ликвидуса MEN сплав находится в жидком состоянии;
- зона 2 — между линиями ликвидуса MEN и солидуса MCN начинается кристаллизация сплава. По правилу фаз, число степеней свободы равно 1: С = 2 + 1 - 2 (компонентов — 2, фаз — 2). Следовательно, кристаллизация происходит в интервале температур и при изменении состава фаз. Из жидкой фазы выделяются кристаллы твердого раствора. С понижением температуры кристаллы твердого раствора продолжают выделяться, состав их меняется по линии солидуса. Одновременно с изменением состава кристаллов происходит изменение состава жидкости. При понижении температуры состав жидкости меняется по линии ликвидуса. Происходит перераспределение атомов компонентов А и В между жидкой и твердой фазами;
- зона 3 — ниже линии солидуса MCN сплав находится в твердом состоянии. Кристаллы сплава однородны и имеют одинаковый состав. Выравнивание состава сплава происходит за счет диффузии (проникновения в кристаллы атомов компонента А из жидкого сплава в уже имеющиеся кристаллы твердого раствора). Частично выравнивание состава кристаллов происходит за счет внутрикристаллической диффузии (за счет диффузии более тугоплавкого компонента из внутренних областей кристаллов к внешним областям).
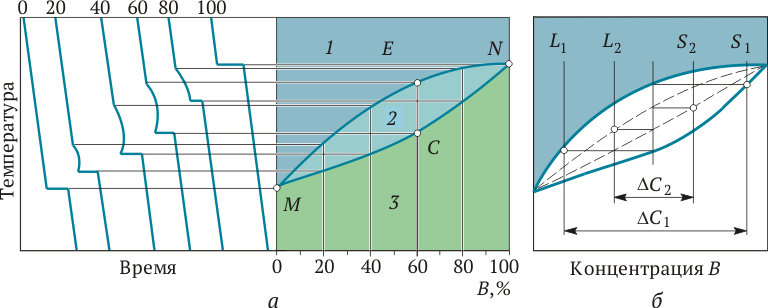 Рис. 1.8.Построение диаграммы состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии:
Рис. 1.8.Построение диаграммы состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии:
а — диаграмма состояния: 0, 20, 40, 60, 80 и 100 — кривые охлаждения сплава при концентрации компонента В соответственно 0, 20, 40, 60, 80 и 100%; MEN — линия ликвидуса; MCN — линия солидуса; 1 — зона жидкого состояния сплава; 2 — зона кристаллизации сплава; 3 — зона твердого состояния сплава; б — диаграммы состояния при разных скоростях охлаждения сплава: L 1, L 2, S 1 и S 2 — точки соответственно ликвидуса и солидуса для большей (1) и меньшей (2) скоростей охлаждения сплава; D С 1 и D С 2 — степень дендритной ликвации для большей (1) и меньшей (2) скоростей охлаждения сплава
При кристаллизации твердых растворов отчетливо виден рост дендритов. Ветви первого порядка образуются при более высокой температуре, поэтому концентрация тугоплавкого компонента в них выше. Ветви второго и высших порядков образуются при меньших температурах, поэтому с увеличением номера порядка в них уменьшается концентрация тугоплавкого компонента. При медленном охлаждении состав дендрита выравнивается за счет диффузии. При высокой скорости охлаждения выравнивания не происходит, состав ветвей дендрита будет различным (дендритная, или внутрикристаллическая, ликвация).
С помощью диаграммы состояния можно оценить склонность сплава к дендритной ликвации (рис. 1.8, б). Рассмотрим быстрое охлаждение сплава. Первые ветви дендрита имеют состав, соответствующий точке S, а последние ветви — точке L. Максимальное различие по составу (степень дендритной ликвации) равно D C 1. При низкой скорости охлаждения диаграмма состояния сужается. Расстояние между точками L 2 и S 2 равно D C 2, D C 2< D C 1, следовательно, степень дендритной ликвации будет меньше.
Дендритная ликвация исправима, если сплав в твердом состоянии медленно нагреть до температуры, при которой интенсивно протекает диффузия (несколько ниже линии солидуса).
Сплавы, образующие ограниченные твердые растворы и эвтектику. Такие сплавы достаточно часто встречаются в практике. Они характерны тем, что один из компонентов неограниченно растворяется в другом жидком компоненте, а в твердом — или совсем не растворяется, или растворяется ограниченно.
Если подобрать количество растворяемого компонента больше предела растворимости при заданной температуре, то часть компонента, превышающая предел растворимости, не войдет в твердый раствор, а образует механическую смесь с кристаллами насыщенного твердого компонента. В сплаве будут находиться две фазы. Чаще всего с повышением температуры растворимость компонента увеличивается. При нагреве такого двухфазного сплава до температуры плавления появится третья фаза — жидкий сплав. Следовательно, на диаграмме состояния (рис. 1.9) должна быть линия, параллельная оси «Концентрация», характеризующая появление жидкой фазы в сплавах, имеющей концентрацию выше предельной.
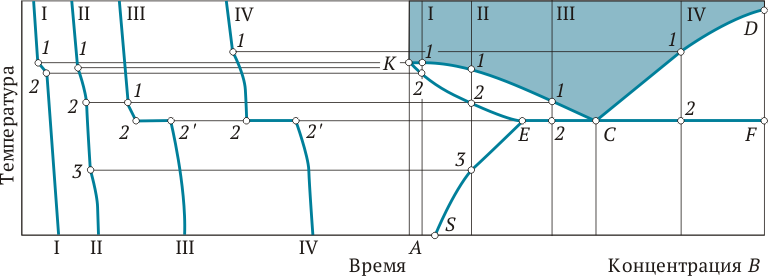 Рис. 1.9.Построение диаграммы состояния сплавов, образующих ограниченные твердые растворы и эвтектику:
Рис. 1.9.Построение диаграммы состояния сплавов, образующих ограниченные твердые растворы и эвтектику:
I, II, III и IV — сплавы с различной концентрацией компонента В в компоненте А; 1 — точка ликвидуса; 2 — точка солидуса; 3 — точка вторичной кристаллизации; KCD — линия ликвидуса; KECF — линия солидуса; SE — линия изменения растворимости компонента В в компоненте А
На этой диаграмме линия KCD — линия ликвидуса, линия KECF — солидуса, линия ECF — линия эвтектики. Точка Е характеризует предельную растворимость компонента В в компоненте А при эвтектической температуре. Точка S характеризует предельную растворимость В в А при комнатной температуре. Линия SЕ показывает изменение растворимости В в А в твердом состоянии при изменении температуры (растворимость с повышением температуры увеличивается).
Следовательно, в сплавах левее линии SЕ будут ненасыщенные кристаллы А (В), на линии SЕ — насыщенные кристаллы А (В), правее линии SЕ будет механическая смесь насыщенных кристаллов А (В) и компонента В. Диаграмма состоит как бы из двух частей: левее точки Е — диаграмма состояния твердого неограниченного раствора, правее точки Е — диаграмма состояния сплава, состоящего из механической смеси.
Рассмотрим кристаллизацию сплавов при разной концентрации компонента В.
Cостав сплава записывают следующим образом: буквенный или цифровой индекс у обозначения фазы или структурной составляющей показывает состав (точку на диаграмме состояния), который имеет данная фаза или структурная составляющая.
Например: запись А ( В ) Е обозначает кристаллы твердого раствора компонента В в А, соответствующего точке Е; запись «Эвт. С [ А (В) Е + В ]» означает: эвтектика состава точки С, состоящая из кристаллов твердого раствора В в А состава точки Е и кристаллов В.
Сплав I кристаллизуется так же, как и неограниченный твердый раствор. В точке ликвидуса (точка 1) образуются кристаллы твердого раствора А (В). От точки 1 к точке 2 (солидус) образуются новые кристаллы твердого раствора А (В). В точке 2 сплав полностью затвердевает, и новых структурных изменений не происходит.
Сплав II кристаллизуется несколько иначе. В точке 1 начинается кристаллизация, из жидкого сплава выделяются кристаллы А (В). Процесс заканчивается в точке 2. В интервале температур от точки 2 до точки 3 начинается вторичная кристаллизация (образование новых зерен в твердом состоянии). Так как растворимость В в А меняется по линии SE, то ниже точки 3 в сплаве находится больше компонента В, чем это возможно, поэтому избыточная часть компонента B будет выделяться в твердом растворе (эта часть компонента обычно обозначается В 11).
Выделение вторичных кристаллов происходит до полного охлаждения сплава (до концентрации, соответствующей точке S). Вторичные кристаллы значительно мельче первичных, так как их выделение идет в «стесненных условиях». Чем ближе сплав к точке Е, тем больше выделяется вторичных кристаллов. Точка Е соответствует максимальному выделению вторичных кристаллов. При медленной термической обработке сплавов выделение мелких вторичных кристаллов приводит к упрочнению сплава. При больших скоростях охлаждения вторичные кристаллы могут не успеть выделиться, и сплав будет однофазным (пересыщенный твердый раствор).
Сплав III — доэвтектический. Кристаллизация начинается при температуре, соответствующей точке 1. В результате выделяются кристаллы А (В). Состав этих кристаллов будет меняться по линии KЕ. При эвтектической температуре (соответствующей точке 2) выделившиеся кристаллы А (В) имеют состав, отвечающий точке Е. При этом жидкая часть сплава, изменяясь по линии KС, будет эвтектической (точка С). Кристаллизуясь, жидкий эвтектический сплав образует эвтектику Эвт. Е [ А (В) Е + В ]. Кристаллизация эвтектики происходит при постоянной температуре (2 — 2 ′). После полного охлаждения структура сплава будет состоять из А (В) S + В 11+ Эвт. С [ А (В) S + В ]. Однако мелкие кристаллы В 11 объединятся с кристаллами В в однородные зерна, поэтому эвтектику можно записать так: Эвт. С [ А (В) S ++ В ]. Для того чтобы различать кристаллы первичной и вторичной кристаллизаций, первичным кристаллам присваивается индекс «1». Окончательную структуру сплава III можно записать в виде А (В)1 S + В 11+Эвт. С [ А (В) S + В ].
Сплав IV — заэвтектический. При температуре, соответствующей точке 1, начинается выделение первичных кристаллов В 1. Эти кристаллы растут в жидкой среде с большими скоростями роста и малым сопротивлением внешней среды, поэтому они вырастают крупными. По достижении точки 2 концентрация жидкого сплава соответствует эвтектической. Сплав затвердевает. От точки 2 до полного охлаждения сплава из кристаллов эвтектики Эвт. Е [ А (В) Е + В ] будут выделяться вторичные кристаллы, которые присоединятся к кристаллам В внутри эвтектики. После полного охлаждения сплав будет иметь состав В 1+Эвт. С [ А (В) S + В ].
Фазовые превращения в железоуглеродистых сплавах
Сплавы на основе железа — черные сплавы (сталь и чугун) — широко применяются в машиностроении. В современных сельскохозяйственных машинах до 80% по массе или до 60% по номенклатуре — сталь и чугун.
Железо — серебристо-белый металл, находится в 8-й группе Периодической таблицы Д. И. Менделеева, его атомный номер — 26, атомная масса — 55,8, атомный радиус — 1,27×10-10 м (0,127 нм), температура плавления — 1539°С. При температуре выше 768°С (точка Кюри) железо теряет свои магнитные свойства. Чистое железо (которое можно получить современными металлургическими способами) содержит 0,0001% примесей. Техническое железо содержит 0,1…0,2% примесей. Железо имеет два типа кристаллических решеток: ОЦК и ГЦК. В интервале температур 1539…1392°С железо имеет полиморфную модификацию Fea c решеткой ОЦК; в интервале температур 1392…911°С — модификацию Fe g c решеткой ГЦК; ниже температуры 911°С — модификацию Feb c решеткой ОЦК.
На кривой охлаждения железа, показанной на рис. 1.10, приняты следующие обозначения: критические точки превращения Fea «Fe g и Fe g «Feb соответственно А 4 и А 3; точка Кюри (изменение магнитных свойств железа) — А 2. Остановка при температуре 1539°С связана с началом кристаллизации Fea. Остановки при температурах 1392 и 911°С связаны с полиморфными превращениями железа. Остановка при температуре 768°С связана с изменением магнитных свойств железа.
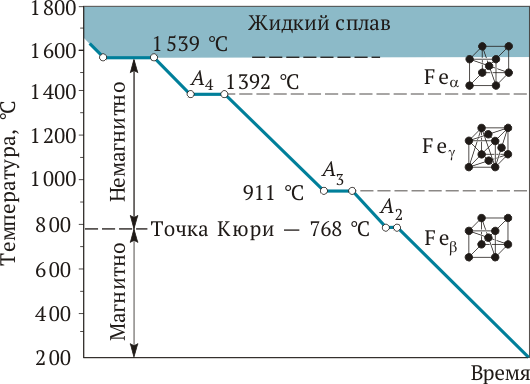 Рис. 1.10.Кривая охлаждения железа:
Рис. 1.10.Кривая охлаждения железа:
А 2 — точка Кюри; А 3 — точка превращения Feb«Fe g; А 4 — точка превращения Fe g «Fеa
При взаимодействии железа с углеродом он может растворяться в решетках железа по механизму внедрения и образовывать соединения Fe3C и Fe2C. Соединение Fe3C содержит наименьшую концентрацию углерода (6,67%), поэтому часть диаграммы «железо—углерод» до концентрации 6,67% можно рассматривать как самостоятельную диаграмму Fe—Fe3C (рис. 1.11).
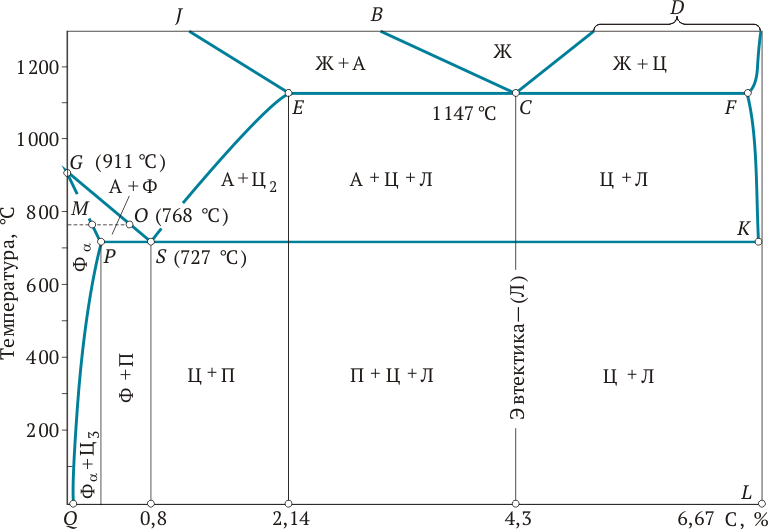 Рис. 1.11.Диаграмма состояния сплава железо—углерод:
Рис. 1.11.Диаграмма состояния сплава железо—углерод:
А — аустенит; Ж — жидкость; Л — ледебурит; П — перлит; Фa — ферритa; Ц — цементит первичный; Ц2 — цементит вторичный; Ц3 — цементит третичный; D — точка плавления аустенита; G — точка полиморфных превращений Fe g «Fеa; BC и JE — соответственно линии ликвидуса и солидуса жидкого сплава с образованием кристаллов аустенита; CD — линия начала кристаллизации жидкого сплава с образованием кристаллов цементита; ECF — эвтектическая горизонталь; PSK — эвтектоидная горизонталь; SE — линия предельной растворимости углерода в Fe g; PQ — линия предельной растворимости углерода в Fea; MO — линия Кюри
В системе Fe—Fe3C различают следующие фазы: жидкий сплав (Ж); твердая фаза — феррит (Ф) — твердый раствор углерода и других примесей в Fea, различают низкотемпературный ферритa с растворимостью углерода до 0,02% и высокотемпературный ферритd с предельной растворимостью углерода 0,1%; аустенит (А) — твердый раствор углерода и других примесей в Fe g, предельная растворимость углерода в Fe g — 2,14%; цементит (Ц) — карбид железа Fe3C со сложной ромбической, плотноупакованной кристаллической решеткой, до температуры 210°С (обозначается А 0) цементит ферримагнитен; графит (Г) — имеет слоистую гексагональную решетку.
Анализ диаграммы состояния показывает, что некоторые ее части схожи с диаграммами, рассмотренными ранее.
Правая верхняя часть диаграммы (линия BCDFEB) соответствует диаграмме эвтектического типа. Линии ВС (ликвидус) и JE (солидус) показывают температуры начала и конца кристаллизации с образованием аустенита. Линия СD отвечает температурам начала кристаллизации цементита. Линия ECF — температура, при которой происходят эвтектические превращения в сплавах.
Линии GS, GP соответствуют температурам начала и конца полиморфного превращения аустенит «феррит. Линия SE — предельная растворимость углерода в Fe g (предельная концентрация углерода в аустените). Линия PQ — предельная растворимость углерода в Fea. Линия МО показывает температуру превращения феррита из магнитного состояния в немагнитное.
Из диаграммы видно, что при содержании углерода менее 2,14% кристаллизация жидкого сплава происходит с выделением кристаллов аустенита. Эти сплавы — железо—углерод — получили название «сталь». Ниже линии GSE начинается распад аустенита на фазы: феррит, цементит, перлит. Перлит (П) — эвтектоидная смесь: феррит + цементит.
При охлаждении до комнатной температуры получаем сплавы различного структурного состава. Левее линии QP — техническое железо (механическая смесь: ферритa ++ 0,0006% углерода). Правее линии QP — сталь. До концентрации 0,8% углерода — доэвтектоидная сталь (при концентрации менее 0,025% углерода — механическая смесь: ферритa+ цементит, при концентрации более 0,025% — механическая смесь: ферритa+ перлит). При концентрации 0,8% углерода — эвтектоидная сталь (перлит). При концентрации более 0,8% углерода — заэвтектоидная сталь (механическая смесь: цементит + перлит).
Левая часть диаграммы включает в себя сплавы с содержанием углерода более 2,14%. Эти сплавы претерпевают эвтектическую кристаллизацию при температуре 1147°С (по линии ECF). При температуре 1147°С жидкий сплав состава, отвечающего точке С (4,3% углерода), кристаллизуется с образованием эвтектической смеси кристаллов аустенита (концентрация углерода — 2,14%) и цементита, получившей название «ледебурит» (Л).
Сплавы с содержанием углерода более 2,14% получили название «белые чугуны». Белыми эти чугуны названы потому, что они практически не содержат свободного углерода и излом таких чугунов светлый, блестящий.
Данные сплавы в зависимости от содержания углерода делятся на доэвтектические чугуны (до 4,3% углерода), конечная их структура — П + Ц1+ Л; эвтектические чугуны (4,3% углерода), структура — Л; заэвтектические чугуны (более 4,3% углерода), структура — Ц1+ Л.
В ледебурите более половины его количества составляет цементит — твердая и хрупкая фракция. Эвтектика (ледебурит) делает чугун твердым и хрупким. Чем больше углерода в сплаве, тем более хрупким является чугун.