Благодаря присутствию двойной связи алкены гораздо более химически активны, чем алканы. Именно двойная связь является реакционным центром их молекул. Для алкенов наиболее характерны реакции присоединения, окисления и полимеризации.
РЕАКЦИИ ПРИСОЕДИНЕНИЯ
ГИДРИРОВАНИЕ
Присоединение водорода (гидрирование) алкенов протекает в присутствии металлических катализаторов (никель, платина, палладий) и приводит к образованию алканов:
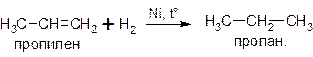
При использовании более активных, чем никель, катализаторов – платины или палладия – реакция гидрирования может протекать и без нагревания.
ГАЛОГЕНИРОВАНИЕ
Присоединение хлора, брома, иода (галогенирование) алкенов протекает в обычных условиях. Продуктами реакций являются дигалогензамещенные алканы:
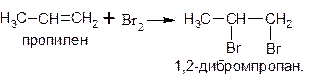
Обычно для проведения бромирования алкенов используют раствор брома в воде – бромную воду. В ходе реакции оранжево-бурая окраска, характерная для бромной воды, исчезает, происходит ее обесцвечивание. Эта реакция является качественной на непредельные углеводороды, в том числе на алкены.
Галогенирование, а также гидрогалогенирование и гидратация алкенов протекают по ионному механизму с образованием в качестве промежуточной частицы карбокатиона (можно дать приложение 1).
ГИДРОГАЛОГЕНИРОВАНИЕ
При взаимодействии алкенов с галогеноводородами (хлороводородом, бромоводородом) образуются галогензамещенные алканы:
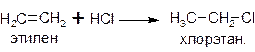
При присоединении галогеноводородов к несимметричным алкенам выполняется правило Марковникова: атом водорода преимущественно присоединяется к более гидрированному атому углерода при двойной связи.
Так, основным продуктом реакции пропилена с бромоводородом является 2-бромпропан (1-бромпропан образуется лишь в незначительных количествах):
|
|
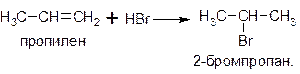
Приведем еще один пример реакции гидрогалогенирования, протекающей по правилу Марковникова:
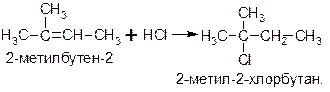
Важно понимать, что правило Марковникова не универсально: оно применимо только в том случае, если молекула алкена не содержит никаких более электроотрицательных, чем углерод, атомов, а реакция присоединения протекает по ионному механизму (можно дать приложение 2 об обращении правила Марковникова).
ГИДРАТАЦИЯ
Присоединение воды к алкенам – г идратация ‑ протекает в присутствии разбавленных серной или фосфорной кислот и приводит к образованию спиртов. Эта реакция также протекает в соответствии с правилом Марковникова:
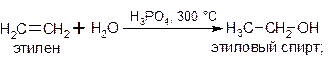
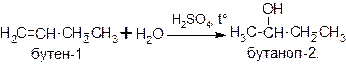
РЕАКЦИИ ОКИСЛЕНИЯ
Алкены, в отличие от алканов, легко подвергаются действию различных окислителей.
При действии на алкены водного или слабощелочного раствора перманганата калия протекает мягкое окисление. При этом двойная связь С=С превращается в простую (разрывается только π-связь) и образуются двухатомные спирты*:
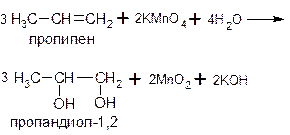
Для проведения этой реакции нагревания не требуется. В ходе ее наблюдается исчезновение характерной фиолетовой окраски перманганата калия и образуются коричневые хлопья диоксида марганца. Говорят, что алкены обесцвечивают водный раствор перманганата калия на холоду. Это еще одна качественная реакция на наличие двойной связи.
При более энергичном окислении – действии перманганата калия в кислой среде при нагревании – протекает ж есткое окисление алкенов. При этом происходит расщепление молекулы по месту двойной связи с образованием смеси карбоновых кислот:
|
|
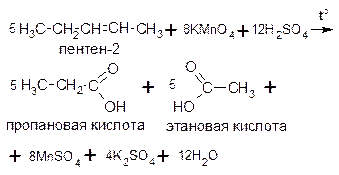
Если двойная связь концевая, то одним из продуктов окисления алкена будет углекислый газ:
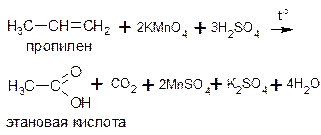
Если же у атома углерода, образующего двойную связь, имеется дополнительный углеводородный заместитель, и нет атома водорода, то в результате его окисления образуется не карбоновая кислота, а кетон:
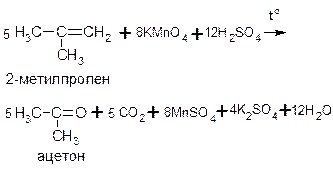
ПОЛИМЕРИЗАЦИЯ
Молекулы алкенов при воздействии различных инициирующих факторов (например, повышении давления, УФ-облучении, действии органических перекисей) или в присутствии катализаторов способны соединяться друг с другом, образуя длинные цепи – молекулы полимеров:
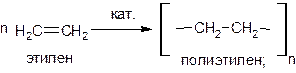
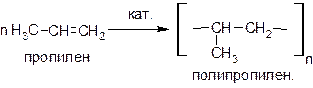
Молекула полимера состоит из многократно повторяющихся простейших фрагментов – элементарных звеньев. При записи формулы полимера элементарное звено заключают в скобки и индексом n указывают степень полимеризации. Полимеризацией алкенов и их производных получают ценные материалы, например, полиэтилен, полипропилен, поливинилхлорид (ПВХ) и др.
СПОСОБЫПОЛУЧЕНИЯ
И ПРИМЕНЕНИЕ АЛКЕНОВ
ПРОМЫШЛЕННЫЕ СПОСОБЫ
В промышленности алкены в больших количествах получают в процессах переработка нефти, в частности, при крекинге алканов (см. конспект «Алканы»).
Другим важным промышленным способом получения алкенов является дегидрирование алканов. В качестве катализаторов этого процесса используют металлы платиновой группы (Pt, Pd, Ni) или Cr2O3, нанесенный на пористый инертный носитель. Температура варьируется от 300 до 600 оС:
|
|
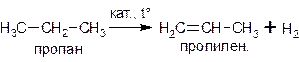
ЛАБОРАТОРНЫЕ СПОСОБЫ
Дегалогенирование протекает при действии активных металлов (цинковой пыли, магниевой стружки) на дигалогензамещенные алканы, атомы галогенов в молекулах которых расположены у соседних атомов углерода:
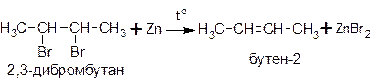
Дегидратация спиртов происходит при нагревании их с концентрированной серной кислотой. В случае этилового спирта температуру поддерживают не ниже 170 ◦С (при более низких температурах в этих же условиях преимущественно образуются простые эфиры):
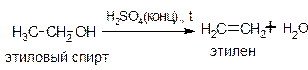
Для проведения этой реакции используют и другие водоотнимающие вещества, например, оксид алюминия:
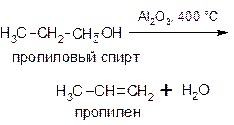
Гидроксильная группа и атом водорода отщепляются от соседних атомов углерода, при этом выполняется правило Зайцева: атом водорода отщепляется преимущественно от наименее гидрированного атома углерода. Так, при дегидратации бутанола-2 основным продуктом реакции является бутен-2:
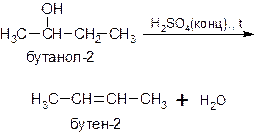
Дегидрогалогенирование с образованием алкенов происходит при нагревании моногалогензамещенных алканов со спиртовыми растворами щелочей. Эта реакция, как и дегидратация, протекает в соответствии с правилом Зайцева:
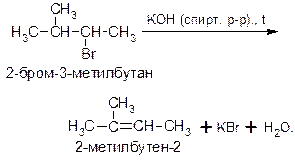
Алкены ‑ важные исходные вещества для промышленного органического синтеза. Из этилена получают этиловый спирт, полиэтилен, полистирол, используют в овощехранилищах для ускорения созревания плодов. Пропилен используют для синтеза полипропилена, фенола, ацетона, глицерина и других веществ.
Лекция 4
АЛКАДИЕНЫ
КЛЮЧЕВЫЕ СЛОВА: алкадиены, диеновые углеводороды, кумулированные, сопряженные и изолированные двойные связи, σ-связь, π-связь, sp2 - гибридизация, дивинил, изопрен, 1,2-присоединение, 1,4-присоединение, полимеризация, синтетический каучук, способ Лебедева получения дивинила.