Предшественник сульфаниламидных соединений был синтезирован в 1908 г., однако химикотерапевтические свойства их были обнаружены только в 1935 г. Все ныне применяемые препараты являются производными сульфаниловой кислоты, ее амида: 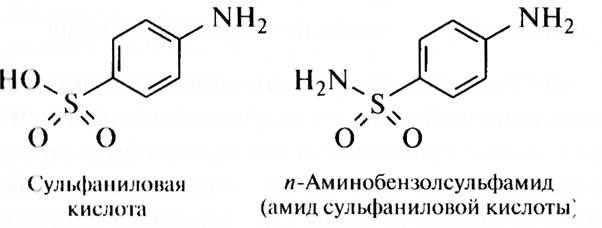
Структурную формулу сульфаниламидного препарата можно представить схемой:

Радикалы на схеме могут быть различны, что и предопределяет большое количество препаратов этой группы. Следует отметить, что большинство препаратов — первичные амины. Если же заменить эту аминогруппу на другие радикалы, то терапевтический эффект пропадает. Однако было установлено, что терапевтический эффект сохраняется, если радикал (заместитель) в первичной аминогруппе после гидролиза позволяет образовать свободную аминогруппу. Изменение положения аминогруппы, введение в ароматическое кольцо дополнительных радикалов приводит к значительной потере терапевтического эффекта или его отсутствию. Замещение атома водорода в сульфамидной группе позволило получить препараты с меньшей токсичностью и различной активностью. Из-за отрицательного индуктивного эффекта S02-rpyппы препараты обладают NH-кислотностью и растворяются в щелочах с образованием солей:

Ацилирование сульфамидной группы приводит к образованию имидов, которые обладают еще большей NH-кислотностью и растворяются даже в карбонатах. Механизм антибактериального действия сульфаниламидов основан на схожести парааминобензойной кислоты и препаратов группы. В присутствии сульфаниламидов микробный фермент осуществляет синтез фолиевой кислоты не из парааминобензойной кислоты, а из ее заместителя. Поэтому получается синтез не фолиевой кислоты, а псевдофолиевой кислоты, при этом образовавшееся соединение не может участвовать в нормальном метаболизме микробной клетки - нарушается синтез белков и нуклеиновых кислот.
Синтез сульфаниламидных препаратов состоит из трех основных стадий: 1) получение хлорангидрида сульфаниловой кислоты; 2) получение соответствующего аминопроизводного Rt-NH2; 3) конденсация хлорангидрида сульфаниловой кислоты с аминопроизводным. Рассмотрим подробнее происходящие процессы.
Первая стадия у всех препаратов общая. Ввиду того, что сульфаниловая кислота не может быть непосредственно превращена в хлорангидрид, ее предварительно ацилируют (защищают аминогруппу) и уже ацетилсульфаниловую кислоту превращают в хлорангидрид:

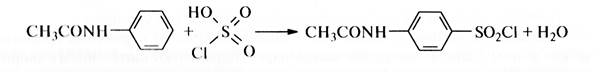
Хлорангидрид ацетилсульфаниловой кислоты можно также получить из ацетанилида действием на него хлорсульфоновой кислоты:
Вторая стадия синтеза индивидуальна для каждого препарата и зависит от R. Нa третьей стадии хлорангидрид ацилсульфаниловой кислоты конденсируют с соответствующим амином:

Реакцию необходимо проводить в слабощелочной среде для нейтрализации выделяющейся хлороводородной кислоты, чтобы она не вступала в реакцию с амином с образованием соли. Ацильную группу омыляют, так как ацилирован-ные препараты не дают терапевтического эффекта. Омыление проводят щелочью, поэтому получаются натриевые соли. Их обрабатывают кислотой и затем проводят очистку:
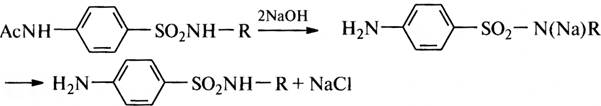
В зависимости от условий синтеза могут получаться таутомеры — амидо- или имидо-формы. Препараты этой группы могут иметь полиморфные модификации, а также быть в виде гидратов или сольватов, что обусловлено технологическим процессом производства и влияет на внешний вид получаемых соединений. Сульфаниламиды проявляют амфотерные свойства. Основные свойства зависят от наличия первичной ароматической аминогруппы. Надо отметить, что в растворах они образуют соли с минеральными кислотами, но соли эти сильно гидролизованы, так как основные свойства проявляются слабо, из-за сопряжения атома азота с ароматическим кольцом. Кислотные свойства выражены сильнее — за счет наличия группы -SO2-NH-, которая содержит подвижный атом водорода, как упоминалось ранее, из-за отрицательного индуктивного эффекта:
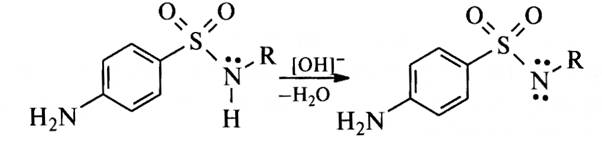
Классификацию сульфаниламидов можно провести двумя способами: I) по химическому строению. В этом случае их подразделяют на а) препараты, замещенные по амидной группе; б) на препараты, замещенные по аминогруппе; в) препараты, замещенные по обеим группам; 2) по продолжительности действия (фармакологическая классификация). В этом случае их делят на препараты корочкою действия, среднедлительного, длительного и сверхдлительного действия.
Испытания на подлинность
Имеются групповые и частные реакции на препараты.
Групповые:
Реакция образования азокрасителя — общая реакция на первичные ароматические амины. Если аминогруппа замещена, ее гидролизуют кипячением с хлороводородной кислогой.
Реакции конденсации — образуют продукты конденсации с 2,4-динитрохлорбензолом в щелочной среде и в кислой среде окрашенные продукты конденсации с ванилином (желтое), формальдегидом (розовое или желто-оранженое), пара-диметиламинобензальдегидом (желтое).
Лигниновая проба — разновидность реакций образования шиффовых оснований; проводится на газетной бумаге или древесине. Первичный ароматическим амин взаимодействует с находящимся в составе лигнина сиреневым альдегидом, или ванилином и дает шиффово основание оранжево-желтого цвета.
Реакции галогенирования — основаны на активировании бензольного кольца донорской аминогруппой; галогены направляются в орто-положение от аминогруппы (пара-положение уже занято сульфамидной группой). Эти реакции могут использоваться как в качественном, так и количественном анализе.
Реакции с растворами солей тяжелых металлов — некоторые ионы тяжелых металлов могут замещать атом водорода в сульфамидной группе, и образовывать внутрикомплексные соединения.
Реакция обнаружения серы — серу можно обнаружить после окисления органической части молекулы концентрированной азотной кислотой (минерилизация). Далее сульфат-ион обнаруживают реакцией с хлоридом бария.
Реакции пиролиза — при термическом разложении в сухой пробирке плавы препаратов приобретают различную окраску, при этом выделяются газообразные продукты.
Реакции с нитропруссидом натрия — препараты взаимодействуют с 1% раство ром нитропруссида натрия в щелочной среде, а после подкисления реакционной смеси минеральной кислотой дают продукт красно-коричневого цвета, или осадок
Реакции окисления — при этом образуются окрашенные соединения хиноидной структуры (индофенолы).
Частные реакции характеризуют строение конкретного препарата по группировкам, входящим в его состав. Например, у натриевых солей препаратов под тверждают наличие иона натрия.