СЛОЖНЫЕ ЭФИРЫ.
Производные карбоновых кислот, в которых атомы водорода карбоксильной группы замещены на углеводородные радикалы, называют сложными эфирами.
Общая формула сложных эфиров 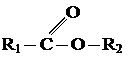
Физические свойства.
Сложные эфиры низших карбоновых кислот представляют собой летучие жидкости, многие из которых обладают приятным фруктовым или цветочным запахом. Они практически нерастворимы в воде.
Получение сложных эфиров.
В основе получения сложных эфиров лежит реакция этерификации между карбоновой кислотой и спиртом. Реакция катализируется сильными кислотами.
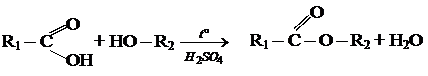
Химические свойства.
1. гидролиз

2. горение
2CH3 – CО – O – СH3 + 7О2 → 6СО2 + 6 H2O
уксуснометиловый эфир
ЖИРЫ
Жирами называют сложные эфиры трехатомного спирта глицерина и высших карбоновых кислот.

1. Животные жиры.
Животные жиры обычно твердые вещества (исключение - рыбий жир). Животные жиры используются в пищу и для получения твердого мыл.
2. Растительные жиры (масла).
Растительные жиры обычно жидкие (исключение - пальмовое масло). Растительные жиры используются в пищу, для получения маргарина, для получения олифы.
ТЕМА: УГЛЕВОДЫ.
1. Моносахариды (глюкоза, фруктоза) - гидролизу не подвергаются.
2. Дисахарида (сахароза, лактоза) – при гидролизе образуют две молекулы моносахаридов.
3. Полисахарида (крахмал, целлюлоза) – при гидролизе образуют много молекул моносахаридов.
ГЛЮКОЗА
1. Физические свойства.
Твердое, белое f кристаллическое вещество, вкус сладкий, растворима в воде.
2. Строение молекулы.
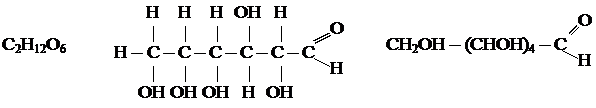
Глюкоза - альдегидоспирт.
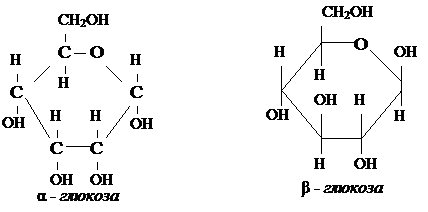
3. Химические свойства.
3.1 Глюкоза как многоатомный спирт реагирует без нагревания с гидроксидом меди, при этом образуется темно-синий раствор глюконата меди.
3.2 Реакции по альдегидной группе.
а) реакция «серебряного зеркала»
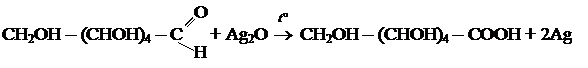
б) с гидроксидом меди
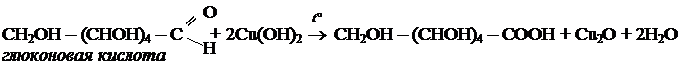
3.3 Брожение глюкозы.
а) спиртовое
С6Н12О6 → 2С2Н5ОН + 2СО2↑
б)молочнокислое
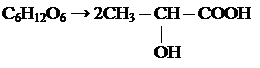
в) маслянокислое С6Н12О6 → С3Н7СООН + 2СО2↑ + 2Н2↑
4. Получение и применение глюкозы.
(С6Н10О5)n + nН2О → nС6Н12О6
крахмал
Глюкоза используется в медицине, для получения этанола, при изготовлении зеркал.
ФРУКТОЗА .
Фруктоза является изомером глюкозы.
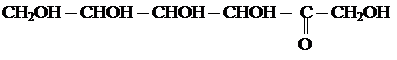
Фруктоза - кетоноспирт. Вместе с глюкозой входит в состав меда, имеет более сладкий вкус, чем глюкоза.
Задача. Сколько литров раствора этанола (плотность 0,79) с массовой долей С2Н5OH 95 %получится при спиртовом брожении 36 кг глюкозы?
САХАРОЗА.
Физические свойства.
Сахароза - твердое, белое, кристаллическое вещество, растворима в воде, вкус сладкий.
Сахароза в природе.
Сахароза входит в состав сока многих растении. Например, в соке сахарного тростника ее 14-16 %, а в соке сахарной свеклы 16-21 %.
Химические свойства.
1. Гидролиз.
С12Н22О11 + Н2О 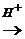 С6Н12О6 + С6Н12О6
С6Н12О6 + С6Н12О6
глюкоза фруктоза
2. Сахароза как многоатомный спирт реагирует с гидроксидом меди, при этом образуется: ярко-синий раствор сахарата меди.
3. Сахароза реагирует с гидооксидом калция. Это свойство лежит в основе получения сахара их свеклы и его дальнейшей очистки.
С12Н22О11 + 2СА(ОН)2 → С12Н22О11 · 2СаО + Н2О
сахарат кальция
С12Н22О11 · 2СаО + 2СО2 → С12Н22О11 + 2 СаСО3↓
Применение сахарозы.
Сахароза используется в кондитерском производстве и для получения, этилового спирта.
Задача. Сколько тонн сахарной свеклы с массовой долей сахарозы 20 %будет подвергнуто гидролизу для получения глюкозы массой 1т?
КРАХМАЛ.
Крахмал - природный полимер, макромолекулы которого состоит из остатков α-глюкозы и имеют в основном разветвленное строение.
Физические свойства.
Крахмал - твердое, белое, аморфное вещество без вкуса и запаха. Крахмал нерастворим в холодной воде, в горячей воле образует коллоидный раствор (клейстер).
Крахмал в природе.
Крахмал является одним из продуктов фотосинтеза и поэтому широко распространена в природе. Зерна риса содержат до 86 %крахмала, пшеницы до 75 %, кукурузы - до 72 %. Вклубнях картофеля содержание крахмала достигает 24 %.
Химические свойства.
1. Гидролиз
(С6Н10О5)n + nН2О 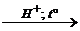 nС6Н12О6
nС6Н12О6
2. Качественная реакция на крахмал.
Реактивом на крахмал является раствор йода. Результат реакции - синее окрашивание.
Применение крахмала.
Крахмал является одним из важнейших компонентов пищи. Значительное количество крахмала перерабатывается на патоку, глюкозу, пищевой спирт, молочную кислоту. Крахмал используют в текстильной промышленности дляотделки тканей.
Задача. Какую массу кукурузных зерен надо взять для получения спирта массой 115 кг, с массовой долей C2H5OH 96 %, если массовая доля крахмала в кукурузных зернах составляет 70 %?
ЦЕЛЛЮЛОЗА (КЛЕТЧАТКА).
Целлюлоза - природный полимер, макромолекулы которого состоят из остатков /3 -глюкозы и имеют линейное строение.
Физические свойства.
Целлюлоза - твердое, белое, аморфное вещество без вкуса и запаха. Она нерастворима в воде и органических растворителях, но растворима в аммиачном растворе сульфата меди.
Химические свойства.
1. Гидролиз
(С6Н10О5)n + nН2О 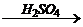 nС6Н12О6
nС6Н12О6
2. Образование сложных эфиров.
[С6Н7О2(OH)3]n + 3nНNО3 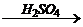 [С6Н7О2(ONO2)3]n + 3nН2О
[С6Н7О2(ONO2)3]n + 3nН2О
тринитрат целлюлозы
[С6Н7О2(OH)3]n + 3nСН3СООН → [С6Н7О2(OСОСН3)3]n + 3nН2О
триацетат целлюлозы
Целлюлоза в природе.
Целлюлоза является основной частью стенок растений, Относительно чистой целлюлозой являются волокна хлопчатника. Древесина содержит от 40 до 50 %целлюлозы.
Применение целлюлозы.
Из целлюлозы изготавливают искусственные волокна, полимерные пленки, пластмассы, бездымный порох, бумагу.
Образование крахмала и клетчатки в зеленых растениях.
6СО2 + 6Н2О 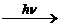 С6Н12О6 + 6О2
С6Н12О6 + 6О2
nС6Н12О6 → (С6Н10О5)n + nН2О
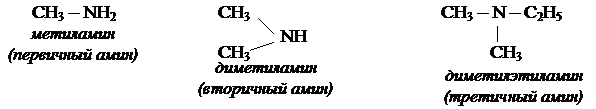
ТЕМА: АМИНЫ
Аминами называет органические производные аммиака, в котором один, два или все три атома водорода замещены на углеводородный радикал.
Классификация и номенклатура аминов.