ФАЗОВОЕ РАВНОВЕСИЕ.
Фундаментальные представления химической термодинамики применимы для характеристики фазового равновесия и фазовых переходов.
Фазовое равновесие означает одновременное существование термодинамически равновесных фаз в гетерогенной системе.
Например, жидкость со своим насыщенным паром (система жидкость-газ), вода и лед при температуре плавления (система жидкость-твердое тело), две несмешивающиеся жидкости (система жидкость-жидкость) и т.д.
Фазовое равновесие в зависимости от состава и параметров системы определяется правилом фаз Гиббса.
Система
/ \
гомогенная (однофазная) гетерогенная (многофазная)
Фаза –гомогенная часть гетерогенной системы, обладающая определенным набором физических и химических свойств и отделенная от других фаз поверхностью раздела.
Компонент –часть системы, которая может быть выделена из неё и существовать вне этой системы.
Например, раствор NaCl: компоненты NaCl и вода.
Число независимых компонентов (параметров) равно общему числу компонентов (параметров) минус число уравнений, связывающих их.
ФАЗОВЫЕ ПЕРЕХОДЫ.

1) кристаллизация (ΔH<0)
2) плавление (ΔH>0)
3) испарение (ΔH>0)
4) конденсация (ΔH<0)
5) сублимация (возгонка) (ΔH>0)
6) десублимация (ΔH<0)
УСЛОВИЯ РАВНОВЕСИЯ В ГЕТЕРОГЕННОЙ СИСТЕМЕ.
Возможность T1≠T2 
Направление T1>→T2< 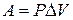
Предел T1=T2 T, P – факторы интенсивности
Для определения возможности, направления и предела протекания процессов в гетерогенных системах можно воспользоваться выражением  (µi – химический потенциал) – фактор интенсивности фазового перехода.
(µi – химический потенциал) – фактор интенсивности фазового перехода.
На рисунке представим схему перехода некоторого малого количества компонента i из фазы I в фазу II.
|
|


µiI >µiII
Возможность фазового перехода определяется химическим потенциалом.
1) Возможность процесса: µiI ≠ µiII
2) Направление процесса: если µiI >µiII , тоI → II
3) Предел процесса: µiI = µiII
Если, например, жидкость находится в равновесии со своим паром, то химический потенциал является одним и тем же для пара и жидкости (µiж = µiп). При повышении температуры химический потенциал компонента в газовой среде снижается и становится ниже его химического потенциала в жидкой среде. Тогда в соответствии с условием µiж > µiп часть жидкости будет самопроизвольно испаряться до тех пор, пока не произойдет выравнивание химических потенциалов сопряженных фаз.
Влияние внешних параметров на фазовое равновесие и фазовые переходы определяется правилом фаз Гиббса.
ПРАВИЛО ФАЗ ГИББСА.
ВЫВОД И АНАЛИЗ.
Для выражения состава двухкомпонентной системы достаточно знать долю одного компонента в системе, а содержание второго компонента будет вполне определенным.
Для системы, в состав которой входят два и более компонентов, можно ограничиться содержанием (К-1) компонентов. Если, например, в стакане чая содержится 3 компонента (вода, чай, сахар), а сахара содержится 0,7%, чая 0,3%, то естественно, что остальное приходится на воду, то есть достаточно знать содержание двух компонентов – на один меньше состава системы.
При распределении этих компонентов в Ф фазах потребуется Ф(К-1) данных для описания состава системы. Когда состав системы изменяется в зависимости от внешних параметров (например, температуры, давления), число которых составляет n, общее число данных о составе системы равно Ф(К-1)+n.
|
|
ЧИСЛО УРАВНЕНИЙ, СВЯЗЫВАЮЩИХ РАВНОВЕСНОЕ СОСТОЯНИЕ К-КОМПОНЕНТОВ В Ф-ФАЗАХ.
Напомню, что равновесное состояние характеризуется отсутствием изменений энергии Гиббса или энергии Гельмгольца ΔG=0 или ΔF=0.
Условием равновесия фаз в гетерогенной многокомпонентной системе является равенство химических потенциалов любого компонента во всех фазах. Тогда число уравнений, связывающих равновесное состояние К компонентов в Ф фазах равно:
 Всего (Ф-1) уравнений
Всего (Ф-1) уравнений
 …………………….. (Ф-1) уравнений
…………………….. (Ф-1) уравнений
.
.
.
 …………………….. (Ф-1) уравнений
…………………….. (Ф-1) уравнений
| К(Ф-1) – общее число уравнений |
Для характеристики фазового состояния системы введено понятие о числе степеней свободы.
Число степеней свободы равновесной термодинамической системы – это число параметров (например температура, давление, концентрация для многокомпонентной системы), которые можно произвольно менять без изменения числа и вида фаз.
Число степеней свободы обозначается через С.
Напомню, что общее число параметров системы выражается как Ф(К-1)+n. Но не все компоненты Ф(К-1)+n, определяющие состав системы, независимы друг от друга. Число степеней свободы С равно общему числу данных о составе системы за вычетом числа связей между ними К(Ф-1):
С=Ф(К–1)+ n–К(Ф–1) или
С = К– Ф + n *
В пределах Земли все системы находятся в одинаковых условиях, и воздействие гравитационного, магнитного, электрического и других полей можно не учитывать. К числу внешних параметров, учитываемых для конденсированных систем (жидкость, твердое тело), относятся температура, n=1, а для неконденсированных систем (газ) – ещё и давление, т.е. n=2. Таким образом, уравнение * С = К– Ф + n принимает вид:
|
|
С = К–Ф+1 ** С = К–Ф+2 ***
(Т) (Т, Р)
Все три уравнения выражают правило фаз Гиббса, которое формулируется следующим образом:
Число степеней свободы равновесной термодинамической системы, на которую влияют n внешних факторов, равно числу независимых компонентов системы минус число фаз плюс n.
С – число степеней свободы.
К – число независимых компонентов.
Ф – число фаз системы.
n – число внешних параметров, влияющих на систему.
n=2 (Т,Р); n=1 (Т или Р)
|
С=1-1+2=2
КЛАССИФИКАЦИЯ СИСТЕМ В СООТВЕТСТВИИ С ПРАВИЛОМ ФАЗ ГИББСА.
1) По числу компонентов:
К=1 – однокомпонентная
К=2 – двухкомпонентная
К=3 – трехкомпонентная
2) По числу фаз:
Ф=1 – однофазная (гомогенная)
Ф=2 – двухфазная (гетерогенная)
Ф=3 – трехфазная (гетерогенная)
3) По числу степеней свободы:
С=0 – инвариантная
С=1 – моновариантная
С=2 – дивариантная
С=3 – тривариантная
t
Например, CaCO3(тв) → CuO(тв)+CO2(г)↑
3 компонента, 2 фазы (гетерогенная система)
С=К-Ф+2=3-2+2=3
Число степеней свободы не может быть меньше нуля. Отрицательное значение числа степеней свободы указывает на то, что не все компоненты находятся в равновесии во всех фазах.