канд. тех. наук Г.Н. Забегалова
канд. техн. наук И.С. Полянская,
Вологодская государственная молочнохозяйственная академия им. Н.В.Верещагина
Д-р техн. наук, заслуженный деятель науки РФ В.Ф. Семенихина
ВНИИ молочной промышленности
Использование тяжелых металлов в различных современных технологиях металлургической промышленности, машиностроения, приборостроения, предметов бытового назначения, фармацевтической и других видах промышленности привело к значительному загрязнению объектов окружающей среды этими токсичными элементами.
Свинец, в частности, стал в России наиболее распространенным токсикантом из группы тяжелых металлов [1]. Большую озабоченность вызывает возможность накопления свинца в кормовых и пищевых растениях до уровней, способных оказать вредное воздействие на организм животных и человека. В непосредственной близости от автострад и на расстоянии до 50 метров содержание этого токсиканта в кормовых растениях может быть в 100 раз больше фонового. Содержание свинца в печени коров при использовании таких кормовых растений повышается в 20 раз, в мясе и молоке – в 3-4 раза.
После попадания в кровеносную систему свинец разносится по всему телу, включаясь в клетки крови и плазму. В крови свинец в основном включается в эритроциты, где его концентрация в 16 раз выше, чем в плазме.
Установлено, что даже небольшое регулярное поступление свинца в организм, если оно продолжительное, приводит к хроническому заболеванию. Соединения свинца относятся к группе тиоловых ядов. Попав в организм человека или животного, свинец вступает в химическое взаимодействие с сульфгидрильными группами различных макромолекул и, в первую очередь, ферментов. Токсичность свинца проявляется в подавлении синтеза гемоглобина, ведущее к анемии, действии на нервные ткани и вегетативную нервную систему.
Экспертами ФАО и ВОЗ установлена величина максимально допустимого поступления свинца для взрослого человека допустимая суточная доза составляет около 0,007 мг/кг массы тела, ПДК свинца в молоке-сырье 0,1 мг/л [1].
С 2002 года Агрохимцентр г Вологды проводит мониторинг площадей сельхозугодий, чтобы оценить ситуацию по содержанию тяжелых металлов в почвах Вологодской области. На основе обобщенных данных за 15 лет содержания тяжелых металлов в почвах сельхозугодий области можно сделать следующие выводы: средняя концентрация тяжелых металлов в почвах не превышала предельно допустимых концентраций (ПДК), а уровень содержания свинца не превышал отметку 0,5 долей ПДК.
Относительно спокойная экологическая обстановка в области по содержанию тяжелых металлов не позволяет однозначно объявить снятой данную проблему.
Экспериментальные данные, показывают, что при поступлении в исходное молоко солей тяжёлых металлов в количестве всего 0,005 мг/л может затормозить нормальный процесс сквашивания в среднем от 8 до 23 %. Удлиняется процесс сквашивания молока при выработке кисломолочных продуктов, замедляется развитие полезной микрофлоры, которая используется при выработке продуктов. Особенно отрицательное влияние оказывают тяжелые металлы на качество творога и сыра. Наблюдается появление постороннего вкуса и запаха, консистенция творога мажущаяся, сыра - крошливая, что обесценивает продукт [1]. Поэтому рассматривается возможность элиминации тяжелых металлов из животноводческой продукции, в частности молока-сырья, с помощью различных сорбентов. Термин «сорбент» включает в себя адсорбенты, абсорбенты, ионообменные материалы и комплексообразователи. Увеличивается число работ, посвященных биосорбции.
В литературе встречаются данные о способности бактерией Аlkaligenes eutrophus, грибов, водорослей и др. к извлечению тяжелых металлов. В производстве функциональных пищевых продуктов получило активное развитие использование сорбционных, радиопротекторных свойств пектинов, хитозана и др. комплексонов, полимеров, пищевых волокон [2, 3, 4]. В международных депозитариях молочнокислых микроорганизмов имеются указания на изученную способность отдельных штаммов (Lactobacillus plantarum B884, Lactobacillus plantarum В815 молочнокислых микроорганизмов связывать тяжелые металлы [5]. Пробиоотические штаммы Bifidobacterium longum, также снижают содержание в организме ряда тяжелых металлов [6]. Опосредованно, через восстановление нормальной микробиоты кишечника, пробиотики, в целом, детоксицируют соли тяжелых металлов за счет перевода их в нетоксические соединения, сорбцию токсических элементов на своей поверхности с последующей их элиминацией [7, 8].
Однако такая сорбция в форме радиопротекторной служит выведению тяжёлых металлов (в том числе радионуклеидов) из организма. Основная цель экспериментов представленных опытов - исследование эффективности способов элиминирования тяжелых металлов из молока-сырья: биопротекторных свойств.
Объектами настоящего исследования служили: сборное молоко коров ряда хозяйств Вологодской области, поступающего на УОМЗ и вырабатываемые из него в лабораторных условиях молочные продукты: 2 вида простокваши, ацидофилин, кефир, творог домашний. Выработка продуктов осуществлялась в соответствии с технологическими инструкциями: кефир, простокваша, ацидофилин – термостатным способом, творог кислотносычужным методом, масло – методом сбивания. Продукты вырабатывали как из исходного сырья, так и сырья с «внесёнными» тяжелыми металлами, используя поливидовые многоштамовые закваски, предназначенные для соответствующего продукта. Основные методы исследований: инверсионная вольтамперометрия; ряд показателей определялся по стандартным и общепринятым методикам. Повторность опыта пятикратная, Р=0,95.
На первом этапе исследования мы изучали эффективность детоксикации молока сорбентами, в частности полифепаном (гидролизным лигнином) при производстве следующих продуктов: кефир, мечниковская простокваша, простокваша и ацидофильное молоко. По результатам эксперимента были построены графики динамики процесса сквашивания (рис. 2-5).
| рис. 2-5 | |||
| Рис. 2- Динамика процесса сквашивания простокваши: К2-3 – контроль, П12-3 – после детоксикации дозой сорбента 0.3 г/кг, П22-3 - после детоксикации дозой сорбента 0.6 г/кг. | Рис.3 - Динамика процесса сквашивания мечниковской простокваши: К1-2 – контроль, П11-2 – после детоксикации дозой сорбента 0.3 г/кг, П21-2 - после детоксикации дозой сорбента 0.6 г/кг. | Рис. 4- Динамика процесса сквашивания ацидофильного молока: К3-2 – контроль, П13-2 – после детоксикации дозой сорбента 0.3 г/кг, П23-2 - после детоксикации дозой сорбента 0.6 г/кг. | Рис. 5 - Динамика процесса сквашивания кефира: К4-2 – контроль, П14-2 – после детоксикации дозой сорбента 0.3 г/кг, П24-2 - после детоксикации дозой сорбента 0.6 г/кг. |
Во всех случаях детоксикация молока-сырья биосорбентами несколько ускорила процесс сквашивания исследуемых продуктов, что говорит о том, что снижение тяжёлых металлов в молоке активизирует развитие заквасочной микрофлоры. Получены патенты на способы очистки молока сырья от тяжелых металлов [10-14].
Табл. 1 Распределение содержания свинца по различным фракциям молока
| № | Фракция молока | Массовая доля жира, % | Свинец | |
| Содержание, мг/кг | Среднее содержание, % | |||
| Молоко | 3,65 | 0,289 + 0,066 | ||
| Обезжиренное молоко | 0,04 | 0,258 + 0,081 | ||
| Белковая (казеин) | 0,55 | 0,315 + 0,072 | ||
| Молочная (творожная) сыворотка (безбелковая, безжировая) | - | 0,196 + 0,048 | ||
| Сливки (жиро-белковая) | 0,385 + 0,126 | |||
| Масло (жировая) | 72,5 | 0,562 + 0,122 | ||
| Пахта (белковая) | 0,4 | 0,191 + 0,047 |
Из таблицы 1 следует, что 57% свинца, содержащегося в молоке, в среднем переходит в сыворотку и пахту (18%). В казеине концентрируется 18% свинца, 10% попадает в масло. Аналогичные результаты получаются и в случае «внесенных» микроэлементов: с сывороткой и пахтой выделяется 72% свинца, в казеин и масло попадает соответственно 18 и 10%.
Цель второго этапа исследования - получение данных сравнительной эффективности различных штаммов, применяемых в составе заквасочной микрофлоры при производстве продуктов с отделением сыворотки (в частности, творога, творожных изделий, сыра) по биопротекторным свойствам, понимаемым в конкретном случае как способность сдвигать распределение свинца в сторону сыворотки, к уменьшению попадания свинца в белковую фракцию (белковый продукт). Сырье: обезжиренное молоко 0,04% с содержанием свинца (с учетом «внесённого») 0,128+0,052 мг/кг (100%).
При выработке продукта сырьё заквашивали одним из 9 вариантов штаммов и их консорциумов (табл. 2).
Табл. 2. Распределение содержания свинца по различным фракциям казеин, сыворотка в зависимости от применяемой закваски
| № | Варианты применяемых заквасок | Белковая (казеин) | Сыворотка (безбелковая, безжировая) | ||
| Содержание, мг/кг | Содержание, % | Содержание, мг/кг | Среднее содержание, % | ||
| Lactococcus lactis subsp. lactis; Lactococcus lactis subsp. cremoris (БК-Углич-№7) | 0,017 + 0,01 | 13 + 1 | 0,111 + 0,06 | ||
| Lactococcus lactis subsp. lactis; Lactococcus lactis subsp. cremoris; Lactococcus lactis subsp. lactis biovar diacetylactis Leuconostoc (БК-Углич-№4) | 0,009 + 0,06 | 7 + 1 | 0,119 + 0,07 | ||
| Lactobacillus acidophilus (невязкий) | 0,023+0,008 | 14 + 1 | 0,110 + 0,067 | ||
| Lactococcus lactis subsp. lactis, + Lactococcus lactis subsp. сremoris + Lactococcus lactis subsp. lactis biovar diacetylactis + Leuconostoc mesenteroides subsp. cremoris + Lactobacillus acidophilus | 0,010 + 0,06 | 8 + 1 | 0,118 + 0,08 | ||
| Streptococcus thermophilus | 0,017 + 0,02 | 13 + 1 | 0,111 + 0,08 | ||
| БК-Углич№7К + Streptococcus thermophilus | 0,017 + 0,03 | 13 + 1 | 0,111 + 0,08 | ||
| Lactobacillus plantarum | 0,017 + 0,06 | 13 + 1 | 0,111 + 0,07 | ||
| Bifidobacterium bifidum + Lactobacillus plantarum | 0,015 + 0,08 | 12 + 1 | 0,113 + 0,09 | ||
| БК-Углич№7К+ Lactobacillus plantarum | 0,015 + 0,06 | 12 + 1 | 0,113 + 0,08 |
По результатам эксперимента прослеживается закономерность, что более высокая степень отхода свинца в сыворотку, соотвественно более чистый продукт получается при применении вариантов консорциумов штаммов №4 (закваска для ацидофильного творога) и №2 БК-Углич-№4 (закваска для большинства видов сыров и творога). Оба консорциума содержат гетероферментативные штаммы лейконостоков и лактококки подвида diacetylactis.
В качестве предположения выдвинута гипотеза: среди метаболитов гетероферментативных микроорганизмов имеются такие, которые проявляют свойства антидода. Таким метаболитом, в частности может быть димеркаптоянтарная кислота, которая переводит свинец в растворимую форму. Исходя из исследований, проводимых ещё в 1962-1969 годах, использование этой кислоты как антидода при отравлении животных тиоловыми ядами показало высокую эффективность. Наличие в её формуле (рис. 6) двух рядом расположенных сульфгидрильных SH-групп приводит при взаимодействии с тиоловыми ядами к образованию нетоксичного комплекса, он быстро выводятся из организма.
Таким образом, димеркаптоянтарная кислота может быть одним из механизмов протекторных свойств гетероферментативных пробиотических микроорганизмов. Для изучения полученного эффекта биопротекторных свойств пробиотических штаммов, необходимы дальнейшие исследования.

Рис. 6. Димеркаптоянтарная кислота
По результатам эксперимента были построены графики динамики процесса сквашивания рис. 1– 5.
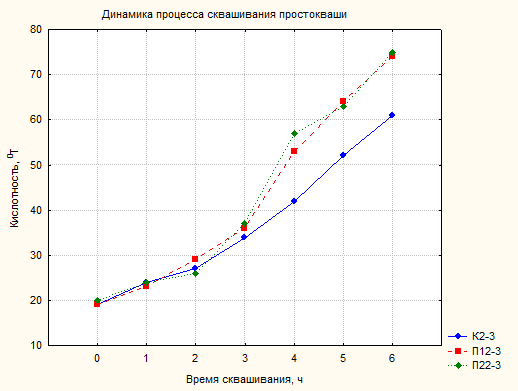
Рис. 1- Динамика процесса сквашивания простокваши:
К2-3 – контроль, П12-3 – после детоксикации дозой сорбента 0.3 г/кг, П22-3 - после детоксикации дозой сорбента 0.6 г/кг.

Рис. 2 - Динамика процесса сквашивания мечниковской простокваши:
К1-2 – контроль, П11-2 – после детоксикации дозой сорбента 0.3 г/кг, П21-2 - после детоксикации дозой сорбента 0.6 г/кг.

Рис. 3 - Динамика процесса сквашивания ацидофильного молока:
К3-2 – контроль, П13-2 – после детоксикации дозой сорбента 0.3 г/кг, П23-2 - после детоксикации дозой сорбента 0.6 г/кг.

Рис. 4 - Динамика процесса сквашивания кефира:
К4-2 – контроль, П14-2 – после детоксикации дозой сорбента 0.3 г/кг, П24-2 - после детоксикации дозой сорбента 0.6 г/кг.
По представленным графикам можно сделать следующий вывод: детоксикация молока – сырья гидролизным лигнином несколько ускорила процесс сквашивания исследуемых продуктов, что говорит о том, что снижение содержания свинца, кадмия и ртути активизирует развитие заквасочной микрофлоры.
Список литературы
1. Забегалова Г.Н. Разработка технологических приёмов детоксикации молока-сырья от солей тяжёлых металлов / Дисс. на соиск. ст. к.т.н. Вологда-Молочное. 2006. 189 с.
2. Садовой В.В., Щедрина Т.В. Исследование квантово-химических характеристик фрагмента молекул биологически активной добавки хитозана // Международный научно-исследовательский журнал. 2016. № 46. С. 166-169.
3. Полянская И.С., Семенихина В.Ф. Классификация функциональных пищевых продуктов на молочной основе // Молочная промышленность. 2017. № 2. С. 56-58.
4. Маркова М.Е., Урьяш В.Ф, Степанова Е.А., Груздева А.Е. и др. Сорбция тяжелых металлов высшими грибами и хитином разного происхождения в опытах in vitro // Вестник Нижегородского университета им. Н.И. Лобачевского, 2008. № 6 С. 118–124
5. Национальный биоресурсный центр - Всероссийская коллекция промышленных микроорганизмов (ВКПМ) / ФГУП ГосНИИгенетика https://www.genetika.ru/vkpm/
6. Кван О.В., Мирошников С.А., Дерябин Д.Г., Беседкин В.Н. Неоднозначность влияния пробиотиков на обмен токсическихэлементов в организме кур-несушек // Вестник ОГУ. 2006. №2.
7. Бондаренко В.М., Чупринина Р.П., Аладышева Ж.И., и др. Пробиотики и механизмы их лечебного действия //
Экспериментальная. и клиническая гастроэнтерологоя 2004. № 3. С. 83-87.
8. Ардатская М.Д. Пробиотики, пребиотики и метабиотики в коррекции микроэкологических нарушений кишечника // Медицинский совет. 2015. № 13. С 94-99.
9. ГОСТ Р 51301-99 «Продукты пищевые и продовольственное сырье. Инверсионно-вольтамперометрические методы определения содержания токсичных элементов (кадмия, свинца, меди и цинка).
10. Патент РФ № 2006116091/13, 10.05.2006 Забегалова Г. Н., Охрименко О.В., Чекулаев Л. Н. Способ очистки молока-сырья от свинца // Патент России № 2326549. 2008. Бюл. №17
11. Патент РФ № 2006118909/13, 30.05.2006. Охрименко О.В., Забегалова Г. Н., Чекулаев Л. Н. Способ очистки молока-сырья от кадмия // Патент России № 2327357. 2008. Бюл. №18
12. Патент РФ № 2010123329/13, 07.06.2010. Способ получения молока-сырья для производства функциональных продуктов // Патент России № 2441397. 2011. Бюл. № 35.
13. Патент РФ № 2010129412/13, 15.07.2010. Полянская И.С., Топал О.И. Способ очистки молока-сырья от токсичных металлов // Патент России № 2441397. 2012. Бюл. № 4.
14. Оксенгендлер Г.И. Яды и противоядия. Л.: Наука. 1982. 192 с
Ирина Сергеевна Полянская, канд. техн. наук, доцент кафедры технологии молока и молочных продуктов
Галина Николаевна Забегалова, канд. техн. наук, доцент кафедры технологии молока и молочных продуктов
ФГБОУ ВПО «Вологодская государственная молочнохозяйственная академия им. Н.В.Верещагина»
Вера Филатовна Семенихина, д-р техн. наук., заслуженный деятель науки РФ, профессор, главный научный сотрудник
ФГБНУ «Всероссийский научно–исследовательский институт молочной промышленности»
Заварин Ю.М., Полянская И.С., Неронова Е.Ю., Закрепина Е.Н., Подхомутов Н.В., Семенихина В.Ф.
Увеличение бифидогенного фактора молочной сыворотки. Молочная промышленность. 2017, № 9. С. 65-66.

