ГЛАВА ОТЧЕТА
Для проведения пациент-ориентированных расчетов использованы персонифицированные трехмерные модели проксимальных анастомозов пяти обследованных пациентов, построенные по данным мультиспиральной компьютерной томографии (рис. 5.1 и рис. 3.4 в файле с иллюстрациями). Для каждой модели анастомоза рассчитывалось пульсирующее течение несжимаемой вязкой кровеимитирующей жидкости с плотностью, r=1000 кг/м3, и вязкостью, m=0.004 Па·с, без учета влияния упругости стенок сосудов и переноса тепла, с использованием квазиламинарной модели. Расчеты проведены в программе ANSYS CFX, в которой реализован метод численного решения нестационарных трехмерных уравнений Навье-Стокса по методу конечных объемов. Согласно этому методу, расчетная область разбивается на достаточно малые контрольные объемы, которые в программном пакете автоматически строятся вокруг узлов расчетной сетки. Для каждого из них применяются уравнения сохранения, записанные в интегральной форме. Для вычисления конвективных и диффузионных потоков через грани контрольных объемов использовалась схема второго порядка точности. Временная дискретизация также осуществлялась со вторым порядком точности. Шаг по времени составлял 0.01 с, при этом для каждого шага по времени выполнялось достаточное для сходимости решения число расчетных итераций.
Для построения расчетной сетки использовалась программа Ansys Meshing среды WorkBench программного пакета Ansys 19.2. Типично (рис.5.2), построенные неструктурированные сетки состоят из тетраэдральных элементов размером 0,3 мм, с 12 призматическими слоями у поверхности сосуда со сгущением к стенке. Коэффициент сгущения 1,4. Толщина призматического слоя 0,4 мм. Количество элементов сетки варьировалось от 2,7 до 3,4 млн для разных моделей. Размер элемента сетки выбирался таким образом, чтобы в артерии на торце участка модели с минимальным диаметром находилось не менее 5 ячеек. Размер призматического слоя соответствовал толщине пограничного слоя, оцененного по значению числа Рейнольдса.
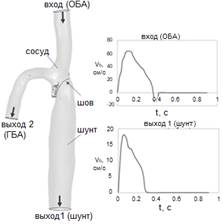
Для задания граничных условий были использованы данные ультразвуковых доплеровских измерений скорости кровотока, а именно, изменение среднерасходной скорости по циклу на входе и выходах различных участков исследуемых моделей анастомоза (рис.5.1). У пациентов наблюдалось различное время цикла: 0.90 с, 0.82 с, 0.97с, 0.67, 0.83 с для моделей пациентов Р., И., Е., К. и В., соответственно. Время увеличения расхода для всех случаев составляет порядка 0.1 с. Существенное различие также наблюдается в величине входной среднерасходной скорости в момент максимального расхода: 60 см/с, 80 см/с, 180 см/с, 90 см/с, 90 см/с для пациентов Р., И., Е., К. и В., соответственно. Модели характеризуются также индивидуальными соотношениями расходов на выходе из шунта к входному (в ОБА) в момент максимального входного расхода: для модели пациента Р. это соотношение составляет 0,6, для И. – 0,7, Е. – 0,2, К. – 0,5, В. – 0,4. Согласно ультразвуковым измерениям, на входе модели имеется фаза обратных токов (отрицательного значения скоростей) различной длительности: для пациента Р. – 0.05 с при максимальной амплитуде обратного тока 10 см/с, для И. – 0,2 с при амплитуде 30 см/с, для Е., К. и В. – 0,2 с при амплитуде 20 см/с.
На входе в расчетную область во всех случаях задавалась кривая среднерасходной скорости в общей бедренной артерии (ОБА), тип условия в программе ANSYS CFX – «inlet». Профиль входной скорости задавался плоским, с нулевыми значениями поперечных скоростей. На выходе из шунта для всех моделей задавалась аналогичная кривая при выборе типа граничного условия «outlet». Задание граничных условий на других участка сосудистого русла зависело от конкретной пациент-ориентированной модели. Например, модель пациента И. имеет три выхода (из шунта, из глубокой бедренной артерии и из поверхностной бедренной артерии, ПБА) в отличие от остальных моделей, имеющих два выхода (в них отсутствует кровоток в поверхностной бедренной артерии). Поэтому для модели пациента И. была также задана кривая на выходе из глубокой бедренной артерии (ГБА). На выходах из моделей, где не задаются условия по скорости, задавалось условие нулевого значения редуцированного давления (относительно референсного) при типе граничного условия «opening»: для моделей пациентов Р., Е., К., В. - это выход из ГБА, для модели пациента И. – из ПБА. На стенках моделей задавалось условие прилипания (все компоненты скорости равны нулю). В качестве начальных условий задавались нулевые поля всех компонент скорости и редуцированного давления.
Важнейшим определяющим (динамическим) параметром моделируемых течений является максимальное число Рейнольдса Re, построенное по величине среднерасходной скорости в момент максимального расхода в ОБА, внутреннему диаметру БА на входе, плотности и динамической вязкости крови. В настоящем исследовании максимальные числа Рейнольдса составляли 1050, 1000, 2260, 1600, 1590 для моделей пациентов Р., И., Е., К. и В., соответственно. Пульсирующий кровоток характеризуется также числом Уомерсли, построенным по внутреннему радиусу БА на входе, периоду пульсаций, плотности и динамической вязкости крови. В проведенных расчетах числа Уомерсли составляли 4,6, 3,5, 3,2, 5,4, 4,8 для моделей пациентов Р., И., Е., К. и В., соответственно.
Расчеты выполнялись на компьютере с частотой 2,6 ГГц, 16 Гб оперативной памяти и 12 процессорами. Расчет проводился с двойной точностью путем распараллеливания вычислений на 6 потоков. Для моделей пациентов Е. и К. расчет длился 15 часов, для В. и Р. – 20 часов, для И. – 30 часов. В ходе численного моделирования рассчитывались три временных циклов, на последнем из которых проводилось осреднение для вычисления средних по циклу сдвиговых напряжений и индекса колебаний сдвиговых напряжений.
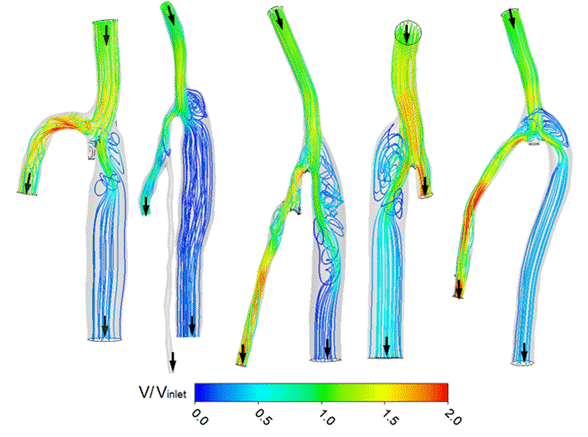
По результатам расчета выполнен анализ динамики трехмерного течения в каждой из моделей, а также изменений по циклу перепада давления DР. Кроме того, посредством осреднения по циклу вычислялись поверхностные распределения осредненного сдвигового напряжения на стенке, TAWSS, и индекса колебаний сдвиговых напряжений OSI. Информация данного рода важна по причине того, что наличие застойных зон в области анастомоза приводит, как правило, к уменьшению осредненных по времени сдвиговых напряжений и росту индекса их колебаний, что, предположительно, имеет влияет на процесс субинтимальной гиперплации после операции. Визуализация формирующихся в течении застойных зон выполнена путем построения линий тока в исследованных моделях в фазу максимального расхода (рис. 5.3). Установлено, что во всех моделях сразу за областью шва в шунте формируются застойные зоны различной протяженности, наибольшие их размеры наблюдаются в модели пациента Е.
Для момента максимального расхода были построены поверхностные (на стенках модели) распределения перепада давления (рис.5.4), вычисленного по отношению к давлению на выходе из шунта. В целом, наблюдается схожесть распределений. Примечательно также, что при значительных различиях в геометриях исследованных моделей значения общего перепада давления между входом в ОБА и выходом из шунта у моделей И., Е., К. и В. близки между собой, при этом в случае модели Р. перепад давления заметно меньше, что, по видимому, обусловлено меньшей пространственной извитостью сосудистого русла.
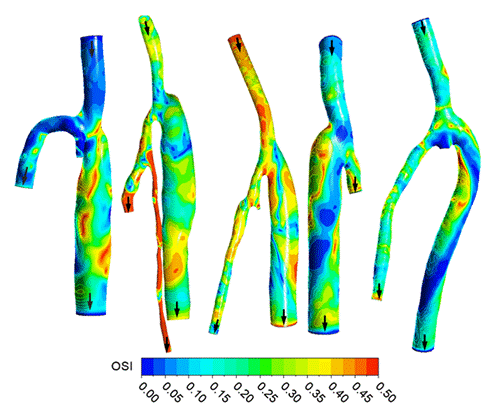
Анализировались поверхностные распределения величин TAWSS (рис. 5.5) и OSI (рис.5.6) в целях определения положения и размеров зон, в которых нарастание неоинтимы после операции наиболее вероятно. Известно, что низкие значения параметра TAWSS и высокие значения OSI указывают на высокие риски указанного послеоперационного осложнения. Общей особенностью всех моделей является наличие зон низких сдвиговых напряжений в области соединения сосуда с шунтом и по длине всего шунта. Что касается индекса колебаний сдвиговых напряжений, их «опасные» значения также локализованы в области шва и в различных местах по длине шунта. Однако в модели пациента Е. величина OSI принимает высокие значения и в самом сосуде на входе, что, вероятно, связано с большой входной скоростью. Для получения сопоставительных интегральных оценок, вычислялись значения TAWSS и OSI, осредненные по участку стенки сосуда (на длине 20 мм) в области соединения сосуда с шунтом (рис. 5.7).
Для модели пациента И. проведено сопоставление рассчитанного значений ТAWSS с данными ультразвуковых измерений толщины неоинтимы (рис.4.7). Измерения проводились от пятки анастомоза (нижний по потоку край пришивного шва) вдоль по стенке шунта на длине до 25 мм на ближней к ПБА стороне. Измеренное распределение толщины неоинтимы в целом коррелирует с расчетными данными по распределению сдвигового напряжения на стенке: при малых сдвиговых напряжениях наблюдается большая толщина неоинтимы и, наоборот, при больших сдвиговых напряжениях толщина неоинтимы меньше.
Проанализировано влияние соотношения диаметра сосуда к диаметру шунта в моделях на параметры течения. В исследованных случаях данное соотношение для модели пациента Р. составляет 0,7, для моделей И., Е., К., В. оно равно 0,63, 0,56, 0,88 и 0,88, соответственно. В случае близкого к единице соотношения диаметров (модели К. и В.) наблюдается наличие зон больших значений ТAWSS в шунте и малых значений OSI, что может снизить риск нарастания неоинтимы в области анастомоза.
Проводилось также сравнение картины течения в дистальном анастомозе пациента О. с течением в проксимальном анастомозе пациента Е. (рис. 5.9). Из набора исследованных моделей проксимального анастомоза модель Е. была выбрана для сравнения с моделью пациента О. (использовавшейся на этапе создания научного задела по проекту), с учетом некоторой схожести геометрий, а также близости значений среднерасходных скоростей в момент максимального расхода в шунтах обеих моделей. В дистальном анастомозе наблюдаются меньшие по размерам застойные зоны. Значения величины ТAWSS больше в шунте в области дистального анастомоза, что говорит о меньшем риске нарастания неоинтимы в самом шунте, однако за областью шва в сосуде за дистальным анастомозом значения ТAWSS низкие, и, следовательно, повышен риск нарастания неоинтимы в самом сосуде за анастомозом.
| 
|

| 
|
| Рисунок 5.1. Модели проксимальных анастомозов и граничные условия для постановки пациент-ориентированных расчетов, построенные на основе обработки клинических данных (верхний ряд - пациенты Р, Е; нижний ряд - К, В) |

|
| Рисунок 5.2. Пример расчетной сетки для модели проксимального анастомоза пациента И |
|
| Рисунок 5.3. Линии тока в момент максимального расхода (пациенты Р, И, Е, К, В) |

| |
| Рисунок 5.4. Поле перепада давления в момент максимального расхода (пациенты Р, И, Е, К, В) | |

| |
| Рисунок 5.5. Поля осредненных по времени сдвиговых напряжений (пациенты Р, И, Е, К, В) | |
| |
| Рисунок 5.6. Поля индекса колебаний сдвиговых напряжений (пациенты Р, И, Е, К, В) | |

| |
| Рисунок 5.7. Осредненные в области проксимального анастомоза значения параметров поля сдвиговых напряжений на стенке (пациенты Р, И, Е, К, В) | |
а 
| б 
|
| Рисунок 5.8. Сравнение результатов расчетов течений в области дистального анастомоза пациента О. и в области проксимального анастомоза пациента Е.: а - линии тока в момент максимального расхода, б - осредненные по времени сдвиговые напряжения |