1. Гелий, находящийся в сосуде под подвижным поршнем, изотермически сжимают. Начальное давление газа p0, а его объём V0. Масса газа в сосуде остаётся неизменной. Установите соответствие между физическими величинами, характеризующими газ, и формулами, выражающими их зависимость от объёма V газа. К каждой позиции первого столбца подберите соответствующую позицию из второго столбца.
| ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ | ФОРМУЛЫ |
| А) Давление P(V) | 1. 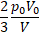
|
| Б) Внутренняя энергия U(V) | 2. 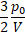
|
3. 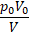
| |
4. 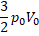
|
Решение: В изотермическом процессе p0V0 = pV; откуда 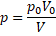 . В этом процессе сохраняется внутренняя энергия. Для одноатомного газа:
. В этом процессе сохраняется внутренняя энергия. Для одноатомного газа:
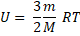
Из уравнения Менделеева-Клапейрона:
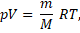
но p0V0 = pV, тогда:
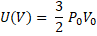
Правильный ответ: А – 3, Б – 4.
2. Чему равна внутренняя энергия 2 молей идеального одноатомного газа при температуре 1270С? R = 8,31Дж/(моль·К).
Решение: Переведём температуру в СИ:
Т = 127 + 273 = 400 К.
Формула для вычисления внутренней энергии одноатомного идеального газа:
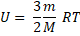
Известно, что число молей 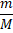 равно двум, подставим численные значения величин в формулу:
равно двум, подставим численные значения величин в формулу:
U = (3/2) · (2 моля) · 8,31 (Дж/моль·К) · 400 К = 9972 Дж.
Ответ: U = 9972 Дж.
Еще один вопрос, который мы сегодня рассмотрим — это необратимость процессов в природе. Можно привести ряд примеров: скажем, яблоко может упасть с яблони, но оно никогда самопроизвольно не залетит обратно на яблоню. Котел, который мы нагреваем с помощью сжигания, дров не может внезапно начать отдавать энергию обратно дровам, а сам начать остужаться. Если вы вытопили печь, то она, несомненно, будет остывать, отдавая свое тепло дому. Не может произойти такого, чтоб вся комната начала остывать, а печка бы снова раскалилась. Если вы уроните стакан, то он вполне может разбиться о пол, но вот самопроизвольно восстановиться из осколков стакан не сможет. Можно продолжать приводить подобные примеры до бесконечности, но все они говорят нам о том, что макроскопические процессы в природе протекают в определенном направлении. В обратном направлении они могут протекать только в случае внешнего воздействия, но такие процессы уже нельзя будет назвать самопроизвольными. Отличной демонстрацией невозможности обратимости процессов может послужить практически любое видео в обратной перемотке. В соответствии с подобными наблюдениями, был сформулирован второй закон термодинамики. Мы используем формулировку Рудольфа Клаузиуса: невозможно перевести тепло от более холодной системы к более горячей при отсутствии других одновременных изменений в обеих системах или в окружающих телах.
Таким образом, второй закон термодинамики указывает направление протекания процессов, что уже говорит о том, что природные процессы необратимы.
Рассмотрим еще один пример, который позволяет статистически обосновать необратимость тепловых процессов.
Как вы знаете, находясь в сосуде газ занимает весь объем сосуда. Если отодвинуть поршень, увеличив объем, то газ, незамедлительно расширится. Но вот сжаться сам по себе он не сможет.
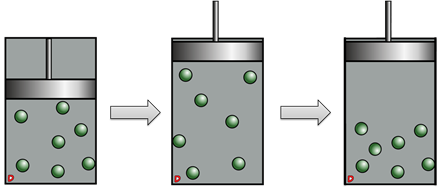
Чтобы газ самопроизвольно сжался нужно, чтобы все его молекулы оказались в одной половинке сосуда. Мы не будем сейчас объяснять, как рассчитывается вероятность такого события, а просто приведем числа:
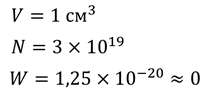
Смело можно сказать, что эта вероятность практически нулевая. Да и без расчетов вы понимаете, что такие события никогда не происходят в реальности. Например, какова вероятность того, что пылинки в вашей комнате полностью покроют одну половину стола, а на другую половину не попадут вообще? Или какая вероятность того, что человек, случайно переставляющий шахматные фигуры, сможет обыграть Гарри Каспарова? Ответ на этот вопрос может быть только один: такие события попросту невероятны.