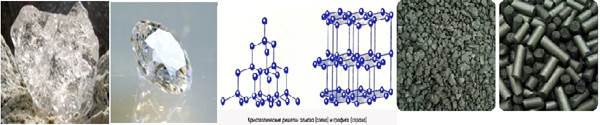
НЕМЕТАЛЛЫ
Из 109 химических элементов 22 неметаллы, расположены в правом верхнем углу ПСХЭ, из них 6 – инертные газы (8A).
Элементы с неметаллическими свойствами находятся в IIIA-VIIA - группах Периодической системы:
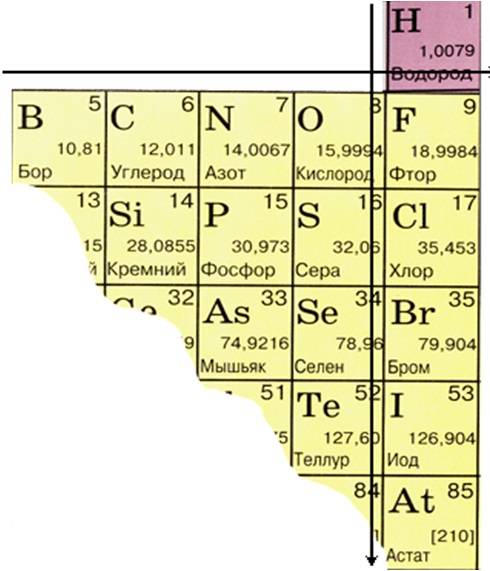
Особенности атомного строения неметаллов:
1. Небольшой атомный радиус
2. На внешнем уровне 4-8 электронов (исключение водород – 1 электрон, гелий – 2 электрона)
3. Располагаются только в главных подгруппах
4. Характерно высокое значение ЭО
5. Степени окисления от -4 до +8
Особенности строения простых веществ
Химические связь ковалентная неполярная или вещества атомарного строения
АТОМАРНОЕ СОСТОЯНИЕ
Инертные или благородные газы не образуют молекул и существуют в атомарном состоянии (не образуют решеток)
He –гелий, Ne-неон, Ar-аргон, Kr-криптон, Xe-ксенон, Rn-радон
АТОМНЫЕ КРИСТАЛЛИЧЕСКИЕ РЕШЁТКИ: алмаз (С) и кремний (Si)
3. МОЛЕКУЛЯРНАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
Многие неметаллы образуют молекулу, состоящую из двух атомов (H2, O2 , N2, F2, Cl2, Br2, I2), при этом образуется очень непрочная связь.
При обычной температуре неметаллы могут быть в разном агрегатном состоянии
1. Газообразные - O2-кислород, H2 - водород, N2- азот, Cl2-хлор, F2-фтор.
2. Жидкие - Br2 -бром
3. Твердые – S –сера, P-фосфор, I2 –йод, C–-алмаз и графит
Многие не проводят электрический ток (кроме графита и кремния).
Не проводят тепло.
В твердом состоянии - хрупкие
Не имеют металлического блеска (кроме иода-I2, графита-C и кремния Si)
Цвет охватывает все цвета спектра: красный-красный фосфор, желтый –сера, зеленый-хлор, фиолетовый –пары иода.
Температура плавления изменяется в огромном интервале: tпл (N2)= -210⁰C, а tпл (Алмаз) =3730⁰С

АЛЛОТРОПИЯ
Способность атомов одного химического элемента образовывать несколько простых веществ называется аллотропией, а эти простые вещества – аллотропными видоизменениями, или модификациями.
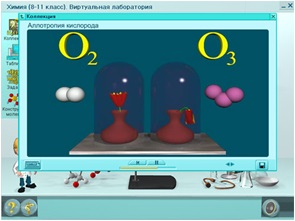
КИСЛОРОД
Кислород образует две аллотропные модификации (причина- строение молекулы)
КИСЛОРОД O₂: Газ без цвета и запаха Входит в состав воздуха (21% по объему). Не ядовит!
ОЗОН O3: Газ бледно-фиолетового цвета с резким запахом свежести.
Обладает бактерицидными свойствами, способен удерживать ультрафиолетовые лучи.
СЕРА
Твердое кристаллическое вещество желтого цвета, нерастворима в воде, водой не смачивается (плавает на поверхности), t кип = 445 °С
Возможные валентности: II, IV, VI. Степени окисления: -2, 0, +4, +6
У серы можно выделить три аллотропных модификации: кристаллическая(ромбическая),моноклинная и пластическая.
Переход из кристаллической в пластическую происходит при нагревании до температуры кипения при последующем быстром охлаждении.

АЗОТ
Азот – газ без цвета и запаха, плохо растворим в воде. Азот является основной частью воздуха (79% по объѐму).
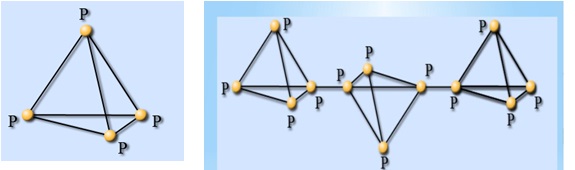
ФОСФОР
Образует семь аллотропных модификаций, причиной является строение кристаллической решётки.
Фосфор белый P₄(молекулярная кристаллическая решётка)
Мягкое, бесцветное вещество. В темноте светится. Ядовит!
Фосфор красный Pn (атомная кристаллическая решётка) аморфное
полимерное вещество(порошок). в темноте не светится, ядовит

УГЛЕРОД
образует две аллотропные формы (причина – строение кристаллической решётки)
Алмаз: Тетраэдрическая кристаллическая решетка
Бесцветные кристаллы. Самое твердое вещество в природе. tпл=3730ºC
Графит: Кристаллическая решетка напоминает соты
Слоистое кристаллическое вещество, жирное на ощупь, непрозрачное,серого цвета.