Агрегатные состояния вещества.
Плавление и отвердевание кристаллических тел
Вы хорошо знаете, что одно и то же вещество может находиться в трёх агрегатных состояниях: в твёрдом, жидком и газообразном. Эти состояния вещества различаются расположением, характером движения и взаимодействия молекул. При некоторых условиях, например при определённых значениях температуры и давления, вещества могут переходить из одного агрегатного состояния в другое. Самым известным таким примером служат вода, лёд и пар.

Лёд Вода Пар
Переходы вещества из одного агрегатного состояния в другое называют агрегатными превращениями.
Многие природные явления обусловлены естественным изменением агрегатных состояний различных веществ. Например, хорошо знакомый вам большой круговорот воды в природе, объясняется изменением агрегатного состояния воды.
Конечно же у вас могут возникнуть вопросы: при каких условиях происходит переход вещества из одного агрегатного состояния в другое? Или как объяснить изменение агрегатного состояния вещества?
Давайте попытаемся найти ответы на эти и другие вопросы. Вы уже знаете, что молекулы одного и того же вещества не меняются с изменением его агрегатного состояния. А меняется их расположение, характер движения и взаимодействия.

Твёрдое тело Жидкость Газ
Вспомним, что в твёрдых телах молекулы плотно прилегают друг к другу и могут только колебаться около своих положений равновесия.
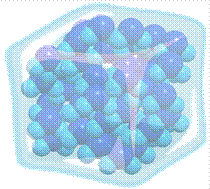
Из-за сильного взаимодействия в твёрдом веществе частиц друг с другом, и отсутствие у них подвижности, приводит к тому, что твёрдые тела сохраняют свою форму и объём.
В жидкостях, молекулы расположены немного дальше друг от друга. Поэтому они совершают беспорядочные колебания и вращения в одном положении, а также могут перемещаться друг относительно друга.

Наличие сил притяжения между молекулами обеспечивает жидкости сохранение объёма, а перемещения — текучесть.
В газах молекулы расположены на значительном расстоянии друг от друга. Поэтому молекула в газе двигается свободно до момента столкновения с другой молекулой или стенкой сосуда, в котором он находится.
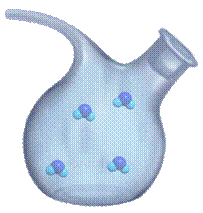
А если газу не мешают стенки сосуда, то его молекулы разлетаются в различных направлениях.
Давайте рассмотрим несколько примеров о том, как люди используют изменение агрегатных состояний веществ в своих целях. Существует такое устройство, как паровая турбина.

Это тепловой двигатель, в котором за счёт разности давлений энергия пара преобразуется в механическую энергию.
Также, чтобы придать ту или иную форму металлическим изделиям, люди сначала приводят металлы к жидкому состоянию, а потом остужают их.

А, например, сжиженный газ используется в холодильных установках.

На прошлых уроках мы с вами говорили о том, что при теплопередаче изменяется внутренняя энергия тела. И чаще всего это связано с изменением его температуры. Но при этом агрегатное состояние вещества остаётся прежним. Однако существуют процессы, при которых внутренняя энергия вещества при получении теплоты увеличивается, а температура остаётся постоянной.
К таким процессам относятся плавление и кристаллизация (отвердевание). Изучим эти процессы с помощью опыта.
Возьмём калориметр, во внутренний сосуд которого положим немного измельчённого льда при температуре минус десять градусов по Цельсию.
Опустим в него термометр и оставим на столе. Будем следить за изменением температуры льда и процессами, которые с ним происходят. Наблюдения показывают, что какое-то время лёд остаётся в твёрдом состоянии, а его температура постепенно повышается.
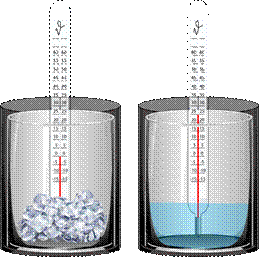
При температуре в 0 оС лёд начинает плавиться, в сосуде появляется вода, но температура льда остаётся неизменной. И она не будет изменяться до тех пор, пока весь лёд не перейдёт в жидкое состояние. Только после этого температура образовавшейся изо льда воды начинает повышаться. И это будет происходить до тех пор, пока она не станет равной комнатной температуре.