Предмет технической термодинамики. Газовые смеси.
№ 1
Первый закон термодинамики есть частный случай:
• Закона сохранения и превращения энергии.
№ 2
В сосуде объемом 0.75 м³ находится 2.5 кг углекислого газа. Удельный объем газа:
• 0.3 м³/кг.
№ 3
В системе находится воздух с избыточным давлением pИЗБ=0.4 МПа. Атмосферное давление pВ=0.1 МПа. Абсолютное давление:
• 0.5 МПа.
№ 4
Температура водяного пара на входе в турбину 525°С. Абсолютная температура пара:
• 798 К.
№ 5
Свойства реального газа будут близки к свойствам идеального газа:
• При высоких температурах.
№ 6
Уравнение состояния для 1 кг идеального газа.
• pv = RT.
№ 7
Величина μR в уравнении состояния идеального газа носит название:
• Универсальной газовой постоянной.
№ 8
На диаграмме p - V изображены линии постоянной температуры - изотермы.
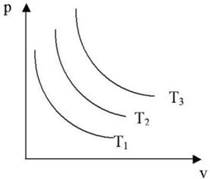
• Т1 < Т2 < Т3.
№ 9
На диаграмме p - Т изображены линии постоянного удельного объема - изохоры.
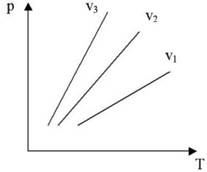
• v1 > v2 > v3.
№ 10
При очень быстром сжатии газа в цилиндре под поршнем параметры газа в разных точках объема различны. Такой термодинамический процесс носит название:
• Неравновесного.
№ 11
По определению, термодинамическая система состоит из рабочего тела и внешней среды, отделенных друг от друга поверхностью. Если эта поверхность не будет пропускать теплоту, то процесс изменения состояния рабочего тела:
• Адиабатный.
№ 12
Прибор для измерения давления носит название:
• Манометра.
№ 13
Уравнение состояния идеального газа.
• pV = mRT.
№ 14
Энтальпия (H) термодинамической системы равна:
• H=U+pV.
№ 15
5 кг газа занимает объем 2 м³. Удельный объем газа:
• 0,4 м³/кг.
№ 16
В каком из процессов теплота, подведенная к газу, больше?
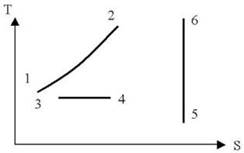
• В процессе 1-2.
№ 17
Площадь под графиком процесса в координатах р-v выражает:
• Работу процесса.
№ 18
Плотность воздуха равна 1,293 кг/м³. Удельный объем воздуха:
• 0,77.
№ 19
Плотность какого газа больше: чистого воздуха, молекулярная масса которого равна 29 условных единиц, или смеси чистого воздуха и водяного пара, молекулярная масса которого равна 18 условных единиц?
• Чистого воздуха.
№ 20
Если условно в объеме, который занимает смесь газов, оставить только один компонент, не изменяя температуры, то давление оставленного компонента будет равно:
• Парциальному давлению.
№ 21
Сухой воздух имеет следующий массовый состав: примерно 23,2% О2 и 76,8% N2. Определить газовую постоянную смеси (Rсм), если RО2=260 Дж/(кг*К) RN2=297 Дж/(кг*К).
• 286,9 Дж/(кг*К).
Первый закон термодинамики. Теплоемкость.
№ 22
При увеличении энтропии (S2 > S1):
• Теплота подводится.
№ 23
Два одинаковых цилиндра заполнены одинаковым газом и отличаются только тем, что в цилиндре А поршень закреплен, а в цилиндре В - уравновешен грузом. Начальные параметры газа (p,V,T) в обоих сосудах одинаковы. К цилиндрам подводится одинаковое количество теплоты.
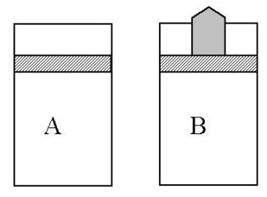
• В цилиндре А температура газа будет выше.
№ 24
Идеальный газ сжимают в изотермическом процессе. Внутренняя энергия газа:
• Не изменится.
№ 25
Уравнение первого закона термодинамики.
• Q=ΔU+L.
№ 26
На диаграмме p - v изображены термодинамические процессы.
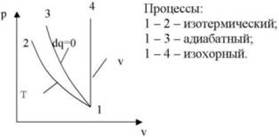
• В изотермическом процессе 1 - 2 теплота отводится от газа.
№ 27
На диаграмме T - s изображены термодинамические процессы.

• В изотермическом процессе 1 - 2 газ совершает работу dl>0.
№ 28
Для изотермического процесса уравнение первого закона термодинамики имеет вид:
• Q=L.
№ 29

• В процессе 3-4 теплота подводится.
№ 30
К газу подводится извне 100 кДж теплоты. Произведенная работа при этом составляет 120 кДж. Если масса газа 0,2 кг, то изменение внутренней энергии газа Δu, кДж/кг:
• -100 кДж/кг.
№ 31
Атмосферное давление 1 бар. Если при постоянной температуре показание манометра уменьшится от р1=17 бар до р2=2 бар, плотность газа в сосуде:
• Уменьшится в 6 раз.
№ 32
Если при неизменном давлении абсолютная температура воздуха увеличится в 2 раза, плотность воздуха:
• Уменьшится в два раза.
№ 33
К газу подводится извне 200 кДж теплоты, изменение внутренней энергии ΔU составляет 20 кДж. Удельная работу, кДж/кг, если количество газа составляет 0,6 кг:
• l=300 кДж/кг.
№ 34
Найти изменение энтальпии 1 кг воздуха, если его температура снизилась от 250°С до 50°С при условии, что теплоемкость не зависит от температуры.
сv=717,5 Дж/ (кг*К).
сp=1004,5 Дж/ (кг*К).
• 200,9 кДж/кг.
№ 35
- изменение внутренней энергии 1 кг воздуха:
• 143,5 кДж/кг.
№ 36
На диаграммах p-v и T-s изображен термодинамический процесс 1 - 2.

• значение теплоемкости газа c < 0.
№ 37
Значения теплоемкостей cp и cv очень мало отличаются друг от друга:
• Для твердых тел.
№ 38
Теплоемкость адиабатного процесса равна нулю.
№ 39
Теплоемкость изотермического процесса бесконечно велика.
№ 40
Формула связи теплоемкостей cv и cp для идеального газа (формула Майера).
• сp-сv=R.
№ 41
Формула для определения средней теплоемкости.
• c=q/(t2-t1).