Следует дифференцировать разные стадии процесса кристаллизации расплавленных металлов, различая образование центров кристаллизации (зачатков) и их рост. Тамман 1898 г указал, что оба явления могут быть охарактеризованы количественно с помощью следующих параметров:
а) числа центров кристаллизации, возникаю за единицу времени в единичном объеме;
б) линейной скорости роста кристаллов, т. е. скорости перемещения грани кристалла, выражаемой в единицах длина/время. По его мнению, подтвержденному многочисленными экспериментами над прозрачными органическими веществами, при развитии зотермического процесса кристаллизации оба параметра остаются неизменными — они для каждого расплава являются функцией одного лишь переохлаждения. Практически линейная скорость кристаллизации может меняться за счет выделения теплоты кристаллизации и вызываемого этим выделением местного повышения температуры.
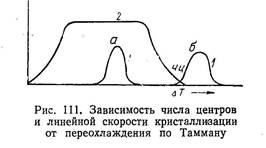
На рис. 111 приведены типичные кривые зависимости числа центров (1) и линейной скорости кристаллизации (2) от переохлаждения. По мере понижения температуры оба параметра вначале растут, а затем, достигнув при определенных переохлаждениях максимальных значений, начинают падать. Однако существует принципиальное различие между кривыми 1 и 2: кривые 1 имеют явно выраженные максимумы при определенных температурах, на кривых же 2 максимальному значению соответствует значительный интервал температур (горизонтальный участок кривой). Ниже мы подробнее остановимся на этом вопросе при изложении современного учения о кристаллизации.
Если температура максимума на кривой числа центров лежит вне области высоких скоростей роста (кривая б рис. 111), то жидкость способна долго не кристаллизоваться при больших переохлаждениях, если же максимум на кривой числа центров лежит в области максимальных значений линейной скорости (кривая а рис. 111), то сильно переохладить жидкость невозможно.
В некоторых случаях кривая числа центров, при малых переохлаждениях почти сливающаяся с осью абсцисс, начиная с некоторого определенного переохлаждения, резко поднимается вверх. Вещества, характеризующиеся такой кривой числа центров, даже при длительных выдержках не кристаллизуются при температурах выше точки начала подъема кривой (эту точку называют границей метастабильности). Однако после перехода через границу метастабильности начинается интенсивно идущий процесс кристаллизации.
На основании представлений о числе центров и скорости роста кристаллов были выведены формулы, с помощью которых можно, зная число центров кристаллизации и линейную скорость роста, в простейших случаях однозначно предсказать кинетику процесса, его длительность и среднюю величину зерна. Точно также, измерив число кристаллов, приходящихся на единицу объема, и определив длительность процесса кристаллизации, можно вычислить кристаллизационные параметры.
К сожалению, на практике такие простейшие случаи по причинам, о которых речь будет идти ниже, при кристаллизации расплавленных металлов не реализуются, и поэтому выводимые ниже формулы при анализе процессов кристаллизации из жидкой фазы могут применяться лишь для получения качественных характеристик.
Представления о кристаллизационных параметрах были применены многочисленными исследователями не только к анализу процессов образования кристаллов из жидкой фазы, но и к анализу процессов, протекающих в твердой фазе (рекристаллизация, фазовые превращения). В самой общей форме проблема была решена Н. А. Колмогоровым, путем применения методов теории вероятностей.
Наиболее совершенен расчет, проведенный Н. А. Колмогоровым и использованный и конкретизированный И. Л. Миркиным. Ниже приведен этот расчет применительно к простейшему случаю, когда скорость зарождения центров и линейная скорость роста кристаллов остаются все время постоянными, причем кристаллы растут с одной и той же скоростью по всем направлениям, сохраняя до момента соприкосновения с другими кристаллами сферическую форму.
Колмогоров определяет вероятность P(t) того, что какая-либо наудачу выбранная точка объема vo, заполненного кристаллизующимся веществом, по прошествии t сек. от начала процесса кристаллизации попадает внутрь закристаллизовавшейся массы. Если начальный объем маточной фазы V o намного больше размеров отдельных кристаллитов, то закристаллизовавшийся за t сек. объем V (t) равен произведению первоначального объема V0 на вероятность Р (t):
V(t) = P(t)· V0. (124)
В начальный момент времени при t = 0 также и V (t) =0.
Для того, чтобы определить, по какому закону растет объем закристаллизовавшейся массы V(t), рассмотрим, что происходит за малый промежуток.времени D t между t и t + D t.
Прежде всего, в закристаллизовавшемся объеме V o— V возникают новые центры кристаллизации. Вероятность образования одного центра кристаллизации в некоторой части незакристаллизовавшегося объема V' £ V o— V за промежуток времени между t и t + D t равна nV'Dt, где п — вероятность образования центра кристаллизации в одном кубическом сантиметре незакристаллизовавшегося объема за одну секунду, равная числу центров кристаллизации, возникающих за одну секунду в каждом кубическом сантиметре. Как вновь возникшие за D t сек. центры кристаллизации, так и кристаллы, возникшие ранее, растут с постоянной линейной скоростью с. Рассмотрим произвольную точку О, находящуюся на расстоянии, превышающем ct, от краев объема V o. Эта точка к моменту t окажется внутри закристаллизовавшейся массы, если в какой-то момент времени t i< ct в какой-либо точке О', находящейся на расстоянии r£ c (t — ti), возникает центр кристаллизации. Если задаться определенным моментом ti, то объем V'(ti), внутри которого в точке О' должен возникнуть центр кристаллизации для того, чтобы и точка О оказалась внутри закристаллизовавшейся массы, определится так:

Вероятность Pi того, что за промежуток времени D t в обьеме, равном V' (ti), образуется центр кристаллизации, равна:
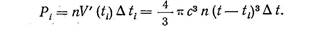 (1 26).
(1 26).
Основное кинетическое уравнение можно вывести, определив вероятность того», что точка О окажется вне закристаллизовавшегося за t сек. объема.
Вероятность qt того, что в объеме V'(tt) за D t сек. не возникнет ни одного центра кристаллизации, равна, очевидно:
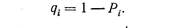
Разобьем промежуток времени t, протекший от начала кристаллизации до данного момента, на s равных между собой малых промежутков D t = t/s. Для того, чтобы точка О оказалась к моменту времени t вне закристаллизовавшегося объема, необходимо, чтобы ни в один из этих малых промежутков времени не зародился такой центр кристаллизации, который за время до момента t мог бы дорасти до точки О. Поскольку вероятность совпадения нескольких независимых фактов равна произведению вероятностей всех этих фактов, вероятность q(t) того, что точка О останется до момента t вне закристаллизовавшегося объема, выразится так:
(128)

Для очень -малого промежутка времениD t вероятность Pt образования центра кристаллизации в объеме Vi также чрезвычайно мала, поэтому, разлагая в степенной ряд выражение  и ограничиваясь только величинами первого порядка малости (т. е. первыми двумя членами ряда), можно написать:
и ограничиваясь только величинами первого порядка малости (т. е. первыми двумя членами ряда), можно написать:
e-pi = 1-Pi (129)
причем погрешность, вносимая в расчет использованием этого уравнения, будет стремиться к нулю при стремлении к нулю промежутка времени D t. В соответствии с этим уравнение (128) можно преобразовать так:
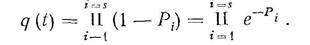
(130)
Логарифмируя уравнение1 (130) и используя (126), получим;
 (131)
(131)
и переходя от малых конечных промежутков времени D t к бесконечно малым промежуткам dt
 (132)
(132)
Отсюда, учитывая уравнения (124) и (127), найдем окончательное выражение для объема V(t), закристаллизовавшегося за t сек:
 (133)
(133)
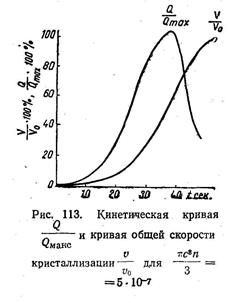
На рис. 112 приведены кинетические кривые, построенные И. Л. Миркиным для различных значений параметра с 3n: Как видно из этого графика, закристаллизовавшийся объем сперва растет очень медленно (малое число растущих кристалликов и малая поверхность каждого из них), затем рост резко ускоряется, кривая круто поднимается вверх, и, наконец, когда незакристаллизовавшийся объем уменьшается до 10—20% от первоначального, кривая вновь делается пологой. Последнее изменение хода кривой вызвано тем, что растущие кристаллиты соприкатсаютея между собой и на поверхности соприкосновения рост их прекращается.
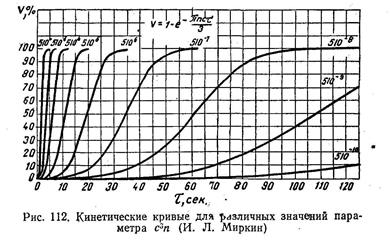
Необходимо отметить, что формула (133), как и формулы, выведенные ранее другими авторами, является приближенной. Она была бы точна лишь в том случае, если бы первоначальный объем был бесконечно велик. Действительно, при конечном значении первоначального объема Vo он должен был бы полностью закристаллизоваться за конечный промежуток времени to = l / c, протекший с момента образования первого центра кристаллизации (l —максимальное расстояние между двумя точками, лежащими на поверхности, ограничивающей кристаллизующуюся массу), между тем как по формуле (133) процесс кристаллизации длится бесконечно долго, поскольку он заканчивается при:

Формула (133) делается заметно неточной, когда незакристаллизовавшийся объем делается очень малым (меньше 1—10% от V0), притом неточность ее проявляется тем сильнее, чем меньше кристаллитов содержит закристаллизовавшееся тело, т. е. чем крупнее зерно.
По формуле (133) можно вычислить промежуток времени, в течение которого кристаллизуется любая определенная доля кристаллизующейся массы 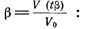

при b = 0,99 (И. Л. Маркин предлагает считать, что при этом кристаллизация практически заканчивается):

Число кристаллов N (t), образовавшихся за промежуток времени t, можно определить по формуле:


При анализе процесса -кристаллизации часто существенную роль играет величина Q (t) = 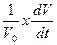 , которую можно назвать общей (объемной) скоростью кристаллизации (превращения). Общая (объемная) скорость кристаллизации равна объему, кристаллизующемуся в 1 см3 металла за одну секунду (точнее — пределу отношения объема, закристаллизовавшегося за бесконечно малый промежуток времени, к величине этого промежутка).
, которую можно назвать общей (объемной) скоростью кристаллизации (превращения). Общая (объемная) скорость кристаллизации равна объему, кристаллизующемуся в 1 см3 металла за одну секунду (точнее — пределу отношения объема, закристаллизовавшегося за бесконечно малый промежуток времени, к величине этого промежутка).
В рассматриваемом нами случае «шаровой» кристаллизации с постоянным числом центров кристаллизации п и постоянной.линейной скоростью с, очевидно
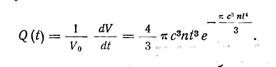 (138)
(138)
Общая скорость кристаллизации может быть определена графически, как тангенс угла наклона касательной к кинетической кривой по отношению к оси абсцисс. Поскольку каждая кинетическая кривая имеет точку перегиба (см. рис. 112), общая скорость кристаллизации, сперва очень малая, растет, достигая максимума в точке перегиба кинетической кривой, и далее падает (рис. 11З). Момент времени t макс, отвечающий максимальному значению общей скорости превращения, определяется так:
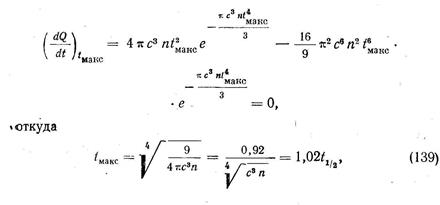
т. е. общая скорость кристаллизации достигает максимума почти точно тогда, когда закристаллизованный объем достигает половины первоначального.
Следует отметить еще одно обстоятельство. Как видно из того же рис. 113, закристаллизовавшаяся масса в начале процесса кристаллизации бывает очень мала и очень медленно увеличивается. Когда изучается превращение в твердом металле, являющемся непрозрачным телом, эта начальная стадия кристаллизации улавливается с большим трудом, а иногда и не удается вовсе обнаружить, что процесс уже начался. Это обстоятельство-приводит иногда к предположению, что процесс превращения при изотермической выдержке начинается не сразу, а по прошествии некоторого промежутка времени, называемого «инкубационным периодом». В большинстве случаев термин «инкубационный период» следует понимать условно: на самом деле и в этот период обычно возникают и растут центры кристаллизации, но закристаллизовавшаяся масса очень мала, и новые кристаллы можно обнаружить лишь в результате большого числа опытов (таков именно смысл по И. Л. Миркину так называемого «инкубационного» периода при эвтектоидном распаде аустенита). Лишь применительно к некоторым превращениям в твердом состоянии, как будет показано ниже, и сейчас имеются основания предполагать существование истинного «инкубационного» периода, во время которого практически кристаллы новой фазы не образуются (такой истинный инкубационный период, возможно, имеет место в начальной стадии распада некоторых пересыщенных твердых растворов).
Как указывалось выше, кинетические расчеты всеми исследователями проводились применительно к процессам перекристаллизации в твердом состоянии. При кристаллизации жидкости процесс роста кристаллов усложняется и тормозится из-за выделения скрытой теплоты плавления, гораздо большей, чем теплота большинства превращений b твердом состоянии, и из-за образования поверхностных пленок. Поэтому линейная скорость роста кристалла в жидкой фазе с течением времени убывает.
Определить закономерности, которым подчиняется изменение линейной скорости роста кристалла в жидкой фазе, невозможно, гак как указанные факторы действуют весьма неопределенно; можно лишь утверждать, что в большинстве случаев скорость эта с течением времени убывает.
И. Л. Миркин, воспользовавшись общей схемой расчета, предложенной Н, А. Колмогоровым для шаровой формы роста, и предположив, что радиус кристалла r растет пропорционально квадратному корню из времени:
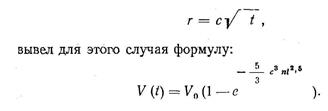
А. А. Бочвар подчеркивает, что процесс кристаллизации реального металлического слитка вообще не может быть описан сколько-нибудь точно с помощью кинетических уравнений из-за крайней его сложности. Кроме указанных выше усложняющих факторов, А. А. Бочвар особое внимание уделяет дендритному характеру процесса кристаллизации, подмеченному и описанному впервые еще Д. К. Черновым (он называл дендриты «разрывными кристаллами»). Как указывают Д. К. Чернов и А. А. Бочвар, особенно сильно выявляется дендритная кристаллизация при затвердевании таких сплавов, у которых велико расстояние между линиями (или поверхностями) солидуса и ликвидуса на соответствующих диаграммах состояния (к их числу относятся многие технически важные сплавы). Законы роста дендритов и заполнения междендритных полостей (особенно в условиях движения жидкости в процессе заполнения изложницы, когда отдельные ветви дендритов отламываются и ставятся своеобразными центрами кристаллизации), как справедливо указывает А. А. Бочвар, настолько сложны и зависят от такого большого количества факторов, что дать их математическую характеристику не представляется возможным. К этому следует прибавить, что существеннейшим не поддающимся учету фактором является наличие в расплавленном металле нерасплавившихся частиц тугоплавких примесей, которые, как будет показано ниже, играют роль зародышей кристаллизации.
И все же понятие о кристаллизационных 'параметрах позволяет ('по крайней мере качественно) разобраться во многих существенных особенностях процессов кристаллизации расплавленных металлов