Примерный вариант диктанта
Написать структурную формулу аминокислот(ы), дать ей систематическое название и обозначение:
1. а) две основные; б) две кислые;
2. а) одну гетероциклическую; б) одну ароматическую;
3. а) с рI = 7; б) с рI >7;
4. а) амид аминокислоты; б) дающую реакцию с FeCl3;
5. а) две, дающих ксантопротеиновую реакцию; б) две серусодержащих;
6. а) с гидрофобным радикалом; б) иминокислоту;
7. а) реагирующую с нингидрином; б) дающую биуретовую реакцию;
8. а) содержащую ОН-группу; б) оптически неактивную;
9. а) две, реагирующих с 2 моль NaOH; б) две, реагирующих с 2 моль HCl;
10. три незаменимых аминокислоты.
4. Заполнить таблицу (кроме графы наблюдения) по лабораторной работе «Качественные реакции аминокислот» Отчеты принимаются в день проведения занятия!!
| Название опыта | |
| Схема реакции | |
| Наблюдения |
Опыт 1. Амфотерные свойства α-аминокислот.
А) На полоску универсальной индикаторной бумаги нанесите стеклянной палочкой 1 каплю 1%-ного раствора аланина. Изменилась ли окраска индикаторной бумаги?
Б) В две пробирки поместите по 3 капли 1%-ного водного раствора аланина. В первую пробирку добавьте по каплям 0,1%-ный раствор соляной кислоты, подкрашенной индикатором конго в синий цвет, а во вторую пробирку – 0,1%-ный раствор NaOH, подкрашенный фенолфталеином. Какие изменения наблюдаются в каждом случае?
Опыт 2. Образование оснований Шиффа.
Возьмите две пробирки. В первую пробирку поместите 5 капель 1%-ного раствора глицина и 1 каплю раствора индикатора метилового красного. Раствор приобретает желтую окраску. Во вторую пробирку поместите 5 капель формалина и 1 каплю раствора индикатора метилового красного. Раствор во второй пробирке, имеющей красную окраску, осторожно нейтрализуйте добавлением 10%-ного раствора NaOH до появления желтого окрашивания. Содержимое двух пробирок перемешайте. Отметьте появление красного окрашивания.
Опыт 4. Дезаминирование α-аминокислот.
Смешайте в пробирке 0,5 мл 1%-ного раствора глицина и равный объем 5%-ного раствора нитрита натрия. Добавьте 2 капли концентрированной соляной кислоты. Смесь взболтайте. Наблюдается ли выделение пузырьков газа?
Опыт 5. Цветные реакции α-аминокислот.
А) Нингидриновая реакция.
В пробирку поместите 5 капель 1%-ного раствора глицина и 2 капли 0,1%-ного раствора нингидрина. Содержимое пробирки встряхните и нагрейте. Какое окрашивание приобретает раствор?
Б) Ксантопротеиновая реакция.
В пробирку поместите 5 капель 1%-ного раствора тирозина и добавьте 3 капли концентрированной азотной кислоты, прокипятите. Отметьте появление окрашивания. Пробирку осторожно охладите и по каплям добавьте 1-2 мл концентрированного раствора аммиака. Что происходит с окраской раствора?
В) Реакция Фоля (ДЕМОНСТРАЦИОННО).
В пробирку поместите 5 капель 1%-ного раствора цистеина и добавьте 3 капли 10%-ного раствора NaOH. Содержимое пробирки нагрейте до кипения и затем добавьте 3 капли раствора ацетата свинца (II). Отметьте окраску образующегося осадка.
Г) Биуретовая реакция.
В пробирку поместите 5 капель 1%-ного раствора глицина и добавьте равный объем 10%-ного NaOH, а затем 2-3 капли 25%-ного раствора сульфата меди (II). Как окрашивается раствор?
Д) Реакция с хлоридом железа (III).
К небольшому количеству твердого аланина добавьте 1 мл 3%-ного раствора FeCl3. Возникшая красная окраска доказывает присутствие a-аминокислоты. Добавьте 1 мл 10%-ной соляной кислоты. Что происходит с окраской раствора?
5. Разобрать тестовые задания по темам:
АМИНОКИСЛОТЫ
1. Имеет оптические изомеры:
а) глицин; б) аланин; в) β–аминопропионовая кислота; г) β–аминомасляная кислота;
д) γ–аминомасляная кислота.
2. Число существующих аминопропионовых кислот равно:
а) одному; б) двум; в) трем; г) четырем; д) пяти.
3. Число оптических изомеров треонина равно:
а) ни одному; б) одному; в) двум; г) четырем; д) пяти.
4. Нейтральной аминокислотой является:
а) валин; б) аргинин; в) лизин; г) аспарагиновая кислота; д) изолейцин.
5. Моноаминодикарбоновой кислотой является:
а) аспарагиновая кислота; б) цистеин; в) глутаминовая кислота; г) фенилаланин;
д) цистеин.
6. Диаминомонокарбоновой кислотой является:
а) пролин; б) лизин; в) глутаминовая кислота; г) тирозин; д) аргинин.
7. Относится к основным аминокислотам соединение:
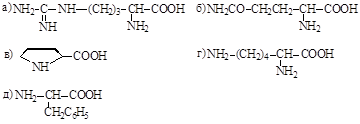
8. Серусодержащей аминокислотой является:
а) треонин; б) триптофан; в) серин; г) цистеин; д) метионин.
9. Аспарагиновая кислота в щелочном растворе существует в преобладающей форме:
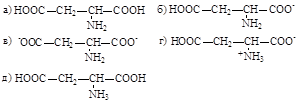
10. Аминокислоту (или аминокислоты) можно получить при гидролизе:
а) глицилфенилаланина; б) метилглицината; в) белка; г) этилбензоата;
д) амида карбоновой кислоты.
11. Тирозин взаимодействует с:
а) HNO2; б) HNO3; в) NaOH; г) FeCl3; д) СН2=СН2.
12. Укажите формулу α–фенил-β-аминопропионовой кислоты:
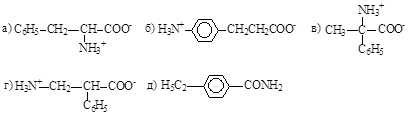
13. Природная аминокислота, реагирующая с двойным количеством щелочи, это:
а) серин; б) треонин; в) тирозин; г) глутаминовая кислота; д) фенилаланин.
14. Заменимой аминокислотой является:
а) глутамин; б) лейцин; в) треонин; г) глицин; д) изолейцин.
15. Полунезаменимой аминокислотой является:
а) гистидин; б) валин; в) фенилаланин; г) метионин; д) лизин.
16. Абсолютно незаменимой аминокислотой является:
а) лизин; б) триптофан; в) аспарагин; г) метионин; д) серин.
17. Выберите циклическую аминокислоту:
а) валин; б) метионин; в) пролин; г) фенилаланин; д) глицин.
18. Гетероцикл содержит аминокислота:
а) тирозин; б) аргинин; в) глицин; г) триптофан; д) гистидин.
19. Выберите иминокислоту, входящую в состав белков:
а) аспарагин; б) серин; в) пролин; г) глутаминовая кислота; д) фенилаланин.
20. Выберите ароматическую аминокислоту, входящую в состав белков:
а) аспарагин; б) гистидин; в) метионин; г) пролин; д) тирозин.
21. Глутаминовая кислота в нейтральной среде имеет суммарный заряд равный:
а) 0; б) +1; в) -1; г) +2; д) -2.
22. Аспарагиновая кислота в сильно щелочной среде имеет суммарный заряд равный:
а) 0; б) +1; в) -2; г) +2; д) -1.
23. Глутаминовая кислота в сильно кислой среде имеет суммарный заряд равный:
а) 0; б) +1; в) -2; г) +2; д) -1.
24. Лизин в сильно кислой среде имеет суммарный заряд равный:
а) 0; б) +1; в) -2; г) +2; д) -1.
25. Выберите аминокислоту, заряженную положительно при значениях рН=7:
а) аланин; б) метионин; в) глутаминовая кислота; г) лизин; д) аргинин.
26. Выберите аминокислоту, заряженную отрицательно при значениях рН=7:
а) аспарагиновая кислота; б) глутамин; в) гистидин; г) аланин; д) глутаминовая кислота.
27. Дисульфидные связи в белках образуют остатки:
а) тирозина; б) цистеина; в) метионина; г) лизина; д) лизина.
28. Продуктами декарбоксилирования α-аминокислот являются:
а) СО2 и β-аланин; б) СО2 и кетокислоты; в) СО2 и оксикислоты;
г) СО2 и биогенные амины; д) СО2 и карбоновые кислоты.
29. Гистамин образуется в клетках организма в результате:
а) дезаминирования гистидина; б) декарбоксилирования гистидина;
в) не образуется, т.к. это незаменимая аминокислота; г) сопряженных с биосинтезом пуринов реакции;
д) взаимодействия двух молекул гистидина.
30. Аланин при взаимодействии с азотистой кислотой образует:
а) акриловую кислоту; б) пропионовую кислоту; в) пировиноградную кислоту;
г) молочную кислоту; д) β-аминопропионовую кислоту.
31. Аспарагиновая кислота с азотистой кислотой образует:
а) малеиновую кислоту; б) фумаровую кислоту; в) яблочную кислоту;
г) янтарную кислоту; д) глутаминовую кислоту.
32. Образуется при декарбоксилировании гистидина:
а) проламин; б) триптамин; в) гистамин; г) серотонин; д) аргинин.
33. Образуется при декарбоксилировании триптофана:
а) проламин; б) триптамин; в) гистамин; г) серотонин; д) адреналин.
34. Установите структуру соединения состава С3Н7NO2, образующего при нагревании диалкилзамещенный дикетопиперазин:
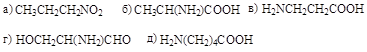
35. Дикетопиперазин образует природная аминокислота:
а) 3-аминопентановая; б) 3-амино-2-гидроксипропановая;
в) 2-(метиламино)бензойная; г) 2-амино-3-гидроксипропановая;
д) 4-аминогексановая.
36. Укажите реакцию, лежащую в основе количественного определения α-амино-кислот по методу Ван-Слайка:
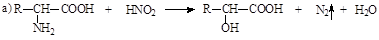
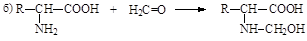
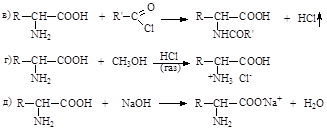
37. Укажите газообразный продукт взаимодействия α–аминокислоты с азотистой кислотой:
а) NH3; б) N2; в) NO; г) NO2; д) N2O.
38. Выберите из колонки 2 те аминокислоты, которые при рН=6.0 будут двигаться в направлении, указанном в 1 колонке:
Колонка 1: 1) к аноду; 2) к катоду.
Колонка 2: а) аргинин рI=10.8; б) валин pI=6.0; в) аланин pI=6.0;
г) глицин pI= 6.0; д) глутаминовая кислота pI= 3,2.
39. Удаление аминогруппы происходит в результате реакции:
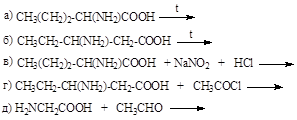
40. Выберите из колонки 2 боковые радикалы, соответствующие аминокислотам из 1 колонки:
Колонка 1: 1) лейцин; 2) изолейцин.
Колонка 2: а) (CH3)2CH-CH2- б) (CH3)2CH-
в) CH3CH2CH(CH3)- г) H2N-(CH2)4- д) CH3-.
41. Выберите из колонки 2 название аминокислоты, образующейся при гидролизе альдимина из 1 колонки:
Колонка 1:
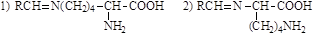
Колонка 2: а) аргинин; б) глутамин; в) аспарагин; г) лейцин; д) лизин.
42. Выберите из колонки 2 соединения, которые образуются в результате дезаминирования в приведенных в колонке 1 условиях:
Колонка 1: 1) дезаминирование α–аланина под действием азотистой кислоты;
2) дезаминирование β–аланина путем нагревания.
Колонка 2:
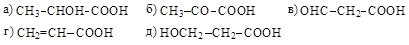
43. Декарбоксилирование глутаминовой кислоты приводит к образованию:
а) 3-аминобутановой кислоты; б) 4-аминобутановой кислоты;
в) 2-аминобутановой кислоты; г) 3-аминопропановой кислоты; д) 2-аминопропановой кислоты.
44. Название треонина по международной номенклатуре IUPAC:
а) 2-амино-3(3’-индолил)пропановая кислота; б) 2-амино-3-гидроксибутановая кислота;
в) 2-аминоэтановая кислота; г) 2-амино-4-метилпентановая кислота;
д) 3-амино-2-гидроксибутановая кислота.
45. Название глутаминовой кислоты по международной номенклатуре IUPAC:
а) 2-амино-3(3’-индолил)пропановая кислота; б) 2-амино-3-гидроксибутановая кислота;
в) 2-аминопентандиовая кислота; г) 2-амино-4-метилпентановая кислота;
д) 2-аминобутандиовая кислота.
46. Название лизина по международной номенклатуре IUPAC:
а) 2-амино-3-метоксипропановая кислота; б) 2,6-диаминогексановая кислота;
в) 2-аминобутановая кислота; г) 2-амино-3-гидроксипропановая кислота;
д) 2-амино-3-фенилпропановая кислота.
47. Валин изображен в соответствии с правилами написания проекционных формул Фишера:
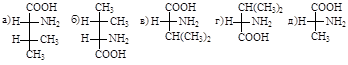
48. Природной аминокислоте соответствует проекционная формула:
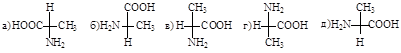
49. Все аминокислоты в составе белков человека, кроме глицина:
а) правовращающие; б) имеют Д-конфигурацию;
в) оптически неактивны; г) имеют L-конфигурацию; д) сладкие.
50. Аминокислоты, не синтезируемые в организме, называются ……
51. Процесс удаление аминогруппы от аминокислоты, называется …..
52. Процесс отщепления карбоксильной группы от аминокислоты в виде СО2, называется ……..
ПЕПТИДЫИ БЕЛКИ
1. Аминокислоты образуют пептиды в процессе реакции:
а) полимеризации; б) поликонденсации; в) дегидрогенизации;
г) этерификации; д) конденсации.
2. Сколько пептидных групп в трипептиде:
а) одна; б) две; в) три; г) четыре; д) пяти.
3. Амидную связь содержат:
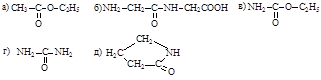
4. Выберите правильное название для трипептида:
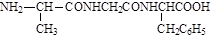
а) аланинглицинфенилаланин; б) аланилглицилфенилаланин;
в) аланилглицилфенилаланил; г) фенилаланилглицилаланин; д) метилглицилглицилфенилаланин.
5. Определите молекулярную формулу трипептида, образованного остатками только одной аминокислоты – глицина:
а) C6H15N3O6; б) C6H13N3O5; в) C6H11N3O4; г) C6H9N3O3; д) C6H7N3O2.
6. Выберите верные утверждения относительно строения и свойств пептидной группы:
а) все атомы находятся в состоянии sp2-гибридизации;
б) пептидная связь гидролизуется в щелочной и кислой средах;
в) вращение вокруг связи С-N затруднено;
г) представляет собой трехцентровую р,π-сопряженную систему;
д) связь С=О способна к реакциям нуклеофильного присоединения.
7. Первичная структура белка формируется за счет связей:
а) водородных; б) сложноэфирных; в) пептидных; г) ионных; д) дисульфидных.
8. Вторичная структура белка обусловлена связью:
а) ионной; б) водородной; в) ковалентной неполярной; г) дисульфидных; д) ковалентной полярной.
9. Третичная структура белка обусловлена:
а) водородными связями между функциональными группами;
б) гидрофобным взаимодействием между углеводородными радикалами;
в) дисульфидной связью между цистеиновыми остатками;
г) пептидной связью;
д) ионным взаимодействием между функциональными группами.
10. Выберите свойства, характерные для всех белков:
а) растворимость и свертывание; б) гидролиз и растворимость в солях;
в) амфотерность и денатурация; г) денатурация и гидролиз;
д) элетропроводность и изменение окраски лакмуса.
11. Концентрированная азотная кислот окрашивает белок в … цвет:
а) синий; б) зеленый; в) желтый; г) фиолетовый; д) красный.
12. При денатурации белка разрушаются связи:
а) водородные; б) дисульфидные; в) ионные; г) пептидные; д) гидрофобные.
13. Инсулин представляет собой:
а) аминокислоту; б) белок; в) фосфолипид; г) фермент; д) полисахарид.
14. Структура белка, представляющая собой последовательность аминокислотных остатков в полипептидной цепи, называется:
а) первичной; б) вторичной; в) третичной; г) четвертичной; д) полипептидной.
15. Трипептид, обнаруживаемый качественной реакцией с ионом Pb+2:
а) Глу-Цис-Тир; б) Мет-Лиз-Лей; в) Илей-Асп-Тир; г) Лиз-Глу-Ала; д) Про-Арг-Гис.
16. Относится к белкам:
а) пенициллин; б) гемоглобин; в) инсулин; г) рибонуклеаза; д) адреналин.
17. В состав антибиотика грамицидина С входят:
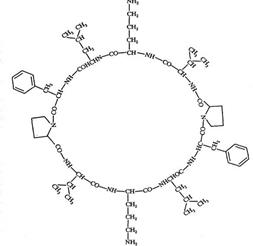
а) пролин; б) валин; в) лизин; г) орнитин; д) изолейцин.
18. Максимальное количество КОН, реагирующее с 1 молем дипептида Гли-Глу, равно:
а) один моль; б) два моль; в) три моль; г) четыре моль; д) пептиды не реагируют со щелочами.
19. Три аминокислоты (по 1 моль) могут образовать …. Разных трипептидов:
а) три; б) шесть; в) один; г) 16; д) девять.
20. Высокомолекулярные азотсодержащие биополимеры, состоящие из аминокислотных остатков, связанных амидными связями, называются …….
21. Любое негидролитическое нарушение уникальной структуры белка, связанное с потерей им физических, биологических и других нативных свойств, называется ……
22. Пространственное строение полипептидной цепи, обусловленное водородными связями, называется ………
23. Последовательность аминокислотных остатков, соединенных пептидными (амидными) связями, называется ……..
24. Пространственное расположение полипептидной цепи, включающей элементы той или иной вторичной структуры, обусловленное водородными, ионными, гидрофобными, дисульфидными связями, называется …….