Лабораторная работа № 3
Определение летучего и связанного аммиака в надсмольной воде коксохимического производства формальдегидным методом
Сущность метода
Метод определения аммиака, содержащегося в надсмольной воде, основан на реакции его количественного взаимодействия с формальдегидом с образованием гексаметилентетрамина:
6 НСОН + 2 (NH4)2SO4 = (CH2)6N4 + 2 H2SO4 + 6 H2O
Путем титрования определяют количество образовавшейся при этом серной кислоты и эквивалентное ей количество азота, содержащееся в надсмольной воде. Реакцию проводят в нейтральной среде.
Мешающие влияния
Определению мешают сероводород, циановодород (синильная кислота) и угольная кислота. Устраняют мешающее влияние этих соединений кипячением пробы с раствором серной кислоты.
Приборы и лабораторная посуда
Конические колбы (ГОСТ 25336-82Е) вместимостью 250 мл
Посуда мерная стеклянная лабораторная (ГОСТ 1770-74Е и ГОСТ 20292-74Е*), вместимостью, мл:
Цилиндры измерительные – 10, 100;
Бюретки - 25;
Пипетки (без делений) – 10;
Пипетки (с делениями) – 5, 10.
Капельница стеклянная (ГОСТ 25336-82Е), вместимостью 50 мл.
Электрическая плитка c закрытой спиралью (ГОСТ 14919-83Е).
Реактивы и материалы
Серная кислота, 1 н.(0,1 н.) раствор;
Едкий натр (не содержащий углекислоты), 1 н. (0,1 н.) раствор;
Формалин 40%-ный, нейтрализованный по фенолфталеину;
Метилоранж (1:1000);
Фенолфталеин (1 г в 100 мл спирта).
Ход определения
В коническую колбу объемом 250 мл наливают 25 мл дистиллированной воды, далее пипеткой отбирают 10 мл анализируемой пробы надсмольной воды и помещают ее в эту колбу, куда прибавляют 3-4 капли индикатора метилоранжа.
Затем из бюретки добавляют 15 мл 0,1 н. раствора серной кислоты до розоватого окрашивания. Если после добавления 15 мл серной кислоты розового окрашивания не произошло, количество кислоты увеличивают до 20 мл или более, пока не произойдет розовое окрашивание (V1 - объем добавленной серной кислоты). Содержимое колбы тщательно перемешивают. При этом происходит нейтрализация пробы и полное связывание летучего аммиака серной кислотой с образованием сульфата аммония.
Исследуемую пробу кипятят 10 минут для удаления сероводорода и других кислых газов, затем охлаждают и оттитровывают избыток 0,1 н. кислоты раствором едкого натра в присутствии одной капли метилоранжа до желтого окрашивания, фиксируют объем NaOH, пошедший на титрование - V2. (Разность объемов (V1 – V2) = V3 (мл) характеризующую общую щелочность воды, включая летучий аммиак, используют для расчета содержания летучего аммиака).
Далее к оттитрованной пробе прибавляют 5 мл 40% (по массе) формалина, предварительно нейтрализованного 1÷10 н. раствором NaOH в присутствии индикатора фенолфталеина до слабо розового окрашивания. Смесь пробы и формалина перемешивают 1 минуту и выдерживают в покое 5 мин.
Затем к исследуемой смеси добавляют 5-7 капель индикатора фенолфталеина и титруют ее 0,1 н. раствором NaOH до появления первого розового окрашивания. В конце титрование ведут медленно, прибавляя щелочь по каплям, так как реакция образования гексаметилентетрамина замедляется. Обьем NaOH, пошедший на заключительное титрование – V4 мл.
Расчет
1. Содержание летучего аммиака в исследуемой воде (х, г/л) вычисляют по формуле:
Х = 
0,001703 – количество NH3, соответствующее 1 мл 0,1 н. раствора серной кислоты;
V1 – объем 0,1 н. раствора кислоты, прилитой к пробе, мл;
V2 – объём 0,1 н. раствора щелочи, затраченный на титрование избытка кислоты, мл;
К – поправочный коэффициент к 0,1 н. раствору щелочи;
Vпр – объем воды, взятой на анализ, мл.
Для Vпр = 10 мл и К = 1 формула принимает следующий вид:
Х = 0,1703 × V3
2. Содержание общего аммиака в исследуемой воде (х, г/л) вычисляют по формуле:
Х = 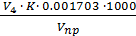 , где:
, где:
0,001703 – количество NH3, соответствующее 1 мл 0,1 н. раствора серной кислоты;
V4 – объём 0,1 н. раствора щелочи, пошедшей на титрование образовавшейся кислоты, мл;
К – поправочный коэффициент к 0,1 н. раствору щелочи;
Vпр – объем надсмольной воды, взятой на анализ, мл.
Для Vпр = 10 мл и К = 1 формула принимает следующий вид:
Х = 0,1703 × V4
Примечание
Если (V1 – V2) = V3 меньше V4, то V3 характеризует содержание аммиака летучего.
NH3 летучий = 0,1703 × V3 , г/л
NH3 связанный = NH3 общий - NH3 летучий, г/л
Если V3 > V4, то в исследуемой надсмольной воде содержится свободная щелочь и связанный аммиак полностью отсутствует. В этом случае летучий аммиак равен общему аммиаку:
NH3 летучий = NH3 общий = 0,1703 × V4 , г/л
NH3 связанный – отсутствие
Разность (V3 – V4) характеризует свободную щелочность, то есть избыток щелочи в надсмольной воде при разложении.
Свободная щелочь в расчете на гидроксид натрия (NaOH) определяется по формуле:
NaOH свободная = (V3 – V4) × 0,4, г/л
Использованные источники
1) Глузман Л.Д. Лабораторный контроль коксохимического производства. /Л.Д. Глузман, И.И. Эдельман. - М.: Металлургия, 1968. 472 с.
2) Методическое руководство по анализу технологических и сточных вод предприятий черной металлургии. 2-е изд., перераб. и доп. М: Металлургия, 1988, 360 с.