Задание 1. Проведите калибровку шкалы барабана монохроматора по известным линиям паров ртути. Для этого получите спектр излучения ртутной лампы. Запишите показания N на барабане, отвечающие наиболее ярким линиям спектра, и соответствующие им длины волн 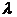 , взятые из спектральной таблицы. Результаты измерений внесите в таблицу 1 и постройте по ним калибровочный график, откладывая по оси абсцисс деления барабана N, а по оси ординат длины волн
, взятые из спектральной таблицы. Результаты измерений внесите в таблицу 1 и постройте по ним калибровочный график, откладывая по оси абсцисс деления барабана N, а по оси ординат длины волн 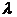 . Калибровку проведите по указанным в таблице длинам волн.
. Калибровку проведите по указанным в таблице длинам волн.
Таблица 1.
| N (дел.) | ||||||||||||
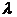 (нм) (нм)
|
Указания:
1) После зажигания ртутной лампы следует выждать 2-3 минуты, пока интенсивность излучения станет достаточной для измерений.
2) Не трогайте сами регулировочные винты монохроматора (при необходимости позовите лаборанта). Калибровку проводите только с помощью барабана.
Задание 2. Получите линейчатые спектры двух неизвестных вам газов. Определив из наблюдений положение наиболее ярких спектральных линий (по барабану), найдите с помощью калибровочного графика соответствующие им длины волн. Затем по спектральным таблицам установите, какие газы были даны для исследования.
По результатам измерений заполните таблицу 2.
Таблица 2
| N (дел.) | 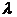 (нм) (нм)
| Элементы |
Указания:
1) Для получения спектра установите трубку с исследуемым газом на специальную платформу. Поставьте ее вблизи входной щели и зажгите в ней электрический разряд. Отцентрируйте ее, т. е. проследите за тем, чтобы светящаяся часть трубки попала на оптическую ось коллиматора. Тогда яркость спектральных линий будет максимальной.
2) При расшифровке спектра неизвестного газа для каждой спектральной линии выпишите из таблицы не один, а ряд элементов, дающих излучение с длиной волны, близкой к найденной. Это повысит точность анализа. Неизвестный газ можно определить по частоте его «попаданий» в каждую из этих групп.
Задание 3.
а) Получите спектр атомарного водорода, заключенного в трубку, и определите длины волн его линий по калибровочному графику.
б) Рассчитайте значение постоянной Ридберга 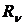 по измеренным длинам волн (формула (1)), взяв n = 2 и k = 3 (красная линия), k = 4 (зеленоголубая линия), k = 5 (синяя линия). Окончательное значение
по измеренным длинам волн (формула (1)), взяв n = 2 и k = 3 (красная линия), k = 4 (зеленоголубая линия), k = 5 (синяя линия). Окончательное значение 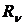 определите как среднее из найденных. Сравните полученное из вашего эксперимента значение
определите как среднее из найденных. Сравните полученное из вашего эксперимента значение 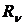 с его табличным значением.
с его табличным значением.
в) Используя найденное экспериментальное значение постоянной Ридберга, рассчитайте значения энергии электрона в атоме водорода при n = 1, 2, 3, 4 и сравните со значениями на рис 1.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Сформулируйте постулаты Бора. Объясните происхождение спектральных линий в спектре атомарного водорода. Какую роль играют числа n и k в формуле (1)?
2. Найдите наибольшую и наименьшую длины волн спектральных линий в серии Бальмера.
3. Выведите формулу (6) для постоянной Ридберга на основании теории водородоподобного атома.
4. Какую наименьшую энергию должны иметь электроны, чтобы при возбуждении атома водорода ударами этих электронов появились все линии всех серий атомарного водорода?
5. Объясните принцип работы монохроматора.
6. Чем различаются по внешнему виду спектры, полученные с помощью призмы и дифракционной решетки?
7. Зависит ли калибровочная кривая от рода газа, с помощью которого она получена?
8. При помощи градуировочного графика оцените величину линейной дисперсии Dl монохроматора (в делениях шкалы на нм) для участков спектра с длиной волны 1) 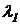 = 450 нм; 2)
= 450 нм; 2) 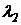 = 650 нм.
= 650 нм.
9. Какова минимальная разность длин волн 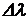 для двух близких линий, разрешаемых спектральным аппаратом с разрешающей способностью R = 1000 на участке спектра с
для двух близких линий, разрешаемых спектральным аппаратом с разрешающей способностью R = 1000 на участке спектра с 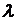 = 500 нм?
= 500 нм?