Рефрактометрический метод анализа
белка основан на измерении показателя преломления белкового раствора, зависящего от его концентрации, температуры, длины волны падающего света и природы вещества.
Между показателем преломления (n) и концентрацией белка в растворе характерна прямо пропорциональная зависимость. Поэтому концентрацию белка в исследуемом растворе находят по показателю преломления с помощью калибровочной кривой, построенной по стандартному раствору белка.
Измерения проводят с помощью специального прибора – рефрактометра, с устройством которого можно ознакомиться по инструкции, прилагаемой к прибору.
Реактивы и оборудование: стандартный раствор белка, раствор исследуемого белка, рефрактометр, пипетки мерные на 1, 2, 5 мл, колба мерная на 100 мл, стеклянные палочки, фильтровальная бумага.
Выполнение работы. В колбах на 100 мл готовят серию (5-6) стандартных растворов белка с концентрациями 1 – 8 мг/мл, измеряют их показатели преломления (n) с помощью рефрактометра, предварительно установив ноль по воде (показатель преломления воды при температуре 20°С равен 1,333). Если во время проведения измерений температура не равна 20°С, то в полученное значение показателя преломления вносят поправку 0.0001 на каждый градус. В случае более низкой температуры поправку вычитают, более высокой – прибавляют. После этого строят график зависимости в координатах n - f (c). Затем, измерив показатель преломления исследуемого раствора, по построенной калибровочной кривой определяют его концентрацию. Результат пересчитывают на 100 г продукта.
Определение массовой доли белка методом формольного титрования
Сущность метода заключается в блокировке NH-групп белков формальдегидом, в результате чего освобождаются карбоксильные группы, которые могут быть оттитрованы щёлочью:
HOOC - R - NH2 + HCOH --> HOOC - R - N = CH2 + H2O
метилен-аминокислота
HOOC - R - N = CH2 + NaOH --> NaOOC - R - N = CH2 + H2O.
В колбу на 100 мл отмеряют пипеткой 10 мл молока, прибавляют 10 капель 1% раствора фенолфталеина и титруют из бюретки 0,1 н раствором щёлочи до не исчезающей слабо-розовой окраски. Затем добавляют 2 мл 40% раствора формалина (предварительно нейтрализованного щёлочью) и вновь титруют 0,1 н раствором щёлочи до такой же окраски. Объём щёлочи, пошедшей на второе титрование, умноженный на 1,94, и даёт массовую долю белков в молоке. После умножения объёма щёлочи на коэффициент 1,38 получают содержание казеина в молоке.
Метод формольного титрования основан на нейтрализации карбоксильных групп моноаминодикарбоновых кислот белков раствором гидроксида натрия, количество которого, затраченное на нейтрализацию, пропорционально массовой доле белка в молоке.
Йодометрическое титрование
^ Название работы: Содержание белка в хлебобулочных изделиях
Источник: https://5fan.ru/wievjob.php?id=1265
КВАЛИФИКАЦИОННАЯ РАБОТА Содержание белка в хлебобулочных изделиях по специальности 020201 – биология
Содержание белка в хлебобулочных изделиях
Качественные реакции
Биуретовая реакция (реакция Пиотровского) - взаимодействия белка в щелочной среде с с сульфатом меди с образование соединения, окрашенного в фиолетово-синий или в фиолетово-красный цвет.
Биуретовую реакцию дают все белки, так как в результате образуется комплекс меди с пептидной связью в молекуле белка. С помощью этой реакции идентифицируются белки
Ксантопротеиновая реакция. Это реакция на белок, которые содержат ароматические аминокислоты, часть которых является незаменимыми для человека.
Это реакция с концентрированной азотной кислотой
Для ее осуществления к р-ру белка прибавляют конц. HNO3 до тех пор, пока не прекратится образование осадка, к-рый при нагр. окрашивается в желтый цвет. Окраска возникает в результате нитрования ароматич. колец аминокислотных остатков белка (тирозина и триптофана). При добавлении к охлажденной жидкости избытка щелочи появляется оранжевое окрашивание, обусловленное образованием солей нитроновых к-т с хиноновой системой сопряженных двойных связей
Реакция с хингидроном

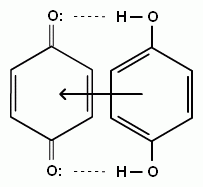
С 1844 года известен хингидрон. Это интенсивно окрашенное, практически черное молекулярное соединение хинона и гидрохинона (состав 1: 1). Хингидрон имеет структуру сандвичего типа. Это комплекс с переносом заряда (КПЗ), в котором имеется общая молекулярная орбиталь с неспаренным электроном. Однако полного переноса электрона не происходит, и в целом молекула хингидрона не обладает радикальными свойствами. В хингидроне оба фрагмента связаны водородными связями.
A-Аминокислоты реагируют с нингидрином, образуя сине-фиолетовый комплекс (пурпур Руэманна), интенсивность окраски которого пропорциональна количеству аминокислоты.
Реакция идет по схеме:
Реакция с нингидрином используется для визуального обнаружения a-аминокислот на хроматограммах (на бумаге, в тонком слое), а также для колориметрического определения концентрации аминокислот по интенсивности окраски продукта реакции.
Описание опыта. В пробирку наливают 1 мл 1%-го раствора глицина и 0,5 мл 1%-го раствора нингидрина. Содержимое пробирки осторожно нагревают до появления сине-фиолетового окрашивания.
РЕАКЦИЯ ФОЛЯ
Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Описание опыта. В пробирку наливают 1 мл раствора цистина, прибавляют 0,5 мл 20%-го раствора гидроксида натрия. Смесь нагревают до кипения, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):