Тема урока: Тепловой эффект химических реакций»
Цели урока: Обеспечить развитие представлений учащихся о законе сохранения энергии.
Организовать деятельность учащихся по применению знаний закона сохранения
энергии в разнообразных ситуациях.
Актуализировать личностный смысл учащихся к изучению темы, помочь осознать
практическую направленность учебного материала.
Содействовать развитию у школьников научных методов познания (наблюдение,
эксперимент), химически правильной речи.
, самодиагностике.
Оборудование: компьютер, проектор, экран.
Содержание урока: Закон сохранения энергии. Превращение энергии в ходе химических реакций.
Тепловой эффект химической реакции. Экзо– и эндотермические реакции.
Термохимические уравнения. Определение теплового эффекта химической
реакции.
Объяснение нового материала.
Тема сегодняшнего урока «Тепловой эффект химических реакций». Но, сначала повторим:
· Назовите химический знак кислорода?
· Какое положение занимает кислород в периодической таблице Д.И.Менделеева?
· Какова его Аr?
· Назовите валентность кислорода?
· Каково содержание кислорода в земной коре? В состав каких веществ входит элемент кислород?
· Составьте химические формулы следующих оксидов:
NaO, CaO, AlO, CO, SO, NO, ClO.
· Какова химическая формула простого вещества кислорода?
· Какова его Мr? М?
· Где в природе находится кислород как простое вещество?
· Перечислите физические свойства кислорода.
· Перечислите химические свойства кислорода.
· Закончите следующие уравнения химических реакций:
Cu + O2 à …; S +O2 à …; CH4 + O2 à … + …; H2S + O2 à … + ….
· Какие из них относятся к реакциям окисления, а какие к реакциям горения?
· По каким признакам вы это определили?
- Да, действительно, в результате реакций горения выделяется свет и тепло, которые мы можем увидеть и почувствовать. В результате некоторых других химических реакций теплота, наоборот, затрачивается или поглощается, и мы можем почувствовать понижение температуры. В этом случае мы можем говорить также о выделении или поглощении энергии.
В каждом веществе запасено определенное количество энергии. С этим свойством веществ мы сталкиваемся уже за завтраком, обедом или ужином, так как продукты питания позволяют нашему организму использовать энергию самых разнообразных химических соединений, содержащихся в пище. В организме эта энергия преобразуется в движение, работу, идет на поддержание постоянной (и довольно высокой!) температуры тела.
Энергия химических соединений сосредоточена главным образом в химических связях. Чтобы разрушить связь между двумя атомами, требуется ЗАТРАТИТЬ ЭНЕРГИЮ. Когда химическая связь образуется, энергия ВЫДЕЛЯЕТСЯ.
Любая химическая реакция заключается в разрыве одних химических связей и образовании других.
Когда в результате химической реакции при образовании новых связей выделяется энергии БОЛЬШЕ, чем потребовалось для разрушения "старых" связей в исходных веществах, то избыток энергии высвобождается в виде тепла. Примером могут служить реакции горения. Например, природный газ (метан CH4) сгорает в кислороде воздуха с выделением большого количества теплоты (сайд.). Такие реакции называются ЭКЗОТЕРМИЧЕСКИМИ от латинского "экзо" - наружу (имея в виду выделяющуюся энергию).

В других случаях на разрушение связей в исходных веществах требуется энергии больше, чем может выделиться при образовании новых связей. Такие реакции происходят только при подводе энергии извне и называются ЭНДОТЕРМИЧЕСКИМИ (от латинского "эндо" - внутрь). Примером является образование оксида углерода (II) CO и водорода H2 из угля и воды, которое происходит только при нагревании (слайд).
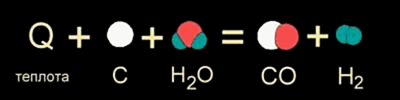
Таким образом, любая химическая реакция сопровождается выделением или поглощением энергии. Чаще всего энергия выделяется или поглощается в виде теплоты (реже - в виде световой или механической энергии). Эту теплоту можно измерить. Результат измерения выражают в килоджоулях (кДж) для одного МОЛЯ реагента или (реже) для моля продукта реакции. Такая величина называется ТЕПЛОВЫМ ЭФФЕКТОМ РЕАКЦИИ. Например, тепловой эффект реакции сгорания водорода в кислороде можно выразить любым из двух уравнений (слайд):
2 H2(г) + O2(г) = 2 H2О(ж) + 572 кДж
или
H2(г) + 1/2 O2(г) = H2О(ж) + 286 кДж
Оба уравнения одинаково правильны и оба выражают тепловой эффект экзотермической реакции образования воды из водорода и кислорода. Первое - на 1 моль использованного кислорода, а второе - на 1 моль сгоревшего водорода или на 1 моль образовавшейся воды.
Значки (г), (ж) обозначают газообразное и жидкое состояние веществ. Встречаются также обозначения (тв) или (к) - твердое, кристаллическое вещество, (водн) - растворенное в воде вещество и т.д.
Обозначение агрегатного состояния вещества имеет важное значение.
Уравнения химических реакций, в которых вместе с реагентами и продуктами записан и тепловой эффект реакции, называются ТЕРМОХИМИЧЕСКИМИ УРАВНЕНИЯМИ.
Тепловые эффекты химических реакций нужны для многих технических расчетов. Представьте себя на минуту конструктором мощной ракеты, способной выводить на орбиту космические корабли и другие полезные грузы (слайд). 
Рис. Самая мощная в мире российская ракета "Энергия" перед стартом на космодроме Байконур. Двигатели одной из её ступеней работают на сжиженных газах - водороде и кислороде.
Допустим, вам известна работа (в кДж), которую придется затратить для доставки ракеты с грузом с поверхности Земли до орбиты, известна также работа по преодолению сопротивления воздуха и другие затраты энергии во время полета. Как рассчитать необходимый запас водорода и кислорода, которые (в сжиженном состоянии) используются в этой ракете в качестве топлива и окислителя?
Без помощи теплового эффекта реакции образования воды из водорода и кислорода сделать это затруднительно. Ведь тепловой эффект - это и есть та самая энергия, которая должна вывести ракету на орбиту. В камерах сгорания ракеты эта теплота превращается в кинетическую энергию молекул раскаленного газа (пара), который вырывается из сопел и создает реактивную тягу.
В химической промышленности тепловые эффекты нужны для расчета количества теплоты для нагревания реакторов, в которых идут эндотермические реакции. В энергетике с помощью теплот сгорания топлива рассчитывают выработку тепловой энергии.
Врачи-диетологи используют тепловые эффекты окисления пищевых продуктов в организме для составления правильных рационов питания не только для больных, но и для здоровых людей - спортсменов, работников различных профессий. По традиции для расчетов здесь используют не джоули, а другие энергетические единицы - калории (1 кал = 4,1868 Дж).