Циклокарбонаты - это новый класс соединений, привлекающих внимание исследователей благодаря потенциальной возможности их использования в безопасных для окружающей среды, беспористых и влагонечувствительных безизоцианатных уретанах и полимерах со звеньями подобного типа.
Циклокарбонаты имеют минимум одну циклокарбонатную функциональную группу на конце цепи олигомерной молекулы (здесь и далее R - алифатический заместитель):
 Рисунок 1 - Циклокарбонат
Рисунок 1 - Циклокарбонат
Циклокарбонаты могут быть синтезированы множеством различных способов. Основным способом производства циклокарбонатов является пропускание диоксида углерода через жидкие эпоксидные олигомеры в присутствии катализатора [3, 4] или взаимодействием эфиров хлорогидрина с карбонатами щелочных металлов или олигомерных полиолов с эфирами (хлоридами) угольной кислоты [5, 6, 7, 8, 9, 10].
Наиболее современным способом получения циклокарбонатов является взаимодействие диоксида углерода с эпоксидным олигомером с функциональностью не менее 2 при низком давлении и температуре в специальном аппарате, позволяющем увеличить площадь поверхности контакта фаз или в каскаде реакторов, в присутствии специального катализатора [4].
Аппарат в данном случае представляет собой барботер с перемешивающим устойством с подводом газа с помощью мешалки [4]:
 Рисунок 2 - Устройство аппарата для синтеза циклокарбонатов, взаимодействием диоксида углерода и эпоксидных олигомеров в присутствии катализатора [4]
Рисунок 2 - Устройство аппарата для синтеза циклокарбонатов, взаимодействием диоксида углерода и эпоксидных олигомеров в присутствии катализатора [4]
В данном аппарате осуществляется активное перемешивание и одновременное интенсивное пропускание диоксида углерода через эпоксидный олигомер, без излишнего вспенивания. В таком случае обеспечивается большая площадь контакта фаз, что приводит к интенсификации процесса взаимодействия и не требует повышения температуры [4].
Реакция хорошо проходит уже при температуре 70-180° C и давлении не менее 0,1 МПа, желательно 0,1-1,5 МПа, за 40-120 минут. Для более чистого продукта предпочтительны более низкие температуры синтеза [4].
Катализаторами данной реакции являются соли аммония, фосфония, четвертичного мышьяка или галогениды щелочных металлов [4].
Так же возможно проводить синтез в тонкослойном реакторе при температуре 65-105° C и при давлении 0,6-0,85 атмосфер в течение 190-330 минут, но в данном случае выход на много меньше, чем при использовании специализированного реактора (см. рисунок 2) [4].
Так же возможен синтез в реакционном растворе этилен карбоната (в данном случае используется обычный барботер), или пропилен карбоната при температуре 60-140° C и давлении 1-10 атмосфер, в присутствии катализатора, в течение как минимум 180 минут. Катализаторами реакции являются азото- и фосфоросодержащие соединения, а так же четвертичные аммониевые соединения. Даже при синтезе из соединений чувствительных к температуре и обладающих стерическими затруднениями для реакции синтеза, побочные реакции не проходят с заметными скоростями, что приводит к получению чистого продукта [3].
Реакцию взаимодействия можно представить данным образом:
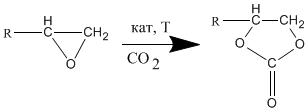 Рисунок 3 - Реакция синтеза циклокарбоната из эпоксида
Рисунок 3 - Реакция синтеза циклокарбоната из эпоксида
В настоящее время производится широчайший ассортимент циклокарбонатов, свойства которых достаточно сильно отличаются из-за наличия в молекуле циклокарбоната не только концевых циклокарбонатных групп, но и разного рода заместителей в боковых цепях макромолекулы, из-за других концевых групп (на концах цепи макромолекулы циклокарбоната могут быть аминные, акрилатные, эпоксидные и другие функциональные группы), из-за строения самой макроцепи макромолекулы и многих других факторов.
В данном случае мы будем рассматривать только лишь свойства циклокарбонатов, продиктованные наличием циклокарбонатной группы.
Циклокарбонаты принимают участие в реакциях с различными нуклеофилами. Наиболее широко изучены реакции взаимодействия циклокарбонатов с аминами (см. рисунок 4)
 Рисунок 4 - Реакция взаимодействия циклокарбонатов с аминами
Рисунок 4 - Реакция взаимодействия циклокарбонатов с аминами
Продуктами реакции являются 2 типа аминоспиртов (в примерном соотношении 30: 70 соответственно). Основным продуктом является второй аминоспирт. Исследования кинетики показывают, что выход реакции увеличивается при увеличении концентрации амина и так же реакция катализируется гидроксилом. Так как продукт реакции катализирует реакцию, то соответсвенно данную реакцию можно назвать автокаталитической [5, 11, 12].
Реакция аминолиза протекает по схеме, изображенной на рисунке 4, при низких и нормальных температурах, при повышенных температурах (>100° C) возможно протекание реакции взаимодействия продуктов реакции (аминоспиртов) с аминами еще не вступившими в реакцию с циклокарбонатами, что приводит к образованию мочевины [13].
Так же, при исследовании кинетики реакций взаимодействия с аминами на примере этиленциклокарбоната и нескольких алкилированных аминов была обнаружена положительная корреляция между количеством атомов водорода в б-положении относительно амина и скоростью реакции. Таким образом можно говорить о том, что амины на первичном атоме углерода реагируют быстрее, чем на вторичных, а на вторичных - быстрее, чем на третичных и т.д. [14, 5]
При изучении кинетики реакций взаимодействия с аминами в различных растворителях, было замечено, скорость реакции аминолиза значительно выше в протонных растворителях по сравнению с апротонными, несмотря на то, что скорость реакции растет при увеличении полярности в протонных растворителях [5, 15].
Проводилось совсем немного работ, изучающих взаимодействие циклокарбонатов с заместителями в основной цепи. При изучении большого количества циклокарбонатов с заместителями в цепи макромолекулы было найдено, что скорость реакции с аминами увеличивается с увеличением электроноакцепторых свойств заместителя [16]. Эти исследования идут в разрез с выводами приводимыми Михеевым, которые противоположны [15]. Это говорит о еще недостаточной изученности данного процесса и необходимости дальнейших исследований в этой области.
Кинетические особенности взаимодействия циклокарбонатов с аминами были изучены в [17, 18].
Первая стадия взаимодействия заключается в нуклеофильной атаке карбоксильной группы циклокабоната амином, результатом которой является тетрагидратный комплекс (см. рисунок 5):
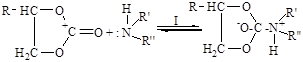 Рисунок 5 - Нуклеофильная атака циклокарбоната амином
Рисунок 5 - Нуклеофильная атака циклокарбоната амином
На второй стадии взаимодействия, следующая молекула амина вовлекается в реакцию. Эта молекула отнимает атом водорода у тетрагидратного итермидиата, который имеет характер биполярного иона (см. рисунок 6):
 Рисунок 6 - Вторая стадия взаимодействия циклокарбонатов с аминами
Рисунок 6 - Вторая стадия взаимодействия циклокарбонатов с аминами
Далее связь C-О разрывается, что вызвано высокой электронной плотностью у атома азота. Образовавшийся ион алкоксида достаточно быстро преобразуется в продукт реакции (см. рисунок 7):
 Рисунок 7 - Третья стадия взаимодействия циклокарбонатов с аминами
Рисунок 7 - Третья стадия взаимодействия циклокарбонатов с аминами
Соотношение количеств образующихся изомерных продуктов зависит от индуктивного эффекта заместителя R, так же как и от объемов заместителей R' и R”.
Когда реакция проводится в протогенном (кислотном) растоврителе, то лимитирующей стадией, определяющей скорость всей реакции, будет стадия депротонирования. В этом случае реакция в целом идет по третьему порядку, и по второму относительно амина. Первая стадия будет протекать достаточно быстро из-за формирования водородных связей между молекулами растворителя и кислородом циклокарбонатной группы (см. русунок 8):
 Рисунок 8 - Формирование водородных связей между молекулами растворителя и циклокарбонатной группой
Рисунок 8 - Формирование водородных связей между молекулами растворителя и циклокарбонатной группой
Когда же реакция проводится в апротонных растворителях, лимитирующей будет первая стадия. В этом случае молекулы растворителя не имеют возможности сформировать водородные связи, которые содействуют протеканию первой стадии. Эта стадия лимитирует и определяет второй порядок для всей реакции вцелом в апротонных растворителях.
Введение в циклокарбонат электронодонорного заместителя приводит к уменьшению частичного положительного заряда на атоме углерода (см. риуснок 9):
 Рисунок 9 - Уменьшение заряда на углероде в случае ввода электронодонорного заместителя в циклокарбонат
Рисунок 9 - Уменьшение заряда на углероде в случае ввода электронодонорного заместителя в циклокарбонат
Это приводит к уменьшению реакционной способности циклокарбоната. Электроноакцепторные заместители, увеличивающие электрофильность атома углерода карбонильной группы, способствуют реакциям взаимодействая с аминами в большей степени. Таким образом, скорости реакции эпоксидных и циклокарбонатных групп сопоставимы и принимают значения 10-4 при 500С. Какая из реакций будет преимущественно проходить во время отверждения эпокси-аминной системы строго зависит от механизма реакции и структуры молекулы модификатора [19].
Как уже говорилось, циклокарбонаты способны взаимодействовать и с другими нуклеофилами, но данные реакции мало изучены по сравнению с реакцией аминолиза. Так, например, реакция циклокарбонатов с уксусной кислотой идет с выделение диокида углерода и образованием сложного эфира [20, 5]:
 Рисунок 10 - Реакция взаимодействия циклокарбоната с уксусной кислотой
Рисунок 10 - Реакция взаимодействия циклокарбоната с уксусной кислотой
По такому же принципу происходит взаимодействие циклокарбонатов с фенолами - так же выделяется диоксид углерода и образуется простой эфир [5, 21, 22, 23, 24].
Данные особенности взаимодействия циклокарбонатных групп предопределили сферы применения циклокарбонатов в качестве модификаторов различных физико-механических и физико-химических свойств композиций.
Одной из наиболее важных сфер применения циклокарбонатов является применение их для модификации свойств эпоксидных смол. Эпоксидные смолы являются одними из самых важных термоотверждаемых смол. Но у них есть существенный недостаток, при их отверждении образуется трехмерный полимер с чрезвычайно большой частотой сшивки макромолекул и достаточно высокой хрупкостью. Для повышения стойкости к ударным нагрузкам, эластичности и других механических свойств было испробовано множество различных подходов. Так при использовании циклокарбонатов, увеличивается гибкость макромолекул в сшитой структуре эпоксидных лаков и клеев. Принимая во внимание тот факт, что неизоцианатные полиуретаны (НИПУ), синтезированные без использования изоцианатов, могут быть получены при отверждении эпоксидных смол, модифицированных циклокарбонатами, с алифатическими аминами (реакция аминолиза). Эта реакция была использована для модификации.
Проводилось отвержение эпоксидов с частично замещенными концевыми эпоксидными группами на циклокарбонатные при помощи аминов, по схеме [25, 26, 27, 21, 28]:
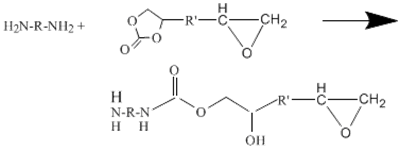 где R' - фрагмент эпоксидного олигомера
где R' - фрагмент эпоксидного олигомера
Рисунок 11 - Отверждение модифицированной эпоксидной смолы аминами
Так, для всех полученных материалов такого типа было замечено:
· время гелеобразования уменьшается при увеличении концентрации циклокарбонатных групп;
· уменьшается вязкость композиций
· реакция модифицированных смол идет с меньшим экзотермическим эффектом, чем немодифицированных;
· отвержденные модифицированные смолы показывают большую стойкость к ударным нагрузкам, гибкость и адгезию к материалам [5, 29];
· даже при наличии менее густой сетки «сшивок» большая часть прочностных характеристик материала выше [5, 25, 30]
Такие изменения можно объяснить наличием полярных уретановых групп и образовавшимися водородными связями. Так же эластичность цепям придается благодаря наличию эфирных алифатических сшивок в отвержденном материале [27, 31, 12].
Данного рода модификацию эпоксидов проводят для получения высокопрочных композиций для пропитки стекло-, угле-, органо- и боропластиков [32, 33], клеев-герметиков для безаварийного ремонта трубопроводов [34], а так же для производства различного типа покрытий, клеев, уплотнителей, искусственной кожи [35], растяжимой изоляции для устойчивых к усталости проводов и металлической проволоки [36]
Другой важной областью применения циклокарбонатов на ряду с получением модифицированных эпоксидных композиций (после отверждения получается НИПУ), является синтез на основе 2-х функциональных циклокарбонатов модифицированных аминных отвердителей.
Так при взаимодействии полиаминов (напиример, триэтилентетраамина) с 2-х функциональными циклокарбонатами получаются полиаминоуретаны (см. рисунок 12):
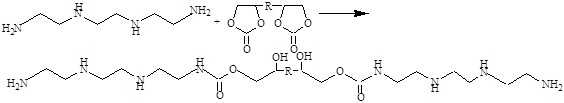 Рисунок 12 - Получение полиаминоуретанов
Рисунок 12 - Получение полиаминоуретанов
Полиаминоуретаны в отвержденном состоянии представляют собой так называемые гибридные неизоцианатные полиуретаны - ГНИПУ [37]). Они содержат в своей структуре дополнительные гидроксильные группы, приводящие к увеличению стабильности и снижению токсичности аминных отвердителей. Так же их введение в эпоксидную композицию позволяет поддерживать более низкую вязкость во время их переработки. Причем при модификации эпоксидных смол с помощью ГНИПУ время гелеобразования композиции снижается в большей степени по сравнению с введением циклокрбонатов. Это может быть объяснено более высокой концентрацией гидроксильных групп, катализирующих процесс отверждения, в начальный момент реакции [27, 38, 39]. Так же одним из преимуществ такого рода отвержденных композиций является отсутствие в них пор, поскольку в процессе отверждения не происходит выделения диоксида углерода, выделяющегося при отверждении циклокарбонатов аминами. Это предопределяет преимущественное использование данного рода композиций для производства химически стойких покрытий [40].
Одной из особенностей композиций на базе циклокарбонатов является их стойкость к воздействию ультрафиолетового излучения (УФ-стойкость). До недавнего времени не было попыток синтезировать стойкие неизоцианатные полиуретаны (НИПУ) для покрытий, но в последнее время ситуация изменилась, было исследовано большое количество способов синтеза УФ-стойких олигомеров с циклокарбонатными, эпоксидными, аминными концевыми группами, а так же ГНИПУ и УФ-стойких НИПУ покрытий [41].
Проблема состоит в отсутствии возможности применения данного рода соединений для нанесения покрытий. Возможно лишь использование таких соединений в качестве добавок к уже существующим композициям. Такой способ применения не позволяет достичь желаемых показателей УФ-стойкости покрытий.
Для решения проблемы были синтезированы циклокарбонаты на основе акриловых эпоксидных смол. Полученные после отверждения НИПУ (отверждение велось при температуре 110оС течение 2 часов) немного желтели под воздействием УФ света лишь после 200 часов экспозиции, что в 2 раза превышает показатель простых отвержденных эпоксидных смол. При использовании аминных УФ-стабилизаторов, производных 2,2,6,6-тетраметил пиперидина (смотри рисунок 13), покрытия на основе ГНИПУ не испытывали изменений в течение 2000 часов в погодных условиях Флориды. Таким образом, покрытия на основе акриловых циклокарбонатов обладают светостойкостью, как и у обычных полиуретановых покрытий на основе акриловых гидроксилсодержащих олигомеров и изоцианатов, но с более высокими механическими свойствами [41].
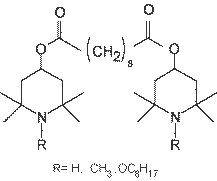 Рисунок 13 - Аминный светостабилизатор на основе 2,2,6,6-тетраметил пиперидина
Рисунок 13 - Аминный светостабилизатор на основе 2,2,6,6-тетраметил пиперидина
Так же покрытия с хорошей стойкостью к действия растворителей, хорошим блеском и твердостью были получены на основе винилэтиленциклокарбоната (синтез см. рисунок 14), отверждаемых при помощи ди- и три- функциональных низкомолекулярных аминов уже при температуре 80 оС. Таким же образом могут быть отверждены покрытия из латексов на основе циклокарбонатов [5, 42].
 Рисунок 14 - Синтез винилэтиленциклокарбоната из эпоксибутена
Рисунок 14 - Синтез винилэтиленциклокарбоната из эпоксибутена
В недавнем времени были получены сополимеры винилэтиленциклокарбоната с метилметакрилатом, этил акрилатом, бутилметакрилатом и стиролом. Но данного рода соединения оказались плохо совмеситмыми с ратворителями, позволяющими наносить такие покрытия, а так же имели высокие температуры гелеобразования 100-144оС [5, 43].
Твердые полимеры, содержащие циклокарбонатные группы, могут быть смешаны с карбаматами аминов и потом использованы в качестве порошковых красок [5, 44].
Водорастворимые акриловые смолы, содержащие циклокарбонатные группы, были получены и сшиты с помощью многофункциональных аминов при температуре 110 оС в течение 30 минут. Причем сформированные покрытия были стойки к действию растворителей [5, 45].
Кислотостойкие покрытия могут быть получены на основе реакции взаимодействия полимеров, содержащих карбоксильные и циклокарбонатные группы, причем группы обоих типов могу принадлежать как различным полимерным молекулам, так и одной. Для отверждения данного рода композиций требуется присутствие катализатора. Отверждение проходит за счет 2-х последовательных реакций: на первом этапе происходит декарбонизация циклокарбоната с образованием эпоксида; на втором - отверждении эпоксида под действием кислоты и катализатора [5, 46, 47].
Так же на основе НИПУ производятся наливные полы и краски для промышленного применения. Данные двухкомпонентные смеси имеют уникальные свойства - наилучшую среди полиуретанов механическую прочность и химическую стойкость на уровне эпоксидов. Одним из преимуществ является безопасность для здоровья из-за отсутствия в составе изоцианатов и безопасность их производства для окружающей среды. Данные покрытия нечувствительны к влажности воздуха или поверхности и так же не имеют в своем составе пор [48].
В значительно меньшей степени циклокарбонаты используются в других отраслях промышленности: в медицине - для производства фотоотверждаемых зубных цементов [5, 49], для иммобилизации энзимов [5, 50, 51], для анализа пенициллина [5, 52]; в электрохимии - этилен- и пропиленциклокарбонаты используются в качестве электролитов [5, 53, 54, 55] и пропиленциклокарбонатакрилат (см. Рисунок 15) как полимерный гель для аккумуляторов [5]; в фототехнике - чувтсвительные комопозициии для фотополимеризации без необходимости иметь фотоинициатор [5, 56, 57, 58, 59, 60].
 Рисунок 15 - Пропиленциклокарбонатакрилат
Рисунок 15 - Пропиленциклокарбонатакрилат
Одним из наиболее распространенных циклокарбонатных модификаторов является трехфункциональный олигоэфирциклокарбонат (смотри рисунок 16). В отечественной промышленности налажено производство данного рода модификаторов научно-производственным предприятием «Макромер». Производятся олигоэфирциклокарбонаты, которые носят торговое название Лапролаты (физико-химический свойства представлены в таблице 1). Данные модификаторы предназначены для использования в качестве реакционноспособных модификаторов эпоксидных систем для получения эпоксиуретановых материалов различного назначения: покрытий, адгезивов, герметиков, строительных мастик, пигментных паст и т.п.
 Рисунок 16 - Трехфункциональный олигоэфирциклокарбонат
Рисунок 16 - Трехфункциональный олигоэфирциклокарбонат
Отверждаются данные циклокарбонаты так же - первичными ди- и полиаминами с образованием гидроксиуретановых связей. Так же в составе полученного уретана появляется большое количество эфирных связей из олигоэфирной составляющей Лапролата, которые способствуют эластификации полученного 3-х мерного полимера.
Таблица 1 - Физико-химичекие свойства Лапролатов [61]
| Марка | Лапролат 803 | Лапролат 301 |
| Функциональность | ||
| Массовая доля циклокарбонатных групп, % | 21,0-31,0 | 26,0-31,0 |
| Массовая доля эпоксидных групп, %, не более | 2,5 | 1,0 |
| Вязкость при 25°С, мПа.с | 3500-7500 | 20-30 |
Лапролаты растворимы в большинстве органических растворителей, хорошо совмещаются с эпоксидными смолами и аминами, устойчивы при длительном хранении.
Добавление Лапролатов в эпоксидные системы увеличивает ударную вязкость, эластичность, адгезию, устойчивость к истиранию и т.д. отвержденных материалов, обеспечивает стойкость материалов к гидролизу и термоокислению [61].