Экспериментальные исследования на животных с использованием ЭКГ сверхвысокого разрешения как этап создания методологии и инструментария функциональной электрокардиографии ишемии
М.М. Галагудза1,2, К.В. Зайченко3
1Федеральный Центр сердца, крови и эндокринологии им. В.А. Алмазова Министерства здравоохранения Российской Федерации
2 Санкт-Петербургский государственный медицинский университет им. акад. И.П.Павлова
3 Санкт-Петербургский государственный университет аэрокосмического приборостроения
Experimental animal studies using ultrahigh-resolution ECG as a prerequisite for development of the methodology and equipment for functional electrocardiography of ischemia
М.М. Galagudza1,2, К.V. Zaichenko3
1 V.A. Almazov Federal Heart, Blood and Endocrinology Centre
2 I.P. Pavlov Federal Medical University
3 St-Petersburg State University of Aerospace Instrumentation
Аннотация. В работе проведено исследование возможности получения дополнительной информации о развитии ишемической болезни сердца из ЭКГ-сигналов, регистрируемых с использованием компьютеризированного электрокардиографа сверхвысокого разрешения, при проведении экспериментов по моделированию ишемии миокарда у подопытных животных. Эти модели выполнялись на наркотизированных крысах–самцах линии Wistar на целостном организме с сохраненными нейрогуморальными влияниями на сердце, путем перевязки левой коронарной артерии. Был проведен анализ характеристик полученных ЭКГ-сигналов. При этом зафиксированы значительные изменения высокочастотных составляющих этих сигналов в процессе развития ишемии, в частности существенное снижение их спектральной плотности мощности. Показано значение такого анализа ЭКГ-сигналов для создания методологии и инструментария функциональной электрокардиографии ишемии.
Abstract. In the present study, the potential of getting additional information about the characteristics of ischemic heart disease from ECG signal registered using computer-based electrocardiograph of ultrahigh resolution was assessed in the animal model of myocardial ischemia. Myocardial ischemia was elicited in the anesthetized male Wistar rats retaining systemic neurohumoral influences on the heart by means of left coronary artery ligation. The characteristics of thus obtained ECG signals were analyzed. The significant changes in the high-frequency components of these signals, including a substantial decrease in their spectral density, were detected during early phases of ischemia. The role of such an analysis of ECG signal in the development of methodology and equipment for functional detection of ischemia is demonstrated.
Ключевые слова: функциональная электрокардиография, сверхвысокое разрешение, ишемия миокарда, моделирование, экспериментальные исследования, спектральный анализ
Keywords: functional electrocardiography,ultrahigh-resolution, myocardial ischemia, modeling, experimental studies, spectral analysis.
Реферат
Исследована возможность совершенствования ЭКГ–диагностики ишемии, в том числе верификации диагноза ишемической болезни сердца (ИБС), на основе дополнительной информации, получаемой из ЭКГ-сигнала, в частности о стадии развития ишемического повреждения. Изучение параметров ЭКГ-сигнала на разных этапах экспериментов по моделированию ишемии миокарда производились с использованием метода электрокардиографии сверхвысокого разрешения (ЭКГ СВР), позволяющего регистрировать низкоамплитудные и высокочастотные (ВЧ) составляющие электрокардиосигналов (ЭКС). Модели ишемии миокарда выполнялись на наркотизированных животных (крысах–самцах линии Wistar) на целостном организме с сохраненными нейрогуморальными влияниями на сердце, путем перевязки левой коронарной артерии. В ходе опытов применялась искусственная вентиляция легких и микрохирургическая техника. С целью верификации факта возникновения ишемии миокарда проводилась оценка размеров анатомической зоны риска и зоны инфаркта. В ходе эксперимента у животных регистрировались электрокардиограммы с помощью экспериментального компьютеризированного электрокардиографа «СВР-2К», реализующего метод ЭКГ СВР и контрольного электрокардиографа «Кардиотехника–8». На всех этапах моделирования ишемии-реперфузии миокарда регистрировались ЭКС в низкочастотном- (НЧ) и ВЧ-каналах «СВР-2К». Были исследованы их количественные и качественные характеристики с целью поиска параметров электрокардиограммы (ЭКГ-маркеров), коррелирующих с начальными фазами ишемии, и для подтверждения наличия диагностически значимых и информативных признаков ишемии в НЧ- и ВЧ-областях спектра ЭКС. Проводилось сравнение электрокардиограмм и спектральных составов ЭКС, полученных до перевязки левой коронарной артерии (в норме) и на различных этапах ишемии миокарда. В ходе анализа компонентов спектра ЭКС в ВЧ-канале в процессе развития ишемии зафиксированы их значительные изменения. С развитием ишемии спектральная плотность мощности ВЧ-составляющих ЭКС существенно снижается. При этом на первой минуте после перевязки левой коронарной артерии, когда процесс развития ишемии уже начался, в ЭКС на выходах НЧ-каналов обоих электрокардиографов отсутствуют видимые изменения сигналов по сравнению с нормой, а анализ спектрального состава ВЧ-составляющих ЭКС по методу ЭКГ СВР уже фиксирует заметное снижение уровня спектральной плотности мощности ВЧ-компонентов ЭКС. Описанные изменения спектральных характеристик ЭКС воспроизводились у всех животных экспериментальной группы. Таким образом применение методики ЭКГ сверхвысокого разрешения с последующим спектральным анализом в ВЧ-канале позволяет надежно верифицировать признаки ишемии миокарда уже спустя 60 секунд после перевязки коронарной артерии в эксперименте.
Summary
The potential for refinement of ECG-diagnostics of ischemia, including early verification of ischemic heart disease and determination of the stage of the ischemic injury, was investigated in the present study. The characterization of the ECG signal parameters at the different stages of the experiment was performed using the technique of ultrahigh resolution electrocardiography (UHR-ECG). This technique enables to register both low-magnitude and high-frequency (HF) components of the electrogram (EG). Myocardial ischemia was elicited in the anesthetized male Wistar rats retaining systemic neurohumoral influences on the heart by means of left coronary artery ligation. Experiments were performed using mechanical lung ventilation and microsurgical technique. For verification of the reproducibility of ischemia, both anatomical area at risk and infarct size were determined after the end of the experiment. During the experiments, the ECG was registered by the prototype computer-assisted electrocardiograph “SVR-2K” for UR-ECG and control electrocardiograph “Cardiotechnika-8”. The electrocardiogram was registered in low- (LF) and high-frequency (HF) channels of “SVR-2K” during the entire period of myocardial ischemia-reperfusion injury. We assessed both quantitative and qualitative characteristics of the ECG in order to identify the parameters of ECG (or ECG-markers) which are most closely correlated with the early phases of ischemia, and also for confirmation of the presence of predictive and informative signs of schemia in the HF and LF areas of the ECG spectrum. A comparison of ECG and spectral characteristics of ECG obtained prior to left coronary artery ligation (normal state) was done with the postischemic values. The analysis of the components of ECG spectrum in the HF channel has revealed significant changes during ischemia. The spectral power of the HF components of ECG has been significantly attenuated starting from the beginning of ischemia. It should be noted that on the first minute after coronary artery ligation the LF channels of both electrocardiographs failed to detect any visible changes of the signals as compared with baseline while the analysis of the spectral composition of the HF components according to the technique of the UR-ECG has revealed the substantial decrease in the spectral power of the HF-components of ECG. The described changes in the spectral characteristics of ECG were reproducible among all animals of the experimental group. In conclusion, the application of the UHR-ECG with subsequent spectral analysis in the HF-channel gives the opportunity for decisive verification of the signs of myocardial ischemia already after 60 seconds after coronary artery ligation in the experimental settings.
Несмотря на огромный прогресс в разработке новых методов диагностики и терапии, ишемическая болезнь сердца (ИБС) остается ведущей причиной смертности и инвалидизации трудоспособного населения в большинстве стран мира. В основе лечения острого коронарного синдрома сегодня лежит экстренная реваскуляризация миокарда, то есть максимально быстрое восстановление кровотока к сердечной мышце с помощью различных методик. Однако для выполнения подобного вмешательства требуется не менее скорая верификация диагноза инфаркта миокарда. В настоящее время диагноз инфаркта устанавливается на основе клинических, биохимических и электрокардиографических (ЭКГ) критериев.
К сожалению, следует констатировать, что при использовании применяемых в практической медицине ЭКГ методик возможности диагностики острой ишемии миокарда по ЭКГ-критериям в настоящее время ограничиваются алгоритмом «да-нет» и приблизительным суждением о протяженности очага поражения миокарда – субэндокардиальная или трансмуральная ишемия. При этом нереализованной, но весьма актуальной задачей совершенствования ЭКГ–диагностики ишемии является получение дополнительной информации из ЭКГ-сигнала, в первую очередь, о стадии развития, а затем и о степени ишемического повреждения, его локализации, потенциальной обратимости и других параметрах. Поэтапное решение перечисленных задач может способствовать существенному улучшению результатов диагностики и лечения ишемии на разных стадиях ее развития, в том числе, инфаркта миокарда.
Можно утверждать, что данная область инструментальной диагностики будет революционизирована при обнаружении параметров электрокардиограммы, отражающих выраженность ишемии и состояние адаптации миокарда к ней. Извлечение информации из ЭКГ о подобных взаимосвязях и их верификация ознаменуют эру функциональной электрокардиографии ишемии.
Существует острая необходимость в разработке методов профилактического повышения устойчивости миокарда к ишемии, поскольку не всегда достижимо выполнение экстренной реваскуляризации миокарда в течение 90 минут после возникновения загрудинной боли. К таким методам относятся различные варианты кондиционирования миокарда, когда перед началом продолжительной ишемии или непосредственно после нее выполняются кратковременные эпизоды ишемии (по 3-5 мин.) с последующим столь же кратковременным восстановлением кровотока (реперфузией), предотвращающие те или иные проявления повреждения миокарда, вызванные тестовой ишемией. Разработка подобных подходов и изучение их механизмов требует проведения предварительных экспериментальных исследований на лабораторных животных. Подобные эксперименты направлены, в частности, на выработку оптимального протокола индукции кондиционирования миокарда, включая продолжительность и кратность кондиционирующих ишемических эпизодов.
Отдельную актуальную задачу представляет собой поиск параметров электрокардиограммы, коррелирующих с объемом ишемии и с ее выраженностью. К сожалению, сегодня приходится констатировать, что основной критерий ишемии - девиация сегмента ST - не всегда четко коррелирует с ее выраженностью (Birincioglu et al., 1999) [1].
Для решения указанных задач с 2010 года коллективом сотрудников кафедры медицинской радиоэлектроники ГУАП, кафедры патофизиологии Санкт-Петербургского государственного медицинского университета им. акад. И. П. Павлова и Института экспериментальной медицины Федерального Центра сердца, крови и эндокринологии им. В. А. Алмазова проводятся совместные исследования, посвященные поиску новых ЭКГ-маркеров процесса развития ишемического повреждения миокарда у подопытных животных.
Исследования параметров ЭКГ на разных этапах экспериментов производились на нескольких, специально разработанных в Научно-образовательном центре «Биомедицинской радиоэлектроники и информатики» (НОЦ БРЭИ, ГУАП, СПб), лабораторных макетах, реализующих метод электрокардиографии сверхвысокого разрешения (ЭКГ СВР) [2], [3](нс)* для регистрации низкоамплитудных и высокочастотных (ВЧ) составляющих электрокардиосигналов (ЭКС) в расширенных амплитудном и частотном диапазонах (АЧД). В качестве контрольного прибора использовался электрокардиограф «Кардиотехника–8» (ЗАО «Инкарт», СПб). Экспериментальные исследования проводились на основе моделирования ишемии миокарда по схеме, представленной на рис. 1.
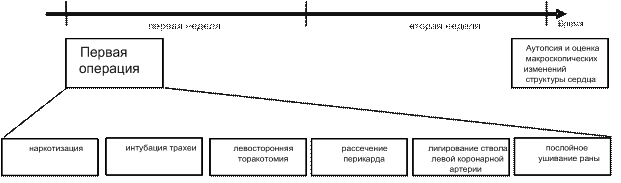
Рис. 1. Схема эксперимента
Модели ишемии миокарда можно разделить на те, что выполняются на наркотизированных животных и на изолированном сердце. Модели in vivo [1] имеют особенно большое значение, поскольку они выполняются на целостном организме с сохраненными нейрогуморальными влияниями на сердце. Модель ишемии миокарда у крыс путем перевязки левой коронарной артерии была впервые предложена Г. Селье с соавторами в 1960 г. К настоящему времени данная модель усовершенствована благодаря применению искусственной вентиляции легких и микрохирургической техники. Модель ишемии миокарда является одной из наиболее часто используемых хирургических моделей заболеваний человека.
Материалы и методы
Все эксперименты проведены в соответствии с «Руководством по уходу и использованию лабораторных животных» (публикация Национального Института Здоровья № 85–23, США) и «Руководством по экспериментальному (доклиническому) изучению новых фармакологических веществ» [4].
Материал исследования. Эксперименты выполнены на крысах–самцах линии Wistar массой 260–330 г (питомник «Рапполово»), содержавшихся в условиях 12/12 часового светового режима и получавших стандартный корм и питьевую воду ad libitum[2]. Фотография, снятая в ходе одного из экспериментов, представлена на рис. 2.
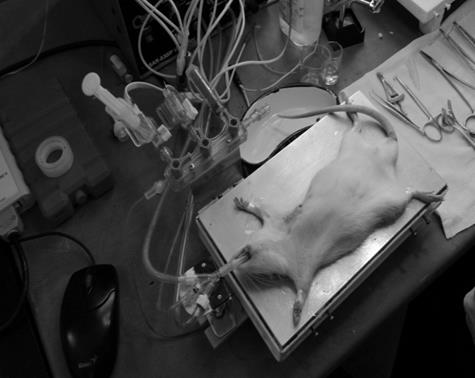
Рис. 2. Подопытное животное на термостатируемом операционном столике
Анестезия. В качестве вводной анестезии использовалось внутрибрюшинное введение пентобарбитала натрия в дозе 60 мг/кг (Pentobarbitalnatrium, Apoteket, Umea, Швеция). В качестве поддерживающей анестезии во всех экспериментах использовали внутривенную инфузию раствора пентобарбитала натрия для достижения хирургического наркоза.
Моделирование ишемии–реперфузии миокарда. Эксперименты проводились при искусственной вентиляции легких через трахеостому (SAR–830Р, Stoelting, США, частота дыхания – 50/мин., дыхательный объем в пределах от 1,5 до 3 мл/100 г массы). Доступ к сердцу производили путем торакотомии в четвертом межреберье слева, вскрывали перикард и, ориентируясь на медиальный край ушка левого предсердия слева и конус легочной артерии справа, определяли локализацию общего ствола левой коронарной артерии (ЛКА), под который с помощью атравматической иглы (6–0) подводили полипропиленовую лигатуру (Cardiopoint, CV–301). Для создания обратимой ишемии миокарда формировали окклюдер[3]: концы лигатуры, охватывающей коронарную артерию, проводили в просвет полиэтиленовой трубки диаметром 1 мм и длиной 5–6 см (PE 40), после чего путем смещения трубки к сердцу добивались окклюзии[4] ЛКА, а в противоположном направлении – реперфузии[5]. С целью поддержания окклюзии в течение 30 минут на трубку накладывали зажим. В ходе эксперимента животные находились на термостатируемом операционном столике; при этом температура тела животного поддерживалась в пределах 37,0±0,5ºС.
Измерения. В ходе экспериментов непрерывно измерялось артериальное давление (АД) специальным датчиком давления (Baxter, США), соединенным с усилителем, через гепаринизированный катетер, введенный в аорту через общую сонную артерию, и регистрировали на персональном компьютере с помощью программного обеспечения PhysExp 2.0 (свидетельство об официальной регистрации программы для ЭВМ № 2004612138 от 17.09.04). Регистрация частоты сердечных сокращений (ЧСС) осуществлялась в исходном состоянии, после торакотомии, перед окклюзией ЛКА, на 15 и 30 минуте окклюзии ЛКА, на 30 и 60 минуте реперфузии, а также в конце эксперимента, т. е. через 90 минут после реперфузии ЛКА.
В ходе эксперимента у животных регистрировали электрокардиограммы на экспериментальном компьютеризированном электрокардиографе «СВР-2К», реализующем метод ЭКГ СВР. Этот электрокардиограф был специально разработан и изготовлен в НОЦ БРЭИ для записи, отображения и обработки информации в процессе проведения данной серии экспериментов на животных. Регистрировались ЭКС в НЧ- и ВЧ-каналах «СВР-2К», а также в режиме реального времени каждые 30 секунд производился расчет в последних десяти кардиоциклах спектральной плотности мощности составляющих ЭКС в ВЧ-канале.. Использование в ходе данного цикла экспериментов для текущего контроля в режиме реального времени именно спектральной плотности мощности составляющих ЭКС в ВЧ-канале было вызвано тем, что в проводившихся ранее исследованиях в Великобритании [5, 6] и в США [7, 8] в области регистрации и анализа ВЧ-компонентов ЭКС для исследования возможности диагностирования ИБС было показано, что пациенты с выраженной ишемией имеют гораздо больше ВЧ-компонентов в электрокардиограмме, чем здоровые.
Кроме того, регистрировались ЧСС и контрольная ЭКГ кардиографом «Кардиотехника–8» по стандартной методике в стандартных отведениях I, II, III.
Анализ аритмий. Анализ частоты возникновения и тяжести ишемических и реперфузионных желудочковых тахиаритмий (ЖТА) проводился в соответствии с международным соглашением Lambeth Conventions [9], представляющем собой инструкции по трактовке и учету экспериментально индуцированных нарушений ритма. Механическая и электрическая дефибрилляция, а также какие–либо антиаритмические препараты для купирования возникающих ишемических и реперфузионных нарушений ритма в данном исследовании не применялись.
Методика определения размера анатомической зоны риска и зоны инфаркта. С целью верификации факта возникновения ишемии миокарда в отдельной серии острых экспериментов (n=5), а также для количественной оценки воспроизводимости результатов, проводили оценку размеров анатомической зоны риска и зоны инфаркта с помощью методики «двойного окрашивания» синим Эванса и трифенилтетразолием хлоридом (ТТС) (MP Biomed., США) [10]. В указанной серии экспериментов продолжительность ишемии составляла 30 минут, а реперфузии – 90 минут. Данные по размерам зоны риска и инфаркта представляли в виде отношения объема зоны риска к общему объему сердца, а также в виде отношения объема зоны инфаркта к объему зоны риска (в процентах).
Обработка данных. Записи ЭКГ для их последующей обработки с целью уменьшения влияния помех и устранения артефактов, а также для вычисления спектральных плотностей мощности составляющих ЭКС в НЧ- и ВЧ-каналах обрабатывались с помощью программных пакетов MatLab и MathCad.
Статистическая достоверность различий функциональных данных в каждой временно́й точке, а также размеры анатомической зоны риска и зоны инфаркта оценивалась с помощью программного пакета SPSS (ANOVA, тест Шеффе). Категориальные данные, в частности, частота возникновения нарушений ритма, сравнивались с помощью теста Фишера. Все функциональные данные выражались в виде «среднее ± стандартное отклонение».
Результаты
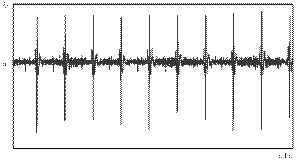
В результате экспериментов были получены ЭКГ-данные в норме и в процессе развития ишемии миокарда. На рис. 3 показаны записи электрокардиограмм животного в нормальном состоянии (до операции) в двух каналах электрокардиографа «СВР-2К» и спектральная плотность мощности ЭКС в ВЧ-канале, рассчитанная в десяти кардиоциклах. При этом были исследованы количественные и

| 
|
| а | б |
| |
| в |
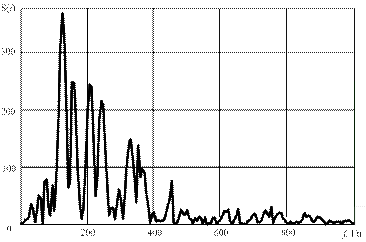
Рис. 3. Примеры ЭКГ-данных животного в норме (до операции): а) в низкочастотном (стандартном) канале; б) в высокочастотном канале; в) спектральная плотность мощности ЭКС в ВЧ-канале
качественные характеристики ЭКС, полученных в серии экспериментов на животных на всех этапах моделирования ишемии-реперфузии миокарда с целью поиска параметров электрокардиограммы (ЭКГ-маркеров), коррелирующих с начальными фазами ишемии для подтверждения наличия диагностически значимых и информативных признаков ишемии в НЧ- и ВЧ-областях спектра ЭКС.
Наступление ишемии миокарда подтверждалась по наличию транзиторного снижения АД, а также по возникновению регионарного цианоза, ишемических изменений на стандартных ЭКГ (элевации сегмента ST) и, иногда, систолического выбухания стенки левого желудочка. На рисунках 4 и 5 приведены репрезентативные записи ЭКГ в трех стандартных отведениях в норме и при острой ишемии миокарда, соответственно.
| I | 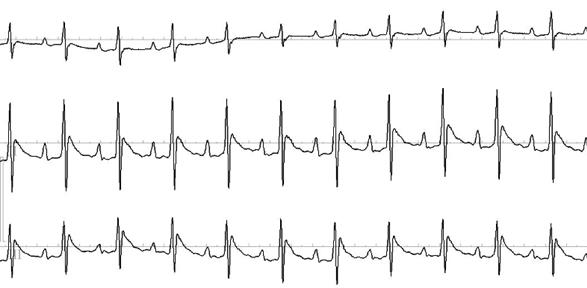
|
| II | |
| III |
Рис. 4. Электрокардиограмма крысы в исходном состоянии (в норме) в стандартных отведениях I, II, III. Скорость записи – 100 мм/с, ЧСС – 420 уд./мин
| I | 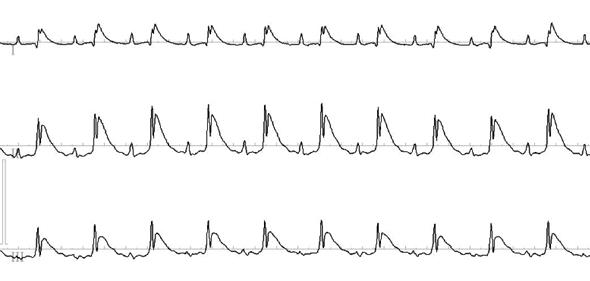
|
| II | |
| III |
Рис. 5. Электрокардиографические признаки острой ишемии миокарда (6-8 минуты после коронароокклюзии): выраженная элевация сегмента ST в I, II, III отведениях
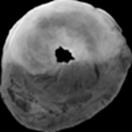
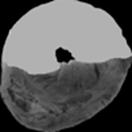
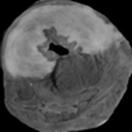
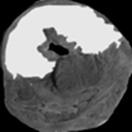
После аутопсии[6] для лучшего отграничения зоны инфаркта от сохранившей жизнеспособность ткани после окраски срезов ТТС в ряде случаев перед фотографированием применяли дополнительную инкубацию срезов в 10%-ном растворе нейтрального формалина. Полученные изображения представлены на рисунке 6. Размер анатомической зоны риска в данных экспериментах составил 42,4±5,6% от общего объема сердца, а размер инфаркта – 62,3±6,5% от объема зоны риска.
| 
| 
| 
|
| а | б | в | г |
Рис. 6. Репрезентативные фотоснимки срезов сердца (контрольная группа, ×7), окрашенные синим Эванса: а – до программного выделения зоны риска; б – после выделения и расчета размера зоны риска и окрашенные трифенилтетразолия хлоридом;
в – до программного выделения зоны инфаркта; г – после выделения и расчета размера зоны инфаркта
Кроме того, по морфологическим и стандартным электрокардиографическим критериям оценивали экспериментальный инфаркт миокарда, развивающийся через 2 недели после коронароокклюзии. Для этого после затягивания лигатуры вокруг ЛКА грудную клетку герметично послойно ушивали: первым рядом швов сближали ребра, второй ряд накладывали на мышцы, третий – на кожу. Верхние дыхательные пути санировали от слизи, после чего трахею ушивали узловым атравматическим швом, а шейный разрез – послойно. Кожные швы обрабатывали 5%-ным раствором йода, в течение 5 дней после операции в целях профилактики гнойных осложнений внутримышечно вводили антибактериальные препараты. Летальность животных в раннем послеоперационном периоде составила 10%, в отдаленном – 25%. Гистологически на 1 сутки обнаруживалась интенсивная лейкоцитарная инфильтрация пограничной зоны, некроз (потеря ядер) кардиомиоцитов в центре инфаркта и некробиотические их изменения в пограничной зоне (причудливая форма ядер, отсутствие продольной и поперечной исчерченности), обширные поля гемо- и плазморрагий. На 10 сутки макроскопически определялся рубец в области переднебоковой стенки ЛЖ, в некоторых случаях захватывавший область верхушки сердца с формированием аневризмы; микроскопически рубец был представлен волокнистой соединительной тканью.
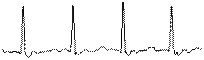
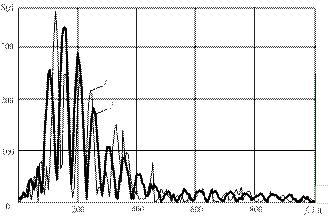
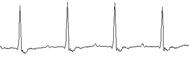
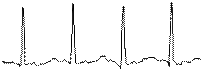
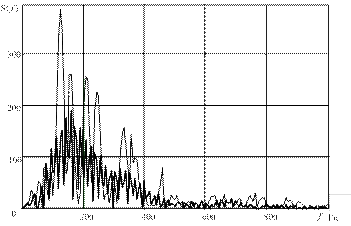
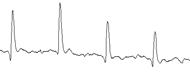
На рис. 7 представлено сравнение электрокардиограмм и спектральных составов ЭКС, полученных до перевязки левой коронарной артерии (в норме) и на различных этапах ишемии миокарда.
|
| ||
| а | |||
| |||
| б | |||
| I – одна минута после торакотомии (рассечения грудной клетки) | |||
|
| ||
| а | |||
| |||
| б | |||
| II – одна минута после перевязки левой коронарной артерии | |||
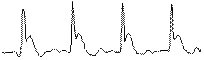
|
| ||
| а | |||
| |||
| б | |||
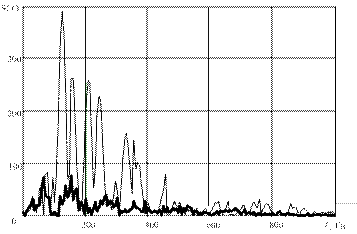
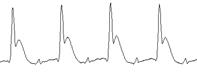
| III – три минуты после перевязки левой коронарной артерии |
Рис. 7. Сравнение ЭКГ-данных на разных этапах экспериментов на животных:
а) ЭКС на выходе низкочастотного канала электрокардиографа сверхвысокого разрешения «СВР-2К»; б) ЭКС на выходе контрольного (стандартного) электрокардиографа; в) спектральная плотность мощности ЭКС в ВЧ-канале «СВР-2К»:
1 – в норме, 2 – на указанном этапе эксперимента
Из сравнения эпюр а и б следует, что сигналы НЧ-канала «СВР-2К» и контрольного (стандартного) электрокардиографа практически идентичны.
В ходе анализа компонентов спектра ЭКС в ВЧ-канале «СВР-2К» в процессе развития ишемии зафиксированы их значительные изменения. С развитием ишемии спектральная плотность мощности ВЧ-составляющих ЭКС существенно снижается. Главным результатом сравнения этих данных является констатация факта, что на первой минуте после перевязки левой коронарной артерии, когда процесс развития ишемии уже начался, в ЭКС на выходах НЧ-каналов обоих электрокардиографов отсутствуют видимые изменения сигналов по сравнению с нормой, а анализ спектрального состава ВЧ-составляющих ЭКС по методу ЭКГ СВР уже фиксирует заметное снижение уровня спектральной плотности мощности ВЧ-компонентов ЭКС. Подобные изменения ЭКГ-данных невозможно зафиксировать с помощью стандартных методов электрокардиографии.
Описанные изменения спектральных характеристик ЭКС воспроизводились у всех животных экспериментальной группы. Полученные результаты могут быть экстраполированы и на другие виды животных, а также на человека, поскольку общие закономерности протекания ишемии едины у всех представителей млекопитающих.
Следует заметить, что уже в ходе данной серии экспериментов раннее обнаружение признаков наступления ишемии нашло практическое применение. В 5-10% случаях перевязки ЛКА происходит неудачное наложение лигатуры, что приводит к потере данного животного для получения адекватных результатов. При отсутствии изменений спектрального состава ВЧ-сигнала, свидетельствующих о наступлении ишемии после первой минуты после коронароокклюзии выполнялась коррекция затягивания лигатуры вокруг ЛКА, что позволило продолжать проведение эксперимента на данном животном.
Заключение
Авторы статьи сформулировали итоги проведенных экспериментальных исследований с технической и медицинской точек зрения.
Экспериментальные исследования на животных подтвердили ранее опубликованные в литературе разрозненные и неконкретные данные о наличии высокочастотных компонентов в ЭКС, а, главное, позволили получить конкретные и однозначные подтверждения их изменений в процессе начала и развития искусственно вызванной ишемии сердца у крыс. Примененный в данной серии экспериментов интегральный, по сути дела, качественный критерий оценки свойств ВЧ-компонентов ЭКС по спектральной плотности их мощности позволяет надежно обнаруживать и фиксировать изменения ВЧ-состава ЭКС на ранних стадиях развития искусственно вызванной ишемии, однако, не дает точных данных об их частотных и временных характеристиках и, хотя предварительные данные об их частотном составе удалось получить, они требуют дополнительных уточнений. Использованная методика, сам ход экспериментов и полученные результаты обозначили необходимость решения задачи как можно более точной фиксации по ЭКГ-параметрам не только начальных стадий вызванной ишемии сердца, но и поиска возможности количественной оценки степени ее развития. Описанные в [15] два других, использованных для анализа экспериментальных записей ЭКС, подхода (методика расчета гистограмм распределений и вейвлет-анализа) не только подтвердили достоверность полученных и приведенных здесь результатов, но и, являются первыми шагами в этом направлении.
Практическая нереализуемость фиксации ЭКС у здорового человека, а затем на различных стадиях многолетнего развития у него кардиозаболевания делает чрезвычайно важной разработку специальных методик экспериментальных исследований ЭКС у подопытных животных на всех этапах быстроразвивающейся искусственно вызванной кардиопатологий для детального изучения и оценивания ЭКГ-характеристик нормальной и патологической электрофизиологии сердца млекопитающих и разработки способов обнаружения, регистрации и описания ЭКГ-признаков этого процесса. Методика, предложенная в данной работе на основе использования метода ЭКГ СВР, является одним из первых шагов на сложном пути решения задачи нахождения ЭКГ-маркеров ИБС человека на ранних стадиях ее развития и разработки новых методик ее диагностики.
К. В. Зайченко
Описанная в данной работе методика моделирования ишемии-реперфузии миокарда дает воспроизводимый результат в виде формирования очага инфаркта миокарда, что подтверждено с помощью электрокардиографических и морфологических критериев как в остром, так и в хроническом эксперименте. Применение метода ЭКГ сверхвысокого разрешения с последующим спектральным анализом в ВЧ-канале позволяет надежно верифицировать признаки ишемии миокарда уже спустя 60 секунд после перевязки коронарной артерии в эксперименте. На данном этапе эксперимента ишемия еще не может быть верифицирована на стандартной ЭКГ с использованием такого критерия, как элевация сегмента ST. Следовательно, использование ЭКГ СВР в перспективе может обеспечить более раннюю диагностику ишемического повреждения миокарда, что имеет большое значение для экспериментальной и клинической практики. Кроме того, наши предварительные исследования показывают, что более подробный анализ ЭКГ-данных, полученных по методу ЭКГ СВР в экспериментах на животных, а также после изучения электрокардиограмм у людей с ИБС на разных стадиях ее развития может позволить получить количественные параметры, коррелирующие с объемом зоны ишемии, а также со степенью адаптации миокарда к ишемии. Последний аспект наиболее интересен с точки зрения дальнейшего изучения и внедрения в клиническую практику, поскольку объективизация степени устойчивости миокарда к ишемии на ранних этапах развертывания ишемического повреждения может влиять на выбор стратегии лечения данного пациента и, следовательно, обеспечить персонификацию лечения инфаркта миокарда.
М. М. Галагудза
Работа выполнена в рамках программы поддержки ведущих научных школ Президента Российской Федерации (№ НШ-3455.2012.8).
Литература
1. Birincioglu M, Yang XM, Critz SD, Cohen MV, Downey JM. S-T segment voltage during sequential coronary occlusions is an unreliable marker of preconditioning. Am J Physiol. 1999. Vol. 2. P. 435-441.
2. К.В. Зайченко, А.В. Зяблицкий, А.И. Краснова, Т.В. Сергеев. От струнного гальванометра до электрокардиографии сверхвысокого разрешения // Биомедицинская радиоэлектроника. 2010. №9. C. 62-78.
3. Гуляев Ю. В., Зайченко К.В. Электрокардиография сверхвысокого разрешения. Задачи. Проблемы. Перспективы // Настоящий сборник.
4. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. Фисенко В. П. М.: Минздрав РФ, ЗАО «ИИА «Ремедиум», 2000.
5. Boyle D., Carson P., Hamer D., High Frequency Electrocardiography in Ischemic Heart Disease. Brit Heart J. 1966. Vol. 28. P. 539–545.
6. Langner, P. H., Jr. (1952). The value of high fidelity electrocardiography using the cathode ray oscillograph and an expanded time scale. Circulation. Vol. 5. P. 249–253.
7. Abboud S., Cohen J., Selwyn A., et al. Detection of transient myocardial ischemia by computer analysis of standard and signal-averaged high-frequency electrocardiograms in patients undergoing percutaneous transluminal coronary angioplasty. Circulation 1987. Vol. 76. P. 585–96.
8. Abboud S. High-frequency electrocardiogram analysis of the entire QRS in the diagnosis and assessment of coronary artery disease. Prog Cardiovasc Dis 1993. Vol.35. P. 311–28.
9. Walker M. J., Curtis M. J., Hearse D. J. et al. The Lambeth Conventions: guidelines for the study of arrhythmias in ischemia, infarction, and reperfusion. Cardiovasc. Res. 1988; 22: 447–455.
10. Галагудза М. М., Некрасова М. К., Сыренский А. В., Нифонтов Е. М. Устойчивость миокарда к ишемии и эффективность ишемического прекондиционирования при экспериментальном сахарном диабете // Российский физиологический журнал им. И. М. Сеченова. 2006. Т. 92. № 3. С. 284–291.
11. Шляхто Е. В., Нифонтов Е. М., Галагудза М. М. Пре- и посткондиционирование как способы кардиоцитопротекции: патофизиологические и клинические аспекты // Сердечная недостаточность. 2008. Т. 9. № 1. C. 4–10.
12. Петрищев Н. Н., Шляхто Е. В., Цырлин В. А., Власов Т. Д., Сыренский А. В., Галагудза М. М. Роль свободных радикалов кислорода в механизмах локального и дистантного ишемического прекондиционирования миокарда // Вестник РАМН. 2006. № 8. С. 10–15.
13. Минасян С. М., Галагудза М. М., Сонин Д. Л., Зверев Д. А., Королёв Д. В., Дмитриев Ю. В., Васильева М. С., Григорова Ю. Н., Власов Т. Д. Методика перфузии изолированного сердца крысы // Регионарное кровообращение и микроциркуляция». – 2009. – Т. 8. – №4(32). – С. 54–59.
14. Selye H., Bajusz E., Grasso S., Mendell P. Simple techniques for the surgical occlusion of coronary vessels in the rat // Angiology. 1960. Vol. 11. № 5. P. 398–407.
Краткие сведения об авторах
Галагудза Михаил Михайлович, доктор медицинских наук, руководитель Института экспериментальной медицины ФГБУ «Федеральный Центр сердца, крови и эндокринологии имени. В. А. Алмазова». Область научных интересов: сердце, ишемия, реперфузия, кардиопротекция, прекондиционирование, посткондиционирование, кардиоплегия. 197341 Санкт-Петербург, ул. Аккуратова, д. 2 тел. +7 (812)499-70-35, e-mail galagoudza@mail.ru.
Зайченко Кирилл Вадимович, доктор технических наук, профессор, заведующий кафедрой медицинской радиоэлектроники Санкт-Петербургского университета аэрокосмического приборостроения, 190000, Санкт-Петербург, Большая Морская ул., 6, тел. +7(812)494-7024, e-mail kvz_k41@aanet.ru
Author’s data
Galagudza Mikhail Mikhailovitch, Doctor of Science (Medicine), head of Institute of Experimental Medicine (Almazov Federal Heart, Blood and Endocrinology Centre). Research interests: the heart, ischemia, reperfusion, cardioprotection, preconditioning, postconditioning, cardioplegia. 2 Akkuratova str., Saint- Petersburg (197341). Phone: +7 (812)499-70-35, e-mail galagoudza@mail.ru.
Zaichenko Kirill Vadimovich, Doctor of Science (Technology), professor, head of the department of medical radioelectronics of St.Petersburg State University of aerospace instrumentation, 190000, St.Petersburg, 67 Bolshaya Morskaya str., tel. +7(812)494-7024, e-mail kvz_41@aanet.ru
[1] – на живом организме.
*(нс) – настоящий сборник
[2] – по желанию.
[3] – управляемый (регулируемый) зазор.
[4] – нарушение проходимости.
[5] – возобновление тока крови.
[6] – посмертное вскрытие и исследование внутренних органов.