Кафедра «Биомедицинские технические системы»
Л.В. Жорина, Г.Н. Змиевской
ИЗУЧЕНИЕ ФОТОДИНАМИЧЕСКОГО ДЕЙСТВИЯ СВЕТА
НА КЛЕТОЧНЫЕ СТРУКТУРЫ
Электронное учебное издание
Методические указания для выполнения лабораторных работ
по курсам «Биофизические основы живых систем» и
«Основы взаимодействия физических полей с биообъектами»
Под редакцией А.В. Самородова
Москва
(С) 2018 МГТУ им. Н.Э. БАУМАНА
УДК 577.3
Рецензент: C. Б. Одиноков
Жорина Л.В.
Ж81 Изучение фотодинамического действия света на клеточные структуры: метод. указания к выполнению лабораторной работы по курсам «Биофизические основы живых систем» и «Основы взаимодействия физических полей с биообъектами» / Л.В. Жорина, Г.Н. Змиевской; под ред. И.Н. Спиридонова. – М.: Изд-во МГТУ им. Н.Э. Баумана, 2014. – 31 с.: ил.
Изложены основные положения теории фотодинамического эффекта, описаны характерные особенности применяемых в клинической практике отечественных фотосенсибилизаторов. Рассмотрена методика определения доз облучения при фотодинамическом воздействии на кровь.
Для студентов старших курсов биомедицинских и биотехнических специальностей.
Рекомендовано учебно-методической комиссией факультета «Биомедицинская техника» МГТУ им. Н.Э. Баумана
Электронное учебное издание
Жорина Лариса Валерьевна
Змиевской Григорий Николаевич
ИЗУЧЕНИЕ ФОТОДИНАМИЧЕСКОГО ДЕЙСТВИЯ СВЕТА
НА КЛЕТОЧНЫЕ СТРУКТУРЫ
© 2018 МГТУ имени Н.Э. Баумана
Введение
Лазерная фотодинамическая терапия — наиболее современный и наименее травматичный метод лечения онкологических заболеваний.
Суть метода состоит в избирательном уничтожении патологических клеток, селективно накопивших специальное вещество — фотосенсибилизатор (ФС), путём воздействия на них излучения с определённой длиной волны. ФС должен обладать рядом специфических свойств, характеризующих его эффективность. Главные из них: селективное накопление в патологических клетках; избирательное и достаточно высокое поглощение излучения на рабочей длине волны облучателя, например, лазера; способность с максимальной эффективностью передавать поглощенную энергию внутриклеточному кислороду и тем самым запускать фотохимические реакции, приводящие к гибели патологических клеток при минимальном воздействии на нормальные клетки. В качестве ФС могут выступать естественные (эндогенные) вещества, участвующие в метаболизме клеток (хлорофилл, порфирин), а также введённые извне. Как ФС для ФДТ используются производные гематопорфирина (ПГП): Фотогем (Россия), Фотофрины I и II (США), Фотосан (ФРГ), а также хлорины, фталоцианины и т.д. В России с 1994 г. разрешен к ограниченному применению синтетический препарат Фотосенс, относящийся к группе фталоцианинов и представляющий собой металлопорфириновый комплекс с участием цинка или алюминия, с 2004 г. — препарат Аласенс на основе 5-аминоливалаланиновой кислоты, с 2006 г — препарат Радахлорин на основе хлорина е 6. ПГП обладает большей селективностью накопления в опухолях, чем чистый гематопрфирин (ГП). Точного химического состава ПГП не имеет, а содержит смесь различных веществ.
Механизм ФДТ еще не изучен до уровня повседневных методических рекомендаций, поэтому каждый медицинский центр, где применяется ФДТ, является одновременно и научным центром. Идет непрерывный поиск и исследование новых, более эффективных, ФС и постоянное совершенствование технических средств (лазерные источники, средства доставки излучения к объекту, средства дозиметрического контроля процесса и управляющие устройства).
Цель работы: приобретение навыков оценки эффективности метода фотодинамического действия света на клеточные структуры на примере наблюдения фотодинамического эффекта (ФДЭ) на взвеси эритроцитов.
После выполнения лабораторной работы студенты смогут:
- на экспериментальном стенде проводить измерения оптической плотности различных прозрачных сред;
- самостоятельно готовить растворы светочувствительного вещества фотосенсибилизатора и суспензии эритроцитов нужной концентрации;
- оценивать дозы начала ФДЭ;
- сравнивать эффективность различных ФС;
- самостоятельно проводить модельные эксперименты по наблюдению ФДЭ.
Краткие сведения из теории
Основным процессом, ответственным за фотодинамический эффект (ФДЭ), можно считать передачу энергии возбуждения от ФС к внутриклеточному кислороду. При поглощении кванта света h ν молекула ФС переходит из основного S 0 в возбужденное S* состояние. Оба эти состояния синглетны, т.е. спины внешних электронов в молекуле ФС антипараллельны, и суммарный спин равен нулю, а спиновое число S = 1 (S = 2 s +1, где s – суммарный спин). Переход S 0 ®S* вследствие этого наиболее вероятен. Ближайшее к S* возбужденное состояние, расположенное чуть ниже, является триплетным (спины внешних электронов параллельны, s = 1 и S = 2s+1 = 3). Оно не может непосредственно заселяться из основного состояния S 0, поскольку действует правило отбора по спину (переход S 0® T* примерно в 104…106 раз менее вероятен, чем S 0® S*). Но ввиду малой разницы энергий S* и T* состояний возможен переход молекулы ФС из S* в T* состояние за счет спин-орбитального взаимодействия, смешивающего состояния с различной спиновой мультиплетностью. Можно найти ряд ФС, у которых вероятность перехода gик из S* в T*, называемого интеркомбинационной конверсией, близка к единице (gик ³ 0,8). Поскольку из-за тех же правил отбора излучательный переход T* ® S 0 запрещен, время жизни триплетного состояния T* много больше (t T* ~ 10-1…10-4 с), чем время жизни синглетного возбуждённого состояния (t S* ~ 10-8… 10-9 с). Происходит, тем самым, накопление молекул ФС в состоянии T*. Этого не могло бы происходить, если бы отсутствовала интерконверсия, и вся поглощенная энергия высвечивалась бы обратно в виде флуоресценции S* ® S 0 (время жизни состояния S* относительно перехода S* ® S 0+ h νфл составляет t s* ~ 10-8…10-9 c). Некоторый очень слабый фон флуоресценции всегда присутствует (gик< 1) и может быть зарегистрирован достаточно чувствительными приемниками излучения.
Поскольку характерной особенностью ФС для ФДТ является преимущественное накопление в опухолевых клетках, повышение интенсивности флуоресценции по сравнению с фоном, характерным для нормальных клеток, является признаком патологии и составляет основу метода люминесцентной диагностики, часто предшествующей ФДТ. Однако легко видеть, что требования к ФС, определяющие его эффективность для терапии и диагностики, противоположны. Для диагностики необходимо, чтобы gик ® 0, для терапии — наоборот, gик ® 1.
Аккумуляция ФС в Т* состоянии делает возможной эффективную передачу энергии возбуждения другим молекулам с образованием свободных радикалов. В данном случае наиболее вероятна передача энергии возбуждения молекуле кислорода. Основное состояние молекулы кислорода 3О2 является триплетным, тогда как ближайшие возбужденные состояния синглетны (1О2*). Наиболее устойчивым из них является состояние 1D g, отстоящее от основного на ~ 0,976 эВ (l = 1,27 мкм). Ввиду различной мультиплетности состояния 1D g и основного 3О2 возможна аккумуляция молекул кислорода в состоянии 1D g.
Характерное время жизни синглетного 1Dg кислорода (1О2*) в жидкой среде сильно зависит от типа среды и может меняться в пределах 1…10-5 с. При наличии в среде возбужденных молекул ФС в состоянии Т*,энергия которого близка к энергии состояния 1D g, весьма вероятно перекрытие электронных оболочек молекул ФС и кислорода с резонансным заселением 1D g состояния кислорода. Этот процесс можно схематически изобразить в виде (см. рис. 1):
T*[][] + 3O2[¯][¯] ® S0[¯][] + 1O2*[][¯]
т.е. электрон с возбужденной орбитали ФС переходит на возбужденную орбиталь 1D g кислорода, а с самой низкой (основной) орбитали кислорода электрон переходит на вакансию в основном состоянии ФС.
Синглетный кислород более активен при взаимодействии с внутриклеточными веществами, чем кислород в основном состоянии 3О2. При этом возможен как физический механизм передачи возбуждения, по типу передачи энергии от ФС к самому кислороду без изменения химического состава, так и химический, при котором кислород вступает в реакцию с соответствующим веществом.
Поскольку в обоих случаях не происходит радиационных переходов, вещества, принимающие энергию возбуждения от синглетного кислорода, называются тушителями. Вещества-тушители всегда присутствуют в клетках и межклеточной среде, нейтрализуя избыточный синглетный кислород. Преобладание физического механизма тушения означает отсутствие фотодинамического эффекта (ФДЭ). Это имеет место в отсутствие ФС, когда синглетный кислород образуется под влиянием естественных факторов (например, при повышенном солнечном облучении). Для реализации же ФДЭ необходимо включение химического механизма тушения, при котором в реакцию с возбужденным 1О2* вступают ненасыщенные соединения, входящие в состав белков и липидов.
Итак, требуемый ФДЭ можно схематически изобразить в виде цепочки реакций:
S 0 + h n 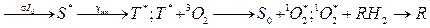 (1)
(1)
Здесь обозначено:
S 0— невозбужденное (синглетное) состояние ФС;
s — эффективное сечение поглощения света молекулой ФС;
I 0— интенсивность падающего излучения [Вт/см2];
S* — возбужденное синглетное состояние ФС;
T* —возбужденное триплетное состояние ФС;
gик— квантовый выход интерконверсии;
3 O 2– невозбужденное (триплетное) состояние молекулы кислорода;
1 O 2*— возбужденное синглетное состояние молекулы кислорода;
RH 2 — химический тушитель (субстрат) — внутриклеточное либо входящее в состав мембран или межклеточной среды вещество, активно взаимодействующее с синглетным кислородом и дающее окисленный продукт R, непосредственно воздействующий на метаболизм клетки с летальным для нее исходом.
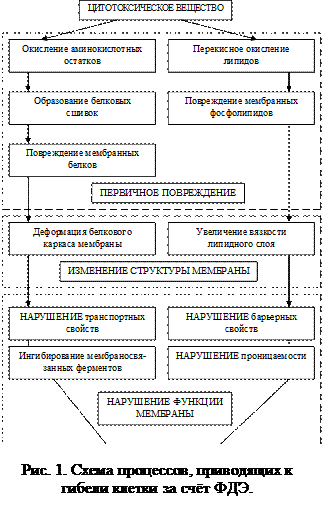
ФДЭ можно ослабить или усилить в присутствии веществ, либо сильно взаимодействующих с синглетным кислородом и тем самым ослабляющих его реакцию с субстратом (ингибиторы), либо нейтрализующих действие физических тушителей, увеличивающих концентрацию субстрата, влияющих на мембранный транспорт (прооксиданты). Наиболее вероятная схема процессов, приводящих к гибели клетки за счет ФДЭ, приведена на рис. 1.
 Возможности метода не ограничиваются онкологией. Имеется ряд интересных сообщений о применениях ФДТ в ряде других областей медицины.
Возможности метода не ограничиваются онкологией. Имеется ряд интересных сообщений о применениях ФДТ в ряде других областей медицины.
Опираясь на данные исследований и практического использования ФДТ, можно в общих чертах сформулировать требования к «идеальному» ФС. Он должен:
— иметь доступный способ получения и обладать постоянным химическим составом;
— быть устойчивым при хранении и введении в организм;
— обладать низкой токсичностью;
— иметь высокую селективность накопления в патологических тканях и сравнительно быстро выводиться из организма;
— слабо накапливаться в коже;
— иметь высокий квантовый выход триплетного состояния;
— иметь возможно более интенсивный максимум в спектре поглощения в области 800-900 нм (область наибольшей прозрачности мягких тканей).
ФС могут быть как растворимы, так и не растворимы в воде (т.е. гидрофильны или гидрофобны). От этого зависит локализация ФС в клетке: в цитоплазме или мембранах, а следовательно и скорость выведения ФС из организма. Гидрофобные ФС в основном локализуются в клеточных мембранах, а гидрофильные путём пиноцитоза попадают в эндосомы и лизосомы. На эффективность ФС сильно влияет агрегация его молекул в воде. Агрегированные молекулы фотохимически не активны, но более липофильны и лучше проникают в клеточные мембраны, где в гидрофобном окружении они могут мономеризоваться и стать активными.
Локализация ФС в клетке также зависит от времени накопления ФС. Гидрофобные ФС накапливаются в мембранах и трудно переходят в водную фазу. В итоге они очень медленно выводится из организма и сохраняются в организме на период более трёх месяцев против двух суток у водорастворимых ФС.
При фотодинамическом воздействии (ФДВ) могут использоваться любые источники света со спектром испускания, соответствующим спектру поглощения ФС, и достаточной мощностью излучения. Возбуждение ФС осуществляется светом определенной длины волны, причем эффективность цитотоксической реакции возрастает с уменьшением ширины полосы поглощения ФС. Идеальным является случай, при котором максимум поглощения ФС совпадает с максимумом спектральной плотности источника света. К сожалению, это на практике удается реализовать далеко не всегда (даже если in vitro желаемое совпадение достигнуто, введение препарата in situ, как правило, изменяет положение максимума поглощения ФС малопредсказуемым образом).