Урок №
Тема: «Альдегиды».
Внимательно изучаем отправленный материал.
Законспектировать.
Выучить определения, формулы альдегидов, запоминать уравнения реакций.
Вещества, в молекулах которых альдегидная группа связана с углеводородным радикалом (или атомом водорода), называют альдегидами. Общая формула альдегидов 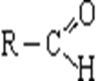

В соответствии с номенклатурой ИЮПАК названия предельных альдегидов образуются от названия алкана с тем же числом атомов углерода в молекуле с помощью суффикса -аль. Например:
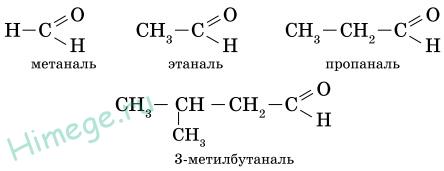
Нумерацию атомов углерода главной цепи начинают с атома углерода альдегидной группы. Поэтому альдегидная группа всегда располагается при первом атоме углерода, и указывать ее положение нет необходимости.
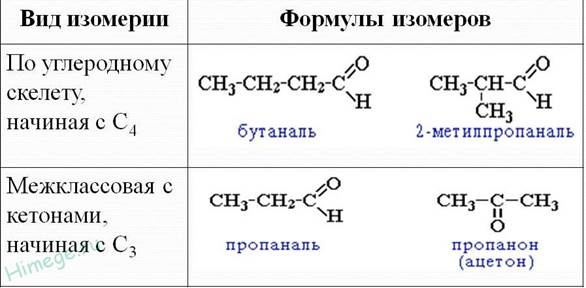
Для альдегидов характерен изомерия углеродного скелета, которая возможна с бутаналя. Межклассовая изомерия (пропаналь и пропанон).
Химические свойства
Реакции восстановления.
Продуктом гидрирования альдегидов являются первичные спирты, кетонов — вторичные спирты. Так, при гидрировании уксусного альдегида образуется этиловый спирт, при гидрировании ацетона — пропанол-2.
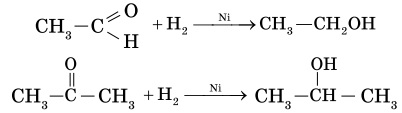
2. Реакции окисления. Альдегиды способны не только восстанавливаться, но и окисляться. При окислении альдегиды образуют карбоновые кислоты.
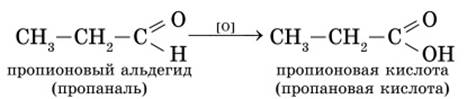
Окисление кислородом воздуха. Например, из пропионового альдегида (пропаналя) образуется пропионовая кислота:
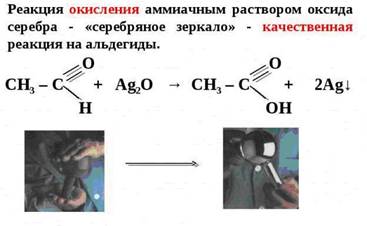
Если поверхность сосуда, в котором проводится реакция, была предварительно обезжирена, то образующееся в ходе реакции серебро покрывает ее тонкой ровной пленкой. Получается замечательное серебряное зеркало. Поэтому эту реакцию называют реакцией «серебряного зеркала». Ее широко используют для изготовления зеркал, серебрения украшений и елочных игрушек.
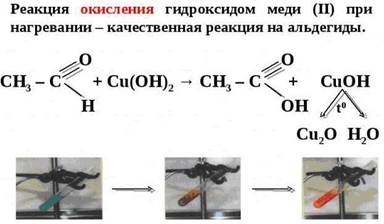
В результате реакции выпадает осадок меди (I) кирпично-красного цвета.
При изготовлении многих отделочных материалов (древесностружечных плит, искусственного камня, звуко- и теплоизоляционных материалов), предметов быта используют полимерные вещества, получаемые на основе органического вещества под названием формальдегид.
Взаимодействием формальдегида с фенолом синтезируют фе- нолоформальдегидную смолу. При растворении ее в спирте или ацетоне получают лаки. Можно пропитать этим веществом стружки и опилки и спрессовать при нагревании — получится древесностружечная плита. Если оклеить такую плиту бумагой с рисунком под дерево или камень, получится прекрасный материал для изготовления мебели. Кроме того, в фенолоформальдегидную смолу добавляют различные цветные наполнители, помещают в форму и нагревают. Так получают устойчивые к высоким температурам изделия из полимерного материала — фенопласта.
Аналогично реакцией формальдегида с мочевиной получают карбамидную смолу, а из нее — твердый полимерный материал аминопласт.
По агрегатному состоянию формальдегид — газ. Как же его заставляют реагировать с твердым фенолом? Формальдегид хорошо растворим в воде, и взаимодействие осуществляют в растворе. Водный раствор формальдегида называют формалин. Он обладает способностью свертывать белок, на этом основано его применение в кожевенном производстве. В результате дубильного действия формалина кожа твердеет и не подвергается гниению. На этом же свойстве основано его применение для хранения биологических препаратов, дезинфекции и протравливания семян.
Лабораторная работа по теме «Альдегиды»
Цель: Изучить реакции окисления, характерные для альдегидов,
научиться проводить качественные реакции;
закрепить навыки работы с лабораторным оборудованием;
развивать аккуратность через оформление навыков, наблюдательность,умение общаться, уважение друг к другу через работу в парах.
Оборудование: нитрат серебра, сульфат меди (II), гидрооксид натрия, раствор формалина, аммиачная вода, прибор для нагревания, пробирки.
Правила техники безопасности:
1. Соблюдать правила пожарной безопасности при работе с сухим горючим.
2. Не пробовать реактивы на вкус.
3. Выполнять только опыты, предусмотренные работой.
4. При попадании реактивов на кожные покровы смыть большим количеством воды.
Ход работы
Опыт №1
Взаимодействие формальдегида с аммиачным раствором серебра – реакция «серебряного зеркала»
1.В пробирку налейте 1 мл раствора нитрата серебра и столько же водного раствора аммиака.
2. Затем прилейте 1,5 – 2 мл раствора формалина (формальдегида).
3.Пробирку с полученным раствором медленно нагрейте, не доводя до кипения, до образования на стенках блестящего налета.
Наблюдения и уравнения реакций запишите и сделайте вывод о проделанной работе.
Опыт №2
Окисление метаналя гидроксидом меди (II)
1.Налейте в пробирку 1 мл раствора этаналя и столько же раствора гидроксида натрия.
2. Затем добавьте несколько капель раствора сульфата меди (II). Пробирку с полученным раствором нагрейте. Что наблюдаете?
3.Напишите уравнение реакции между сульфатом меди (II) и гидроксидом натрия. Напишите уравнение реакции взаимодействия этаналя с полученным раствором гидроксидом меди (II).