ОПЫТ 1. ОБРАЗОВАНИЕ КАЛИЯ ГИДРОТАРТРАТА И КАЛИЯ ТАРТРАТА.
 В пробирку поместите 0,5г кристаллов винной кислоты, растворите в воде, прилейте 2-3 капли раствора хлорида калия, 1 мл этанола, 2 мл ацетата натрия. Что наблюдаете? Назовите осадок, запишите наблюдения, уравнения реакций. Полученный осадок гидротартрата калия разделите на две пробирки. В первую пробирку налейте избыток раствора гидроксида калия (или натрия), хорошо перемешайте. Запишите наблюдения, уравнения реакций, вывод.
В пробирку поместите 0,5г кристаллов винной кислоты, растворите в воде, прилейте 2-3 капли раствора хлорида калия, 1 мл этанола, 2 мл ацетата натрия. Что наблюдаете? Назовите осадок, запишите наблюдения, уравнения реакций. Полученный осадок гидротартрата калия разделите на две пробирки. В первую пробирку налейте избыток раствора гидроксида калия (или натрия), хорошо перемешайте. Запишите наблюдения, уравнения реакций, вывод.
ОПЫТ 2. ДОКАЗАТЕЛЬСТВО НАЛИЧИЯ ГИДРОКСИЛЬНЫХ ГРУПП В ВИННОЙ КИСЛОТЕ.
 В пробирку налейте 1 мл раствора гидроксида натрия, 3-4 капли
В пробирку налейте 1 мл раствора гидроксида натрия, 3-4 капли
раствора сульфата меди (II). Запишите наблюдения. В эту же пробирку поместите 0,5г кристаллов винной кислоты, хорошо перемешайте. Запишите наблюдения, уравнения реакций, вывод.
 ОПЫТ 3. ПОЛУЧЕНИЕ ЖИДКОСТИ ФЕЛИНГА И ПРОВЕРКА ЕЕ ОКИСЛИТЕЛЬНЫХ СВОЙСТВ.
ОПЫТ 3. ПОЛУЧЕНИЕ ЖИДКОСТИ ФЕЛИНГА И ПРОВЕРКА ЕЕ ОКИСЛИТЕЛЬНЫХ СВОЙСТВ.
Получение: в пробирку налейте 1 мл раствора гидроксида натрия, 3-4 капли раствора сульфата меди (II). Перемешайте. Запишите наблюдения. В эту же пробирку поместите несколько кристалликов сегнетовой соли, хорошо перемешайте. Запишите наблюдения, уравнения реакций, вывод.
 Проверка окислительных свойств: содержимое пробирки разделите на две части. В первую пробирку прилейте альдегид и нагрейте. Запишите наблюдения, уравнение реакции, вывод.
Проверка окислительных свойств: содержимое пробирки разделите на две части. В первую пробирку прилейте альдегид и нагрейте. Запишите наблюдения, уравнение реакции, вывод.
 ОПЫТ 4. КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ЛИМОННУЮ КИСЛОТУ И ЕЕ СОЛИ.
ОПЫТ 4. КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ЛИМОННУЮ КИСЛОТУ И ЕЕ СОЛИ.
В пробирку поместите 0,5г кристаллов цитрата натрия, растворите его в воде, прилейте раствор хлорида кальция и нагрейте. Запишите наблюдения, уравнение реакции, вывод, латинское название натрия цитрата.
ОПЫТ 5. ПРОВЕРКА РАСТВОРИМОСТИ САЛИЦИЛОВОЙ КИСЛОТЫ.


ВНИМАНИЕ – ФИЗИЧЕСКИЙ ПРОЦЕСС! Рассмотрите порошок салициловой кислоты. Определите цвет, структуру, запах порошка. Проверьте растворимость салициловой кислоты в холодной и горячей воде, в спирте, в щелочи. Для этого необходимо взять по 0,1 г порошка и 1-2 мл растворителя. Результаты проверок растворимости опишите.
ОПЫТ 6. ВЗАИМОДЕЙСТВИЕ САЛИЦИЛОВОЙ КИСЛОТЫС ХЛОРИДОМ ЖЕЛЕЗА (III).
 0,1 г салициловой кислоты растворите в 2 мл воды. К полученному раствору прибавьте 0,5 мл раствора хлорида железа (III). Содержимое пробирки разделить на три части: в одну добавьте несколько капель разбавленной уксусной кислоты, в другую - несколько капель разбавленной соляной кислоты. Напишите уравнения реакций.
0,1 г салициловой кислоты растворите в 2 мл воды. К полученному раствору прибавьте 0,5 мл раствора хлорида железа (III). Содержимое пробирки разделить на три части: в одну добавьте несколько капель разбавленной уксусной кислоты, в другую - несколько капель разбавленной соляной кислоты. Напишите уравнения реакций.
ОПЫТ 7. ПОЛУЧЕНИЕ САЛИЦИЛОВОЙ КИСЛОТЫ.
0,2 г салицилата натрия растворите в 2 мл воды, добавьте небольшими порциями хлороводородную кислоту. Напишите уравнение реакции.
ОПЫТ 8. ГИДРОЛИЗ АЦЕТИЛСАЛИЦИЛОВОЙ КИСЛОТЫ.
В пробирку поместите несколько кристалликов ацетилсалициловой кислоты и добавьте 1 мл воды. Разделите раствор на две пробирки. В одну добавьте 1 каплю раствора хлорида железа (III).
 + FeC13è реакция не идет. Почему?
+ FeC13è реакция не идет. Почему?
Раствор во второй пробирке прокипятите в течение 30 сек. на небольшом пламени в присутствии концентрированной серной кислоты.

охладите и прибавьте 1 каплю раствора хлорида железа (III).

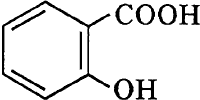 + FeC13è комплекс фиолетового цвета
+ FeC13è комплекс фиолетового цвета
3 СН3СООН + FeC13è (СН3СОО)3Fe + 3 НС1
красно-бурый раствор
Опишите наблюдения. Напишите уравнения реакций.