Термины вольтамперометрия и амперометрия относятся к методам, при которых на клеммы электродов электрохимической ячейки накладывается изменяющийся потенциал; при этом в ячейке имеются так называемые электроактивные (то есть способные к окислению или восстановлению) соединения, а проводимость внутри ячейки обеспечивается индифферентным, или поддерживающим, электролитом.
Ток через ячейку постоянно измеряется, в результате чего возникает кривая зависимости тока от наложенного потенциала, которую называют вольтамперограммой.
Наиболее простой вариант метода- это волътамперометрия с линейной разверткой потенциала. Типичная вольтамперограмма показана на рисунке.
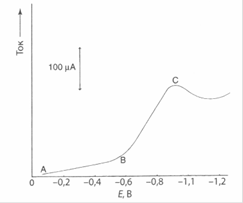
В начале кривой (точка А) ток небольшой. Между точками А и В очень медленный подъем кривой обусловлен остаточным (или примесным) током и зарядкой двойного слоя на границе электрода с раствором. Этот ток иногда называют фоновым. В точке В наложенный потенциал приближается к потенциалу восстановления частиц, находящихся в окисленном состоянии (Ох). При дальнейшем увеличении потенциала электроны с возрастающей скоростью переходят с электрода на Ох в соответствии со следующим уравнением реакции:
Все возрастающая скорость восстановления приводит к увеличению тока через ячейку. Можно показать, что общий ток через ячейку в этой области кривой слагается из катодного тока, или тока восстановления (г'с), и анодного тока.
По мере увеличения наложенного потенциала Е возрастает iс и падает ia, что и вызывает наблюдаемый подъем вольтамперометрической волны. Однако этот подъем не бесконечен: концентрация Ох в приэлектродном пространстве падает за счет его восстановления, а скорость Ох из раствора к электроду ограничена. В результате в точке С ток достигает своего пикового значения (рис. 2.9).
Влияние скорости диффузии Ох на величину диффузионного тока id определяется первым законом диффузии Фика, согласно которому:
Поток вещества к поверхности электрода = dN/dt = D dC/dx,
Второй закон диффузии Фика описывает уменьшение концентрации вещества в данной точке пространства во времени.
В приведенных выше уравнениях С — это концентрация вещества (например, Ox), N - его количество в молях, D — коэффициент диффузии, а х — расстояние от поверхности электрода.
Кондуктометрия
Кондуктометрия основана на измерении электропроводности раствора и применяется для определения концентрации солей, кислот, оснований и т.д. При кондуктометрических определениях обычно используют электроды из одинаковых материалов, а условия их проведения подбирают таким образом, чтобы свести к минимуму вклад скачков потенциала на обеих границах раздела электрод/электролит (например, используют переменный ток высокой частоты). В этом случае основной вклад в измеряемый потенциал ячейки вносит омическое падение напряжения IR, где R – сопротивление раствора. Электропроводность однокомпонентного раствора можно связать с его концентрацией, а измерение электропроводности электролитов сложного состава позволяет оценить общее содержание ионов в растворе и применяется, например, при контроле качества дистиллированной или деионизованной воды. В другой разновидности кондуктометрии – кондуктометрическом титровании – к анализируемому раствору порциями добавляют известный реагент и следят за изменением электропроводности. Точка эквивалентности, в которой отмечается резкое изменение электропроводности, определяется из графика зависимости этой величины от объема добавленного реагента.
Потенциометрия
Потенциометрия применяется для определения различных физико-химических параметров исходя из данных о потенциале гальванического элемента. Электродный потенциал в отсутствие тока в электрохимической цепи, измеренный относительно электрода сравнения, связан с концентрацией раствора уравнением Нернста. В потенциометрических измерениях широко применяются ионоселективные электроды, чувствительные преимущественно к какому-то одному иону в растворе: стеклянный электрод для измерения рН и электроды для селективного определения ионов натрия, аммония, фтора, кальция, магния и др. В поверхностный слой ионоселективного электрода могут быть включены ферменты, и в результате получается система, чувствительная к соответствующему субстрату. Отметим, что потенциал ионоселективного электрода определяется не переносом электронов, как в случае веществ с электронной проводимостью, а в основном переносом или обменом ионов. Однако уравнение Нернста, связывающее электродный потенциал с логарифмом концентрации (или активности) вещества в растворе, применимо и к такому электроду. При потенциометрическом титровании реагент добавляют в анализируемый раствор порциями и следят за изменением потенциала. S-образные кривые, характерные для такого типа титрования, позволяют определить точку эквивалентности и найти такие термодинамические параметры, как константа равновесия и стандартный потенциал.
Амперометрия
Амперометрия. Метод основан на измерении предельного диффузионного тока, проходящего через раствор при фиксированном напряжении между индикаторным электродом и электродом сравнения. При амперометрическом титровании точку эквивалентности определяют по излому кривой ток – объем добавляемого рабочего раствора. Хроноамперометрические методы основаны на измерении зависимости тока от времени и применяются в основном для определения коэффициентов диффузии и констант скорости. По принципу амперометрии (как и вольтамперометрии) работают миниатюрные электрохимические ячейки, служащие датчиками на выходе колонок жидкостных хроматографов. Гальваностатические методы аналогичны амперометрическим, но в них измеряется потенциал при прохождении через ячейку тока определенной величины. Так, в хронопотенциометрии контролируется изменение потенциала во времени. Эти методы применяются главным образом для изучения кинетики электродных реакций.
Кулонометрия
В кулонометрии при контролируемом потенциале проводят полный электролиз раствора, интенсивно перемешивая его в электролизере с относительно большим рабочим электродом (донная ртуть или платиновая сетка). Полное количество электричества (Q, Кл), необходимое для электролиза, связано с количеством образующего вещества (А, г) законом Фарадея:
A=QM/nF
Кулонометрическое титрование заключается в том, что при постоянном токе электролитически генерируют реактив, вступающий во взаимодействие с определяемым веществом. Ход титрования контролируют потенциометрически или амперометрически. Кулонометрические методы удобны тем, что являются по своей природе абсолютными (т.е. позволяют рассчитать количество определяемого вещества, не прибегая к калибровочным кривым) и нечувствительны к изменению условий электролиза и параметров электролизера (площади поверхности электрода или интенсивности перемешивания). При кулоногравиметрии количество вещества, подвергшегося электролизу, определяют взвешиванием электрода до и после электролиза.-где M – мол. масса (г/моль), F. Существуют и другие электроаналитические методы. В переменно-токовой полярографии на линейно меняющийся потенциал налагают синусоидальное напряжение малой амплитуды в широкой области частот и определяют либо амплитуду и фазовый сдвиг результирующего переменного тока, либо импеданс. Из этих данных получают информацию о природе веществ в растворе и о механизме и кинетике электродных реакций. В тонкослойных методах используются электрохимические ячейки со слоем электролита толщиной 10–100 мкм. В таких ячейках электролиз идет быстрее, чем в обычных электролизерах. Для изучения электродных процессов применяют спектрохимические методы со спектрофотометрической регистрацией. Для анализа веществ, образующихся на поверхности электрода, измеряют поглощение ими света в видимой, УФ- и ИК-областях. За изменением свойств поверхности электрода и среды следят с помощью методов электроотражения и эллипсометрии, которые основаны на измерении отражения излучения от поверхности электрода. К ним относятся методы зеркального отражения и комбинационного рассеяния света (рамановская спектроскопия), спектроскопия второй гармоники (фурье-спектроскопия).
Заключение
На сегодняшний день электроаналитические методы определения веществ – одни из самых перспективных в аналитической химии. Это связано прежде всего с их чувствительностью и возможностью определять малые концентрации ионов. Тем не менее есть и недостатки, среди которых следует отметить достаточную дороговизну оборудования и необходимость использования вспомогательных средств измерения. Однако на сегодняшний день не существует другого метода способного видеть 10-9-10-8 концентрации ионов. В связи с этим эти методы остаются перспективными и многообещающими для исследований в аналитической химии. Именно поэтому следует изучать теоретические основы методов и принципы их работы. В своем реферате я постарался раскрыть принципы только самых основных и известных электроаналитических методов. Но наука не стоит на месте и методы совершенствуются им на смену приходят новые более совершенные и чувствительные.
Литература
1. Виноградова Е.Н., Галлай З.А., Финогенова З.М. Методы полярографического и амперометрического анализа. М., изд-во МГУ, 1999
2. Рейшахрит Л.С. Электрохимические методы анализа. Ленинград, изд-во ЛГУ, 1998
3. Зозуля А.П. Кулонометрический метод анализа М. Химия, 2000
4. Выдра Ф., Штулик К., Юлакова Э Инверсионная вольтамперометрия. М. Мир, 2007, 278 с.
5. Камман К. Работа с ионселективными электродами. М.,Изд-во "Мир",. 1999, 283 с.
6. Ф. Штольц «Электроаналитические методы», Москва, 2006