Кроме коэффициента β затухание характеризуют и другими величинами:
1. Время релаксации τ — это промежуток времени, за который амплитуда затухающих колебаний уменьшается в е раз. Из выражения а = а 0е-β t видно, что
 =
= 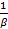 (13)
(13)
Интервал времени τ называют также постоянной времени осциллятора. Это оценка времени, в течение которого продолжается процесс свободных колебаний осциллятора, выведенного из положения равновесия. Разумеется, по истечении времени колебания продолжаются, но амплитуда, спадая по экспоненциальному закону, становится столь малой, что практически можно полагать, что колебания прекратились (скажем, через промежуток времени 5/βамплитуда падает более чем в 100 раз).
2. Логарифмический декремент затухания. Его определяют, как
 , (14)
, (14)
Где: Т — период затухающих колебаний.
Логарифмический декремент затухания λ показывает, насколько изменяется амплитуда колебаний за один период. Например, при λ = 0,01 амплитуда колебаний изменяется за 1 период приблизительно на 1%. Из формул (13) и (14) следует, что
λ= =  , (15)
, (15)
где N e — число колебаний за время τ, в течение которого амплитуда уменьшается в е раз.
3. Добротность осциллятора. По определению при малых значениях логарифмического декремента:
Q =  =π N e (16)
=π N e (16)
Эту величину применяют для характеристики чувствительности колебательной системы к резонансным воздействиям. Из (16) следует, что добротность пропорциональна числу колебаний N e, совершаемых системой за время релаксации.
В заключение отметим, что анализ формулы (10) приводит к выводу: затухающие колебания возможны при условии β < ω0. Хотелось бы обратить внимание, что при увеличении коэффициента затухания β период затухающих колебаний будет расти, и при β = ω0 система будет совершать апериодическое движение: выведенная из положения равновесия, она возвращается в это положение, не совершая колебаний.
ВОПРОС 13
Волна — изменение состояния среды или физического поля (возмущение), распространяющееся либо колеблющееся в пространстве и времени или в фазовом пространстве.
Поперечная волна - волна, в которой частицы среды перемещаются перпендикулярно направлению распространения волны.
Продольная волна - волна, в которой движение частиц среды происходит вдоль направления распространения волны.
Бегущая волна — волновое движение, при котором поверхность равных фаз (фазовые волновые фронты) перемещается с конечной скоростью (постоянной для однородной среды).
Стоя́чая волна́ —колебания в распределённых колебательных системах с характерным расположением чередующихся максимумов)и минимумов амплитуды
Длина волны
Минимальное расстояние, на которое распространяется волна за время, равное периоду колебания точки среды около положения равновесия, называется длиной волны.
Фазовая скорость 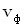 - это скорость распространения данной фазы колебаний, т.е. скорость волны.
- это скорость распространения данной фазы колебаний, т.е. скорость волны.
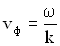 .
.
Геометрическое место точек, до которого к некоторому моменту времени дошел колебательный процесс, называется волновым фронтом.
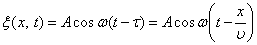 (1) – это уравнение плоской волны.
(1) – это уравнение плоской волны.
Таким образом, x есть смещение любой из точек с координатой x в момент времени t. При выводе мы предполагали, что амплитуда колебания 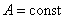 . Это будет, если энергия волны не поглощается средой.
. Это будет, если энергия волны не поглощается средой.
Уравнение (1) может принять семеричный вид относительно времени t и смещения x.
Для этого вводится понятие  , модуль волнового вектора показывает, сколько λ волн укладывается в длину 2
, модуль волнового вектора показывает, сколько λ волн укладывается в длину 2  , сам вектор направлен нормально к волновой поверхности, тогда:
, сам вектор направлен нормально к волновой поверхности, тогда:

 (1)
(1)

Если волна распространяется произвольно, ее направление фиксируется углами  , по отношению кOxyz, то уравнение волны можно записать так:
, по отношению кOxyz, то уравнение волны можно записать так:
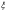



Где 
ВОПРОС 14
Наложение упругих волн.Стоячая волна и её особенности
Упругие волны — это возмущения, распространяющиеся в твердой, жидкой и газообразной средах благодаря действию в них сил упругости.
Сами эти среды называют упругими. Возмущение упругой среды — это любое отклонение частиц этой среды от своего положения равновесия.
особенности
Если в среде распространяются одновременно несколько волн, то колебания частиц среды оказываются геометрической суммой колебаний, которые совершали бы частицы при распространении каждой из волн в отдельности. Следовательно, волны просто накладываются одна на другую, не возмущая друг друга. Это утверждение называется принципом суперпозиции волн. Принцип суперпозиции утверждает, что движение, вызванное распространением сразу нескольких волн, есть снова некоторый волновой процесс.
Каждая стоячая волна обладает следующими свойствами. Вся область пространства, в которой возбуждена волна, может быть разбита на ячейки таким образом, что на границах ячеек колебания полностью отсутствуют. Точки, расположенные на этих границах, называются узлами стоячей волны. Фазы колебаний во внутренних точках каждой ячейки одинаковы. Колебания в соседних ячейках совершаются навстречу друг другу, то есть в противофазе. В пределах одной ячейки амплитуда колебаний изменяется в пространстве и в каком-то месте достигает максимального значения. Точки, в которых это наблюдается, называются пучностями стоячей волны. Наконец, характерным свойством стоячих волн является дискретность спектра их частот. В стоячей волне колебания могут совершаться только со строго определенными частотами, и переход от одной из них к другой происходит скачком.
ВОПРОС 15
Интервал в теории относительности — расстояние между двумя событиями в пространстве-времени, являющееся довольно прямым обобщением евклидовского расстояния между двумя точками — на пространство-время (определение см. ниже). Интервал лоренц-инвариантен, то есть не меняется при переходе от одной инерциальной системы отсчёта к другой, или, говоря иначе, является инвариантом (скаляром) в специальной и общей теории относительности.
Это свойство интервала делает его фундаментальным понятием, на основе которого может, в соответствии с принципом относительности, быть осуществлена ковариантная формулировка физики (то есть формулировка, законы которой записываются одинаково в любой инерциальной системе отсчета), и роль интервала при этом почти столь же велика, как роль обычного расстояния в обычной (евклидовской или римановой) геометрии.
В частности, преобразования Лоренца (преобразования координат, включая время, оставляющие неизменной запись всех фундаментальных уравнений физики при замене системы отсчета) могут быть формально найдены как группа преобразований, сохраняющих инвариантным интервал.
Инвариантность интервала послужила основой для введения пространства Минковского, в котором смене инерциальных систем отсчёта соответствуют «вращения» этого пространства, что явилось по сути, видимо, первой явной формулировкой концепции пространства-времени.
Понятие интервала лежит в основе специальной и общей теорий относительности (и важно в теориях, так или иначе включающих их в себя).

Иногда, особенно при абстрактном изложении, слово 'интервал' может заменяться просто словом 'расстояние' или 'длина 



ВОПРОС 16
Релятивистский импульс
Уже на нашей памяти закон сохранения импульса претерпел некоторые изменения. Они, однако, не коснулись самого вакона как такового, просто изменилось понятие импульса. В теории относительности, как оказалось, импульс уже не сохраняется, если его понимать так же, как и прежде. Дело в том, что масса не остается постоянной, а изменяется в зависимости от скорости, а потому изменяется и импульс. Это изменение массы происходит по закону

|
где m0— масса покоящегося тела, с — скорость распространения света. Из этой формулы видно, что при обычных скоростях (если v не очень велико) m очень мало отличается от m0, а импульс поэтому с очень хорошей точностью выражается старой формулой.
Компоненты импульса для одной частицы можно записать в виде

|
где v2 = v2x + v2y + v2z. Если просуммировать x-компоненты импульсов всех взаимодействующих частиц, то эта сумма как до столкновения, так и после окажется одной и той же. Это и есть закон сохранения импульса в направлении оси х. То же можно сделать и в любом другом направлении.
В гл. 4 мы уже видели, что закон сохранения энергии неверен, если мы не признаем эквивалентности энергии во всех ее формах, т. е. электрической энергии, механической энергии, энергии излучения, тепловой и т. д. Про некоторые из этих форм, например тепло, можно сказать, что энергия «скрыта» в них. Напрашивается вопрос: а не существуют ли также «скрытые» формы импульса, скажем «тепловой импульс»? Дело в том, что импульс утаить невозможно; скрыть его очень трудно по следующим причинам.
Мера тепловой энергии — случайного движения атомов тела — представляет собой просуммированные квадраты их скоростей. В результате получается некоторая положительная величина, не имеющая направленного характера. Так что тепло как бы заключено внутри тела независимо от того, движется ли оно как целое или нет. Поэтому сохранение энергии в тепловой форме не очень очевидно. С другой стороны, если мы просуммируем скорости, которые имеют направление, и в результате получим не нуль, то это означает, что само тело целиком движется в некотором направлении, а такое макродвижение мы уже способны наблюдать. Так что никакой случайной внутренней потери импульса не существует: тело обладает определенным импульсом, только когда оно движется целиком. В этом и состоит основная причина того, что импульс трудно скрыть. Но тем не менее скрыть его все же можно, например в электромагнитное поле. Это еще одна из особенностей теории относительности.
Ньютон считал, что взаимодействие на расстоянии должно быть мгновенным. Но это, оказывается, неверно. Возьмем, например, электрические силы. Пусть электрический заряд, расположенный в некоторой точке, вдруг начинает двигаться, тогда его действие на другой заряд в другой точке не будет мгновенным: существует небольшое запаздывание. При таком положении, даже если силы действия и противодействия равны между собой, импульсы не будут компенсироваться. Существует небольшой промежуток времени, в течение которого будет происходить нечто странное; в то время как первый заряд испытывает какое-то воздействие силы и реагирует на нее изменением своего импульса, второй стоит как ни в чем не бывало и не изменяет импульса. На передачу влияния второму заряду через разделяющее их расстояние требуется некоторое время: «влияние» распространяется не мгновенно, а с некоторой конечной (хотя и очень большой) скоростью 300 000 км/сек. В течение этого крохотного промежутка времени импульс частиц не сохраняется. Но, разумеется, после того как второй заряд испытает влияние первого, импульсы компенсируются, наступает полный порядок, но все-таки в течение некоторого момента закон был нарушен. Мы представляем дело таким образом, что в течение этого интервала существует импульс другого рода, чем импульс частиц mv, и это импульс электромагнитного поля. Если сложить его с импульсами частиц, то эта сумма в любой момент сохраняется. Однако тот факт, что электромагнитное поле может обладать импульсом и энергией, делает его реальностью, а утверждение о том, что между частицами действуют силы, переходит в утверждение о том, что частица создает поле, которое в свою очередь действует на другую частицу. Само же поле имеет многие свойства, аналогичные частицам; оно может нести энергию и импульс. Для иллюстрации рассмотрим еще один пример; в электромагнитном поле могут существовать волны, которые мы называем светом. И вот оказывается, что свет тоже несет какой-то импульс, так что когда он падает на предмет, то передает ему некоторое количество своего импульса. Это эквивалентно действию какой-то силы, ведь освещенный предмет изменяет свой импульс, как будто на него действует некоторая сила. Итак, падая на предмет, свет оказывает на него давление. Хотя это давление очень мало, но достаточно тонкими приборами его все же можно измерить.
Оказывается, что в квантовой механике импульс тоже не mv, а нечто совсем другое. Здесь уже трудно определить точно, что же такое скорость частицы, но импульс все-таки существует. Разница же состоит в том, что когда частицы действуют как частицы, то их импульс по-прежнему mv, но когда они действуют как волны, то импульс уже измеряется числом волн на 1 см: чем больше волн, тем больше импульс. Однако, несмотря на это различие, закон сохранения импульса справедлив и в квантовой механике. Неверными оказались уравнение Ньютона f = ma и все его выводы закона сохранения импульса, тем не менее в квантовой механике в конце концов этот закон продолжает действовать!
ВОПРОС 17
Макросистемой называют систему, имеющую массу, сравнимую с массой окружающих нас тел и состоящую из очень большого числа микрочастиц (атомов и молекул). Например, в одном моле вещества содержится N A = 6,02.1023 молекул, а масса одного моля воздуха всего 29 грамм при объёме 22,4 литра при нормальных условиях.
Для описания макросистем используют два метода: статистический и термодинамический. В дальнейшем вместо термина макросистема иногда будем использовать термин термодинамическая система.
Статистический метод основывается на применении законов теории вероятностей для получения функции распределения физической величины. Данный метод включает в себя:
А). статистическую физику равновесных состояний (для описания состояния макросистемы, если функция распределения не зависит от времени);
Б ). кинетическое описание макросистемы, позволяющее получить на основе уравнений динамики микрочастиц решения для целого ряда практически важных задач для процессов в газе, плазме и различных конденсированных средах, а также описывать необратимые процессы;
В). г идродинамическое описание макросистемы, позволяющее составить уравнения для средних значений динамических параметров среды (скорости течения, температуры, плотности и т.д.). В эти уравнения входят коэффициенты переноса (вязкости, теплопроводности, диффузии).
Термодинамический метод заключается в описании поведения систем с помощью основных постулатов (начал термодинамики), справедливость которых подтверждается только опытным путём. Данный метод включает в себя:
А). равновесную термодинамику, которая достаточно точно описывает большинство окружающих нас термодинамических систем и существующих тепловых машин;
Б). термодинамику необратимых процессов, которая описывает системы в состояниях, заметно отличающихся от равновесного.
Термодинамический и статистический методы изучения макросистем дополняют друг друга. Термодинамика позволяет изучать явления без знания их внутренних механизмов, а статистический метод позволяет понять суть явлений, установить связь поведения системы в целом с поведением и свойствами отдельных частиц.
Любое макроскопическое тело состоит из огромного числа молекул (один моль вещества содержит 6´1023частиц). Состояние такой системы может быть описано с помощью макроскопических параметров, таких как объем, давление, температура, внутренняя энергия и других величин, характеризующих тело в целом. Охарактеризованное таким способом состояние называется макросостоянием.
Состояние тела, охарактеризованное так, что заданы состояния каждой его молекулы, называется микросостоянием. Каждое микросостояние это способ реализации макросостояния.
Всякому макросостоянию системы соответствуют различные микросостояния, причем количество их очень велико. Число микросостояний, которыми может быть реализовано данное макросостояние, называется термодинамической вероятностью макросостояния или статистическим весом, обозначаетсяW.
В квантовой механике состояние системы (частицы) характеризуется волновой функцией (вообще говоря вектором состояния) — комплекснозначной функцией «координат», квадрат модуля которого интерпретируется как плотность вероятности получения заданных значений «координат». Согласно современным представлениям вероятностное определение состояния является полным и причиной вероятностного характера квантовой физики не являются какие-либо «скрытые» факторы — это связано с природой самих процессов. В квантовой физике оказываются возможными любые взаимопревращения различных частиц, не запрещенные теми или иными законами сохранения. И эти взаимопревращения подчиняются закономерностям — вероятностным закономерностям. По современным представлениям принципиально невозможно предсказать ни момент взаимопревращения, ни конкретный результат. Можно лишь говорить о вероятностях тех или иных процессов превращения. Вместо точных классических величин в квантовой физике возможна только оценка средних значений (математических ожиданий) этих величин, например, среднее время жизни частицы.
Сре́днее значе́ние — числовая характеристика множества чисел или функций (в математике); — некоторое число, заключённое между наименьшим и наибольшим из их значений.
ВОПРОС 18
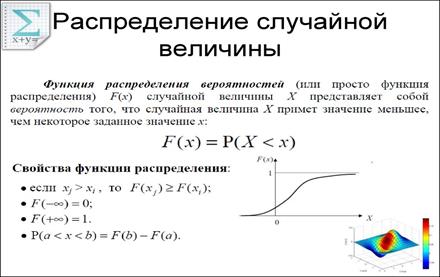
Функция распределения.
Функции распределения используют в тех ситуациях, когда имеют дело с большим числом случайных событий. С функцией распределения ознакомитесь на примере распределения ожидающих электричку пассажиров на платформе. Проведем ось ОХ вдоль платформы. Разобьем платформу на участки длинами Dx1, Dx2,... Dxk,...Dxm. Обозначим числа пассажиров, стоящих в ожидании электрички на каждом из участков DN1, DN2,... DNk,... DNm. Если для каждого из участков величина одна и та же, то распределение пассажиров на платформе является равномерным. При малых значениях Dxkвеличину nkназывают плотностью распределения координаты пассажиров. По прибытии электрички, до открытия дверей пассажиры группируются напротив них; образуются "сгустки". Теперь распределение не является равномерным. Величина nkтеперь зависит от координаты участка. Произошло изменение распределения. Плотность распределения обладает очевидным свойством , где N - полное число пассажиров на платформе. Размерность плотности распределения м-1. В приведенном примере случайным событием, или случайным экспериментом, является размещение пассажира в данном месте с координатой х. Координата х - случайная величина.
ВОПРОС 19
Скорости молекул газа имеют различные значения и направления, причем из-за огромного числа соударений, которые ежесекундно испытывает молекула, скорость ее постоянно изменяеться. Поэтому нельзя определить число молекул, которые обладают точно заданной скоростью v в данный момент времени, но можно подсчитать число молекул, скорости которых имеют значение, лежащие между некоторыми скоростями v 1 и v 2. На основании теории вероятности Максвелл установил закономерность, по которой можно определить число молекул газа, скорости которых при данной температуре заключены в некотором интервале скоростей. Согласно распределению Максвелла, вероятное число молекул в единице объема; компоненты скоростей которых лежат в интервале от  до
до 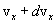 , от
, от  до
до 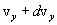 и от
и от  до
до 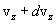 , определяются функцией распределения Максвелла
, определяются функцией распределения Максвелла

где m - масса молекулы, n - число молекул в единице объема. Отсюда следует, чтсг число молекул, абсолютные значения скоростей которых лежат в интервале от v до v + dv, имеет вид

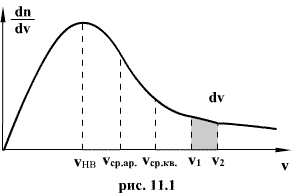
Распределение Максвелла достигает максимума при скорости  , т.е. такой скорсти, к которой близки скорости большинства молекул. Площадь заштрихованной полоски с основанием dV покажет, какая часть от общего числа молекул имеет скорости, лежащие в данном интервале. Конкретный вид функции распределения Максвелла зависит от рода газа (массы молекулы) и температуры. Давление и объем газа на распределение молекул по скоростям не влияет.
, т.е. такой скорсти, к которой близки скорости большинства молекул. Площадь заштрихованной полоски с основанием dV покажет, какая часть от общего числа молекул имеет скорости, лежащие в данном интервале. Конкретный вид функции распределения Максвелла зависит от рода газа (массы молекулы) и температуры. Давление и объем газа на распределение молекул по скоростям не влияет.
Кривая распределения Максвелла позволит найти среднюю арифметическую скорость
 .
.
Таким образом,

| (11.1) |
С Повышением температуры наиболее вероятная скорость возрастает, поэтому максимум распределения молекул по скоростям сдвигается в сторону больших скоростей, а его абсолютная величина уменьшается. Следовательно, при нагревании газа доля молекул, обладающих малыми скоростями уменьшается, а доля молекул с большими скоростями увеличивается.
·
·
· ВОПРОС 20
·
Идеальный газ – это модель разреженного газа, в которой пренебрегается взаимодействием между молекулами. Силы взаимодействия между молекулами довольно сложны. На очень малых расстояниях, когда молекулы вплотную подлетают друг к другу, между ними действуют большие по величине силы отталкивания. На больших или промежуточных расстояниях между молекулами действуют сравнительно слабые силы притяжения. Если расстояния между молекулами в среднем велики, что наблюдается в достаточно разреженном газе, то взаимодействие проявляется в виде относительно редких соударений молекул друг с другом, когда они подлетают вплотную. В идеальном газе взаимодействием молекул вообще пренебрегают.
Теория создана немецким физиком Р. Клаузисом в 1957 году для модели реального газа, которая называется идеальный газ. Основные признаки модели:
· расстояния между молекулами велики по сравнению с их размерами;· взаимодействие между молекулами на расстоянии отсутствует;· при столкновениях молекул действуют большие силы отталкивания;· время столкновения много меньше времени свободного движения между столкновениями;· движения подчиняются законом Ньютона;· молекулы - упругие шары;· силы взаимодействия возникают при столкновении.
Границы применимости модели идеального газа зависят от рассматриваемой задачи. Если необходимо установить связь между давлением, объемом и температурой, то газ с хорошей точностью можно считать идеальным до давлений в несколько десятков атмосфер. Если изучается фазовый переход типа испарения или конденсации или рассматривается процесс установления равновесия в газе, то модель идеального газа нельзя применять даже при давлениях в несколько миллиметров ртутного столба.
Давление газа на стенку сосуда является следствием хаотических ударов молекул о стенку, вследствие их большой частоты действие этих ударов воспринимается нашими органами чувств или приборами как непрерывная сила, действующая на стенку сосуда и создающая давление.
Давление и температура с точки зрения молекулярно кинетической теории.
Температура
Любое макроскопическое тело или группа макроскопических тел называется термодинамической системой.
Тепловое или термодинамическое равновесие - такое состояние термодинамической системы, при котором все ее макроскопические параметры остаются неизменными: не меняются объем, давление, не происходит теплообмен, отсутствуют переходы из одного агрегатного состояния в другое и т.д. При неизменных внешних условиях любая термодинамическая система самопроизвольно переходит в состояние теплового равновесия.
Температура - физическая величина, характеризующая состояние теплового равновесия системы тел: все тела системы, находящиеся друг с другом в тепловом равновесии, имеют одну и ту же температуру.
Абсолютный нуль температуры - предельная температура, при которой давление идеального газа при постоянном объеме должно быть равно нулю или должен быть равен нулю объем идеального газа при постоянном давлении.
Давление - это явление когда частицы (молекулы) "давят" на сосуд (под действием внутренней энергии и теплового беспорядочного движения ударяются в стенки сосуда). Чем больше кинетическая энергия частицы тем больше сила удара об стенку приходящаяся на единицу площади, тем больше давление.
Уравнение состояния идеального газа
Параметры, с помощью которых описывают состояние идеального газа, как макросистемы это давление (p), объем (V), температура по шкале Кельвина (T). Очевидно, что уравнение, которое их связывает, является очень значимым с точки зрения теории и практики. Называется оно уравнением состояния идеального газа (иногда просто уравнением идеального газа):
p=nkT
где k -1.38 ×10 ^23)Дж/К – постоянная Больцмана,
n=N/V
n- число молекул в единице объема газа (концентрация частиц вещества), N — число его молекул в заданном объеме
Уравнению (1) можно придать известную форму уравнения Клапейрона (Надо отметить, что от изменения формы записи уравнения (2), (3)
не перестают быть уравнениями состояния идеального газа):
p=uRT/V
или
p=RT/uр
где u количество молей
· газа, R=Na×K=8,3 Дж/(моль•К) – молярная (универсальная) газовая постоянная, (Na-6,022×10^-23моль-1 (постоянная Авогадро)), u– молярная масса газа, p – плотность газа
· ВОПРОС 21

ВОПРОС 22
понятие числа степеней свободы: это число независимых координат, полностью определяющих положение тела (материальной точки, системы материальных точек) в пространстве. Так, например, положение материальной точки определяется тремя координатами (x, y, z), следовательно, i = 3. Тонкий стержень имеет 5 степеней свободы (x, y, z, a, b), т.е. 3 поступательных и 2 вращательных, твердое тело имеет 6 степеней свободы (x, y, z, a, b, g), т.е. 3 поступательные и 3 вращательные. I = 3, для двухатомных молекул газа (H2, O2, N2) с жесткой связывающей характеристикой i = 5, для трех- и более атомных молекул газа с жесткой связью CO2, NH3) i = 6. Естественно, что жестких связей между атомами не существует - атомы могут совершать колебания. С учетом этого полное число степеней свободы i. = I + 2iколеб. Я считаю, что = 0. Итак, независимо от числа степеней свободы. Преимущества перед средними значениями равны 1/3 значения <Wk>, т.е. <Wk> / 3 = кТ / 2. Важнейший закон классической статистической физики - закон неравномерного распределения энергии по степеням свободы - утверждает: при каждой степени свободы в среднем должны совпадать одинаковые кинетическая энергия, равная kT / 2. Следовательно, средняя кинетическая энергия молекулы, <Wk> = kT. Взаимодействующая энергия может представлять собой молекулярную энергию. Для одного моля для низкой массы газа Таким образом, температура газа зависит от числа степеней свободы его молекул.
ВОПРОС 23
Первое начало термодинамики представляет собой закон сохранения энергии, один из всеобщих законов природы (наряду с законами сохранения импульса, заряда и симметрии):
Энергия неуничтожаема и несотворяема; она может только переходить из одной формы в другую в эквивалентных соотношениях.
Первое начало термодинамики представляет собой постулат – оно не может быть доказано логическим путем или выведено из каких-либо более общих положений. Истинность этого постулата подтверждается тем, что ни одно из его следствий не находится в противоречии с опытом. Приведем еще некоторые формулировки первого начала термодинамики:
Полная энергия изолированной системы постоянна;
Невозможен вечный двигатель первого рода (двигатель, совершающий работу без затраты энергии).
Первое начало термодинамики устанавливает соотношение между теплотой Q, работой А и изменением внутренней энергии системы ΔU:
Изменение внутренней энергии системы равно количеству сообщенной системе теплоты минус количество работы, совершенной системой против внешних сил.
 (I.1)
(I.1)
 (I.2)
(I.2)
Уравнение (I.1) является математической записью 1-го начала термодинамики для конечного, уравнение (I.2) – для бесконечно малого изменения состояния системы.
Внутренняя энергия является функцией состояния; это означает, что изменение внутренней энергии ΔU не зависит от пути перехода системы из состояния 1 в состояние 2 и равно разности величин внутренней энергии U2 и U1 в этих состояниях:
 (I.3)
(I.3)
Следует отметить, что определить абсолютное значение внутренней энергии системы невозможно; термодинамику интересует лишь изменение внутренней энергии в ходе какого-либо процесса.
Рассмотрим приложение первого начала термодинамики для определения работы, совершаемой системой при различных термодинамических процессах (мы будем рассматривать простейший случай – работу расширения идеального газа).
Изохорный процесс (V = const; ΔV = 0).
Поскольку работа расширения равна произведению давления и изменения объема, для изохорного процесса получаем:
 (I.1)
(I.1)
 (I.4)
(I.4)
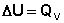 (I.5)
(I.5)
Изотермический процесс (Т = const).
Из уравнения состояния одного моля идеального газа получаем:
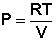 (I.6)
(I.6)
Отсюда:
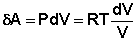 (I.7)
(I.7)
Проинтегрировав выражение (I.6) от V1 до V2, получим
 (I.8)
(I.8)
Изобарный процесс (Р = const).
 (I.9)
(I.9)
Подставляя полученные выражения для работы различных процессов в уравнение (I.1), для тепловых эффектов этих процессов получим:
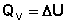 (I.10)
(I.10)
 (I.11)
(I.11)
 (I.12)
(I.12)
В уравнении (I.12) сгруппируем переменные с одинаковыми индексами. Получаем:
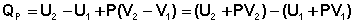 (I.13)
(I.13)
Введем новую функцию состояния системы – энтальпию H, тождественно равную сумме внутренней энергии и произведения давления на объем:

Тогда выражение (I.13) преобразуется к следующему виду:
 (I.14)
(I.14)
Т.о., тепловой эффект изобарного процесса равен изменению энтальпии системы.
Адиабатический процесс (Q = 0).
При адиабатическом процессе работа расширения совершается за счёт уменьшения внутренней энергии газа:
 (I.15)
(I.15)
В случае если Cv не зависит от температуры (что справедливо для многих реальных газов), работа, произведённая газом при его адиабатическом расширении, прямо пропорциональна разности температур:
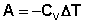 (I.16)
(I.16)
ВОПРОС 24
Количественная мера передаваемого в каком либо процессе через границы системы упорядоченного движения называется работой, сам такой вид обмена энергией также называется работой.
Подчеркнем, что работа существует только при наличии процесса и его величина зависит от того, как протекает процесс. Поэтому работа является функцией процесса.
Полную работу А, совершаемую газом при изменении его объема от V 1 до V 2, найдем интегрированием формулы (52.1):

При изохорном процессе газ не совершает работы над внешними телами, т. е.

При изобарном процессе работа газа при увеличения объема от V 1 до V 2 равна


Исходя из  и
и 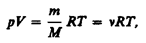 найдем работу изотермического расширения газа:
найдем работу изотермического расширения газа:

Из первого начала термодинамики (dQ= d U+dA) для адиабатического процесса следует, что

Изохорический процесс
Изохорический процесс происходит при постоянном объеме. Зависимость давления от температуры описывается уравнением:
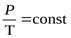 - закон Шарля, (2)
- закон Шарля, (2)
который читается: для данной массы газа при постоянном объеме давление газа линейно возрастает с увеличением температуры.
Изобарический процесс
Изобарический процесс. Это процесс, происходящий при постоянном давлении, Р =const.
Зависимость объема от температуры описывается законом:

 - закон Гей-Люсака, (3)
- закон Гей-Люсака, (3)
который читается: для данной массы газа при постоянном давлении объем газа линейно возрастает с ростом температуры.
Изотермический процесс
Если в некотором процессе не изменяются масса и температура газа, то такой процесс называется изотермическим.
При m = const T = const P1V1 = P2V2 или PV = const.
Полученное PV = const уравнение называется уравнением изотермического процесса.
Это уравнение было получено английским физиком Робертом Бойлем в 1662 году и французским физиком Эдмоном Мариоттом в 1676г.
Уравнение Р1 / Р2 = V2 / V1 называется уравнением Бойля-Мариотта.
Состояние газа характеризуется тремя макропараметрами:
P — давлением,
V — объёмом,
T — температурой.
При графическом изображении процесса можно указать только два пара
ВОПРОС 25
1)Теплоёмкость количество теплоты, поглощаемой телом при нагревании на 1 градус;