Введение
Элементы-органогены – C, H (в углеводородах), O, N (в большинстве производных углеводородов), иногда S и P. Гетероэлементы – O,N. Функциональная группа – это атом, или группа атомов, определяющих
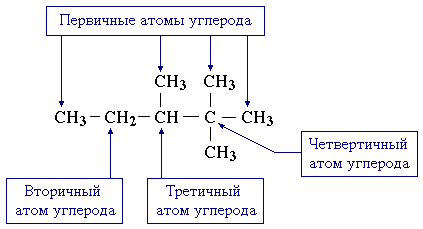 характерные свойства определенного класса соединений. Атом углерода, связанный в цепи только с одним другим атомом углерода, называют первичным, с двумя – вторичным, с тремя – третичным.
характерные свойства определенного класса соединений. Атом углерода, связанный в цепи только с одним другим атомом углерода, называют первичным, с двумя – вторичным, с тремя – третичным.
Примером первичных алкилов может служить метил ·CH3(связан с 1 атомом углерода). вторичных — изопропил ·CH(CH3)2 (связан с 2 атомами углерода), третичных (связан с 3 атомами углерода)— трет -бутил ·C(CH3)3
Виды изомерии:
Структурная
А) Изомерия углеродной цепи (углеродного скелета)
Пример — бутан СН3—СН2—СН2—СН3 и изобутан (СН3)3СН
Б) Изомерия функциональной группы (межклассовая изомерия)
Пример - этанол (CH3—CH2—OH) и диметиловый эфир (CH3—O—CH3).
В) Изомерия положения кратной связи
Пример - 2-хлорбутановая кислота и 4-хлорбутановая кислота.
Г) Межклассовая
Пример - Алкены и циклоалканы
2) Пространственная
А) Геометрическая
Пример – цис-бутен-2 и транс-бутен-2
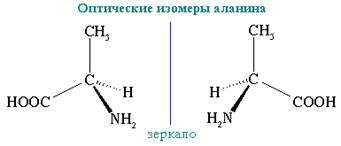
Б) Оптическая
Пример – 3-метилгексан или
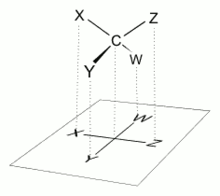
Проекция Ньюмана — в стереохимии алканов способ визуализировать химическую конформацию связи углерод-углерод. (бутан)

Проекция Фишера — способ изображения трёхмерной молекулы в виде проекции, в которой вертикальные связи удаляются за проекционную плоскость, а горизонтальные связи выступают перед этой плоскостью
Конформация – пространственное расположение атомов в молекуле, обусловленное поворотом вокруг сигма-связей (конформация циклопентана – «конверт»)

Углеводороды. Алканы
Углеводороды – органические соединения, состоящие из углерода и водорода. Они делятся на ациклические(алифатические) и циклические. Ациклические – на насыщенные (алканы) и ненасыщенные (алкены, алкины, алкадиены). Циклические – на алициклические (циклоалканы, циклоалкены) и ароматические (арены). Алканы – это насыщенные ациклические углеводороды, в молекулах которых атомы связаны одинарными сигма-связями.  -гибридизация – смешивание 1 s- и 3 p-орбиталей. Сигма-связь – соединяет 2 центра атомов, очень прочная. Физ. св-ва – С1-С4 – при обычных условия газы, С5-С15 – жидкости, с С16 – тв.в-ва. Углеводороды разветвленного строения име.т более низкую плотность и темп. кипения, чем их неразветвл. изомеры, т.к. молекулы неразветвл. строения плотнее примыкают друг к другу и сильнее взаимодействуют между собой, чем разветвл. молекулы. С увеличением молекулярной массы увелич. температура кипения и плавления. Алканы нерастворимы в воде, но растворимы в бензоле, CCl4. Метан – газ без цвета и запаха, легче воздуха. Нахождение А. в природе: метан – главная составляющая часть природного газа. Высшие алканы входят в состав пчелиного воска, восковых покрытий листьев, плодов и семян растений. Хим. св-ва:
-гибридизация – смешивание 1 s- и 3 p-орбиталей. Сигма-связь – соединяет 2 центра атомов, очень прочная. Физ. св-ва – С1-С4 – при обычных условия газы, С5-С15 – жидкости, с С16 – тв.в-ва. Углеводороды разветвленного строения име.т более низкую плотность и темп. кипения, чем их неразветвл. изомеры, т.к. молекулы неразветвл. строения плотнее примыкают друг к другу и сильнее взаимодействуют между собой, чем разветвл. молекулы. С увеличением молекулярной массы увелич. температура кипения и плавления. Алканы нерастворимы в воде, но растворимы в бензоле, CCl4. Метан – газ без цвета и запаха, легче воздуха. Нахождение А. в природе: метан – главная составляющая часть природного газа. Высшие алканы входят в состав пчелиного воска, восковых покрытий листьев, плодов и семян растений. Хим. св-ва:
Алканы являются насыщенными углеводородами, поэтому не вступают в реакции присоединения.
Для реакций алканов характерен радикальный механизм.
Условия проведения радикальных реакций: высокая температура, действие света, присутствие соединений – источников свободных радикалов (инициаторов), неполярные растворители.
Реакции окисления алканов:
CH4 + 2 O2→ CO2 + 2 H2O + 802,5 кДж
CH3-CH2-CH2-CH3 + 3O2→2CH3-COOH + 2H2O
бутан уксусная кислота
С водяным паром: CH4 + H2O→ CO + 3H2
Дегидрирование алканов: С2Н6=С2Н4+Н2
Изомеризация алканов: С5Н12-AlCl3,100-  CH3-CH(CH3)-CH2-CH3
CH3-CH(CH3)-CH2-CH3
Крекинг алканов: C6H14-500-  C2H4+C4H10, (пропен+пропан, бутен+бутан)
C2H4+C4H10, (пропен+пропан, бутен+бутан)
Реакции замещения:
- Галогенирование: CH4 + Cl2→CH3Cl + HCl
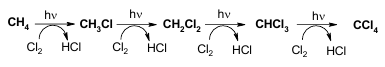
- Нитрование алканов (реакция Коновалова):

7) Ароматические углеводороды (арены) – углеводороды,молекулы которых содержат одно или несколько бензольных колец – циклических групп атомов с особым характером связи. Ароматическая π-система в молекуле бензола образована взаимно перекрывающимися р-орбиталями 6 атомов углерода. Многоядерные (полициклические) арены - соединения, содержащие ароматические кольца, которые имеют два общих атома углерода, называются конденсированными. К ним относятся нафталин, фенантрен, антрацен. 