Регуляция водно-солевого гомеостаза.
Рассмотрев основные этапы процесса мочеобразования, мы можем перейти к регуляции водно-электролитного гомеостаза, в которых почка выполняет роль эффекторного органа.
Общий объем жидкостей тела составляет у человека примерно 60% массы тела. Этот объем распределен между двумя большими секторами: внутриклеточным и внеклеточным.
| Внутриклеточная жидкость | Внеклеточная жидкость | |
| 40% | Интерстициальная жидкость 16% | Кровь 4% |
Для нормальной жизнедеятельности организма в этих жидкостных средах необходимо поддерживать постоянство физико-химического состава и свойств — гомеостаз. Однако многие факторы, влияющие на организм, такие как прием, потеря или ограничение потребления воды, усиленное потребление соли или ее дефицит, смещение метаболизма и т. д. способны изменять объем и состав жидкостей тела. Отклонения параметров внутренней среды от некоторого нормального уровня включают механизмы регуляции. Система регуляции водно-электролитного гомеостаза имеет много контуров: это и регуляция объема, осмотической концентрации, ионного состава и др.
Для их дальнейшего рассмотрения нам следует найти тот основной контур, с которым связаны остальные. Таким контуром является содержание в организме Na. Действительно, ион натрия, удерживая молекулы воды, определяет объем и осмолярность жидкостей внутренней среды и обеспечивает целый ряд жизненно-важных функций.
Регуляция выведения Na почкой осуществляется двумя системами: антинатрийуретической и натрийуретической. Антинатрийуретическая система обеспечивает задержку Na и уменьшает его выведение. Она имеет гуморальное и рефлекторное звено. Гуморальное звено связано с ренин-ангиотензин-альдостероновой системой (РААС), которая включает следующие элементы: ренин-протеолитический фермент, секретируемый юкстагломерулярным аппаратом (ЮГА) почки. Ренинпродуцирующие клетки чувствительны к уменьшению объема, перепадам АД в приносящих артериолах, и к изменению концентрации Na в канальцевой жидкости (рис. 13)
Ренин действует на ангиотензиноген и отщепляет от него пептид из десяти аминокислот, образуя ангиотензин-I. Под действием ангиотензин-превращающего фермента (АПФ) неактивный ангиотензин-1 переходит в ангиотензин-II, который представляет физиологически высокоактивное вещество, обладающее множественными эффектами, среди которых наиболее значимыми являются стимуляция синтеза и секреции альдостерона корой надпочечников и мощное сосудосуживающее действие. Обратите внимание на то, что действие многих современных гипотензивных лекарственных препаратов, применяющихся для лечения гипертонических состояний, снижает активность РААС именно за счёт ингибирования АПФ.

Рисунок 13 Схема взаимодействия компонентов РААС
Альдостерон является главным «действующим лицом» антинатрийуретической системы. Он усиливает в почечных канальцах реабсорбцию натрия, что приводит к задержке этого иона в организме. Рассмотрим клеточный механизм действия гормона. Своё действие он оказывает в дистальном извитом канальце.
Альдостерон, как и все стероидные гормоны, проникает в клетку и взаимодействует со специфическим белковым рецептором. Образовавшийся комплекс гормон-рецептор проникает в ядро и индуцирует процесс транскрипции генов, в результате включается синтез по крайней мере трех функциональных канальцевых белков: 1.белков–каналов,облегчающих проникновение в клетку Na через апикальную мембрану, 2. белков-насосов Na-K-АТФазы -, непосредственно обеспечивающих активный перенос Na из канальцев в кровь и 3. белков-ферментов в митохондриях, обеспечивающих клетки энергией, необходимой для транспорта натрия. Таким образом, альдостерон увеличивает реабсорбцию натрия и делает это, если можно так выразиться, «виртуозно», воздействуя на все этапы его транспорта. Кроме того, альдостерон уменьшает реабсорбцию калия в канальцах почки.
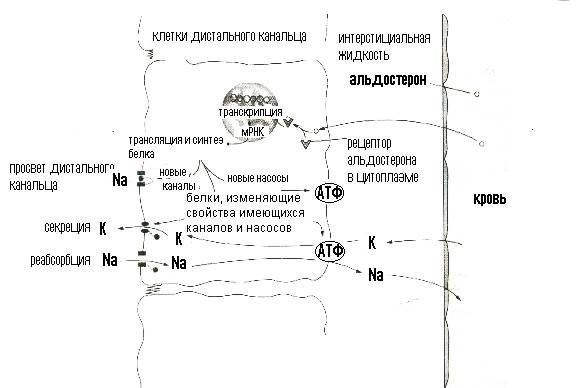
Рисунок 14 Клеточный механизм действия альдостерона
Натрийуретическая система обеспечивает выведение натрия почкой (натрийурез) и активируется при увеличении объема жидкости. Натрийуретическая система представлена семейством веществ, общее название которых НУП (натрийуретические пептиды). К ним прежде всего следует отнести предсердный натрийуретический пептид (ПНП). (Другие названия: кардиопептид, АНП - атриальный натрийуретический фактор, предсердный натрийуретический гормон – ПНГ). Он синтезируется в клетках предсердий и состоит из 28 аминокислот.
ПНП обладает сильным натрийуретическим, диуретическим и гипотензивным эффектом. Его натрийуретический эффект реализуется через влияние на гемодинамику, СКФ и снижение реабсорбции натрия в почечных канальцах. Несмотря на явную способность ПНП усиливать почечную экскрецию натрия, механизм его действия еще полностью непонятен. Возможно, он играет роль модулятора, приводящего активность системы, обеспечивающей баланс натрия, в соответствие с потребностями системы кровообращения.
Существует мозговой или гипоталамический НУП, образующийся в ядрах заднего гипоталамуса. Описан и почечный НУП - уродилатин.
В таблице 2 мы попытались представить факторы, влияющие на натрийуретическую функцию почек.
Таблица 2
| Факторы, вызывающие увеличение экскреции натрия почками: | Факторы, вызывающие уменьшение экскреции натрия почками |
| ПНП (кардиопептид) | альдостерон |
| гипоталамиический НУП | ангиотензин-II |
| уродилатин (почечный НУП) | норадреналин |
| АДГ (вазопрессин) | адреналин |
| окситоцин | почечные нервы |
| дигоксиноподобный натрийуретический гормон | простагландин F2a |
| простагландин Е-2 | инсулин |
| кинины | эстрогены |
| оксид азота (NO) |
Анализируя данные таблицы, следует признать, что существует богатый набор веществ, обладающих как натрийзадерживающим, так и натрийуретическим действием. Они имеют в нефроне разные точки приложения, однако роль многих из них и механизм действия пока не ясен. Однако, такая многофакторная система обеспечивает довольно стабильное содержание натрия в организме.
Теперь мы можем ввести в действие эти системы и включить их в регуляцию водно-солевого обмена. По современным представлениям, поддержание водно-солевого гомеостаза обусловлено взаимосвязанной деятельностью физиологических систем регуляции объема, осмотической концентрации и ионного состава жидкостных сред организма. Эти системы обладают рецепторами, воспринимающими изменение состава и объема внутренней среды, центральными представительствами, где происходит интеграция поступающей информации. Далее соответствующие нервные и гормональные команды передаются основному эффектору-почке. Почка благодаря перестройке, главным образом натрий- и водо-выделительной функции, обеспечивает поддержание основных гомеостатических параметров на оптимальном уровне.
Регуляция объема жидкостей или волюморегуляция.
Волюморегуляция (от слова volume-объем) осуществляется сочетанной деятельностью антинатрийуретической, натрийуретической и антидиуретической систем. Считается, что содержание Na в организме регулируется через изменение объема жидкости, главным образом крови. От содержания Na зависит величина объема жидкости организма. Волюморегуляция осуществляется рефлекторным путем. Информационный блок представлен волюморецепторами.
Волюморецепторы располагаются в артериальной системе и предсердиях и реагируют на степень их растяжения. Объемные сдвиги могут происходить в сторону уменьшения объема или его увеличения.
Уменьшение объема - гиповолюмия может явиться следствием кровопотери, диареи, ортостатических перераспределений крови, уменьшения объема циркулирующей крови или снижения кровяного давления. Целесообразная биологическая реакция почек должна выразиться в уменьшении диуреза и натрийуреза, соответственно задержке Na и воды в организме. Другими словами, в действие должна быть приведена антинатрийуретическая и антидиуретическая система. Последовательность и направленность реакций такова: уменьшение объема циркулирующей крови (независимо от причин) вызывает усиление секреции ренина почками и включает РААС (1 на рисунке 15). В конечном итоге образуется ангиотензин-II, который с одной стороны увеличивает тонус сосудов и способствует повышению кровяного давления, с другой приводит к увеличению секреции альдостерона и увеличению реабсорбции натрия. Таким образом, срабатывает антинатрийуретическая система. Одновременно информация от волюморецепторов а также прессорецепторов об уменьшении объема крови направляется в супраоптическое ядро гипоталамуса (2 на рисунке 15), увеличивается секреция и выделение из задней доли гипофиза АДГ, он действует на почку, где увеличивает реабсорбцию воды. Таким образом, происходит задержка и воды и восстанавливается объем жидкости (рис. 15)
Увеличение объема - гиперволюмия обусловлена увеличением объема внеклеточной жидкости и может явиться следствием переливания крови или кровезаменителей, введением физиологического раствора, развития сердечной недостаточности, отечных состояний.
В этом случае биологически целесообразная реакция со стороны почек проявляется в увеличении экскреции натрия и воды. В данном случае в реакцию вовлекается натрийуретическая система, происходит увеличение выведения Na, вслед за которым уйдет и вода. Последовательность процессов при гиперволюмии такова (рисунок 16 - 1): увеличение объема включает волюморегулирующий рефлекс, возрастает приток крови к сердцу, растягиваются стенки предсердий, раздражаются волюморецепторы, информация от них направляется в гипоталамус, из задних ядер которого выделяется гипоталамический натрийуретический пептид (НУП). Кроме того, при растяжении предсердий из них выделяется предсердный натриуретический пептид (ПНП). Под действием натрийуретических пептидов усиливается выведение натрия и воды.
Предположительно, гиперволюмия может сопровождаться уменьшением активности антинатрийуретической системы и снижением секреции альдостерона, что также способствует выведению натрия (рисунок 16 – 2).
ц
3ы
Рисунок 15 Схема волюморегулирующего рефлекса при гиповолюмии
Одновременно при увеличении наполнения предсердий возбуждение волюморецепторов угнетает секрецию и выделение АДГ, что приводит к 
Рисунок 16 Схема волюморегулирующего рефлекса при гиперволюмии
увеличению диуреза. Таким образом, выводится натрий и вода, и организм разгружается от избытков жидкости. Обратите внимание, что изменение внеклеточного объема жидкости включает волюморегулирующие рефлекторные реакции с однонаправленной параллельной экскрецией и натрия и воды. Это целесообразное явление, поскольку обстоятельства, вызвавшие изменения объема, часто связаны с потерей или избыточным количеством натрия и воды в организме примерно в пропорциональных количествах.
Осморегуляция
Осмотическая концентрация и осмотическое давление плазмы крови являются наиболее жесткими константами внутренней среды организма и определяются главным образом соотношением воды и натрия. Механизмы осморегуляции изучены наиболее подробно и вам будет интересно узнать, что создателями учения об осморегулирующей системе организма являются ваши преподаватели – коллектив кафедры нормальной физиологии НГМА под руководством профессора Финкинштейна Я.Д. Осморегулирующая система построена из совокупности осморегулирующих рефлексов, которые компенсируют сдвиги осмолярности посредством изменения экскреции главным образом воды. Следовательно, главная часть этой системы-антидиуретическая. Выведение воды почкой регулируется АДГ и в конечном итоге определяется теми факторами, которые влияют на скорость синтеза и секреции АДГ. Сенсорный механизм антидиуретической системы представлен осморецепторами. Центральные осморецепторы открыл английский физиолог Е. Верней. Он обнаружил осмочувствительные зоны в супраоптических и паравентрикулярных ядрах гипоталамуса. Однако восприятие осмотического давления обеспечивается не только осморецепторами мозга. Идея о том, что осморецепторы могут быть локализованы и в других органах принадлежит А.Г. Гинецинскому. И действительно, периферические осморецепторы были обнаружены в печени, сердце, почке, легких и других органах. Главной осморецепторной зоной является печень, так как именно в нее по системе воротной вены поступают всосавшиеся в кишечнике натрий и вода. Широко распространенные во многих органах и тканях периферические осморецепторы делают возможным постоянное наблюдение за общими и регионарными изменениями осмолярности и непрерывно снабжают центры необходимой информацией.
Осмотическая концентрация жидкостей внутренней среды, как и их объем, может изменяться в двух направлениях – увеличиваться или уменьшаться. Ее увеличение - гиперосмия может создаться при дефиците поступления воды в организм - дегидратации, или избыточном поступлении соли. При этом включается осморегулирующий рефлекс (рис. 17), возбуждаются осморецепторы и рефлекторно стимулируется секреция АДГ, возрастает водная проницаемость СТ, увеличивается факультативная реабсорбция воды, уменьшается диурез и выделяется небольшой объем гиперосмотичной (концентрированной) мочи. Одновременно увеличивается выведение натрия и осмолярность жидкостей восстанавливается до нормальной. Что касается механизма натрийуреза в этой ситуации, то он не совсем ясен. При значительном обезвоживании организма происходит включение всех регуляторных систем: и объемной и осмотической.

Рисунок 17 Схема осморегулирующего рефлекса
Уменьшение осмотической концентрации – гипоосмия может возникнуть после обильного поступления воды (гипергидратация) или уменьшения поступления соли. Реакция почек в этой ситуации проявляется в увеличении диуреза и снижении экскреции натрия. Включается тот же осморегулирующий рефлекс, возбуждаются осморецепторы, информация поступает в центр, секреция и выделение АДГ тормозится. В результате развивается водный диурез.
Обратите еще раз внимание на то, что когда почки участвовали в регуляции объема, они параллельно изменяли выведение натрия и воды, а в случае осморегуляции почки изменяют их разнонаправлено, что в этой ситуации является биологически целесообразной реакцией (рисунок 17 – графики).
Взаимодействие осмотических и объёмных стимулов обеспечивает адекватные для ситуации изменения экскреции воды почкой. В нормальных условиях главным стимулом секреции АДГ является осмотическая концентрация внеклеточной жидкости. При небольших изменениях объёма крови и смещении осмолярности в первую очередь выравнивается осмотическая концентрация крови. При значительных изменениях объёма внутрисосудистой жидкости (более 10%) к системе осморегуляции подключается система регуляции объема.
Рассмотрим ещё один вопрос. Водно-солевой баланс зависит не только от точно регулируемой экскреции натрия и воды почками, но и от эффективности механизма жажды и солевого аппетита. При неизбежных потерях воды механизм жажды может в какой-то мере обеспечить их компенсацию посредством питья. Что касается натрия, то поддержание его нормальной концентрации во внеклеточной жидкости может осуществляться частично благодаря контролю его потребления (солевой аппетит). Оба чувства формируются при участии ЦНС. Жажда и солевой аппетит, побуждая к поиску воды и натрия стимулируя их потребление, могут частично восстановить водно-солевой гомеостаз, однако, несомненно, что основную роль в обеспечении постоянного состава плазмы крови играют специальные системы, регулирующие выведение натрия и воды почками в точном соответствии потребностям организма.
Заключение
Поддержание стабильности таких жизненно-важных гомеостатических показателей, как объём жидкостных секторов, их осмотическая концентрация осуществляется многокомпонентной системой регуляции (Рисунок 18).

Рисунок 18 Схема взаимодействия нервных и гуморальных механизмов регуляции объема и осмолярности внутренней среды
Информационный блок этой системы представлен рецепторами различной природы, реагирующими на изменения объёма, осмолярности плазмы крови концентрации натрия и давления. Сенсорные механизмы локализуются как в мозгу, так и на периферии. Информация анализируется ЦНС, и для коррекции отклонений регулируемых параметров используются как нервные, так и гормональные механизмы. Объектом этих воздействий является мультифункциональный орган – почка, способная быстро и точно менять экскрецию воды и солей. Регуляторные механизмы, вовлекаемые в стабилизацию объёма и осмолярности внеклеточной жидкости, тесно взаимодействуют друг с другом.
Роль почки в регуляции кислотно-основного равновесия
рН крови является одной из наиболее жёстких констант и колеблется в очень узких пределах 7,35 – 7,45, и это, несмотря на то, что в результате обмена веществ в кровь из тканей за сутки поступают кислые продукты в количестве, эквивалентном двум литрам концентрированной соляной кислоты. Это количество в двадцать раз превышает все основания, содержащиеся в организме, и тем не менее, реакция крови не претерпевает никаких изменений.
Постоянство рН крови поддерживается, прежде всего, буферными системами, которые нейтрализуют сильные кислоты и щёлочи, превращая их в слабые кислоты и щёлочи, и тем самым, предотвращая резкое изменение рН крови. Однако, буферные системы, расходуя на эти процессы свои составные компоненты нуждаются в их восстановлении; они имеют ограниченную ёмкость и могут лишь временно сдерживать сдвиги рН. Окончательное слово в этих процессах принадлежит физиологическим регуляторам – органам выделения – лёгким и почкам. Лёгкие выводят летучие соединения, главным образом угольную кислоту, а почки - нелетучие соединения.
Решающее значение в поддержании постоянства рН крови имеет бикарбонатная буферная система, так как от её составных частей (содержания СО2 и бикарбонатов) главным образом зависит рН крови.
Любая кислота, поступающая в кровь в результате буферного эффекта отдаёт свой Н+ угольной кислоте, что приводит к увеличению парциального давления СО2, которая возбуждает дыхательный центр, объём вентиляции лёгких возрастает и избыток СО2 выводится из организма. Образовавшаяся кислота поступает в почечные канальцы. Реакция может быть представлена в следующем виде:

Таким образом, на нейтрализацию кислот расходуется бикарбонат натрия и происходит уменьшение щелочного резерва крови. Если бы не было механизмов, восстанавливающих использованные в буферной реакции основания, то щелочной резерв был бы быстро израсходован.
Роль почки в регуляции кислотно-основного равновесия и заключается в восстановлении щелочного резерва крови. В её основе лежит способность эпителия почечных канальцев секретировать в просвет ионы Н+ и обменивать их на ионы Na+. При этом достигается сразу два результата:
1) моча подкисляется и из организма окончательно выводится избыток кислых ионов (рН мочи может достигать 4,5).
2) вместо секретируемого иона Н+ реабсорбируется Na+ и одновременно анион HCO3-
3) образуется бикарбонат натрия, который возвращается в кровь и восполняет щелочной резерв крови.
Na+ + HCO3- → NaHCO3
Теперь давайте подробнее рассмотрим эти процессы. В клетках почечных канальцев образуется угольная кислота из воды и углекислого газа под действием фермента карбоангидразы (КА).

Рисунок 19 Реабсорбция бикарбоната в клетках
Проксимального канальца
Ион водорода активно секретируется в просвет канальца, а анион HCO3 - реабсорбируется в кровь. Секретируемый Н+ быстро соединяется с фильтруемым HCO3-, образуя угольную кислоту. Угольная кислота превращается в воду и углекислый газ с помощью карбоангидразы на апикальной стороне щёточной каёмки проксимального канальца. СО2 диффундирует обратно в клетку проксимального канальца, где соединяется с водой и образует угольную кислоту, тем самым завершая этот цикл (рис.19).
Далее включаются несколько вариантов ионообменных реакций, суть которых состоит в обмене иона Н+ на ион Na+ (рисунок 20)
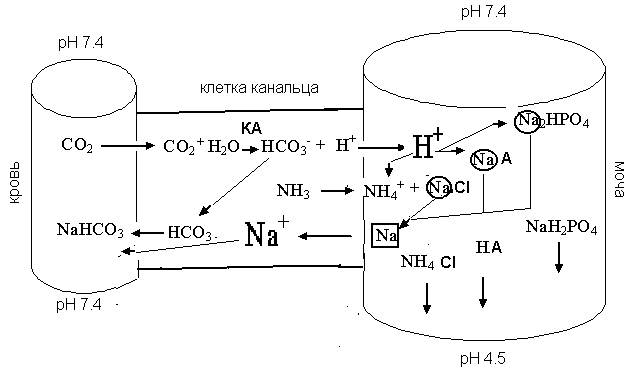
Рисунок 20 Схема процессов, принимающих участие в восстановлении щелочного резерва.
1) Соль слабой кислоты, образовавшаяся в ходе реакции (1) NaA взаимодействует Н+
NaA + H+ → HA + Na+
Свободная кислота (НА) выделяется с мочой, а Na+ реабсорбируется обратно в кровь. Этот путь используется лишь при выделении слабых органических кислот (молочной, ацетоуксусной, мочевой).
2) Кислый фосфат натрия превращается в щелочной. Поступившие в просвет канальца ионы Н+ вытесняют Na+ из щелочного фосфата и превращают его в кислый фосфат.
Na2HPO4 + H+ → NaH2PO4 + Na+
3) Эпителий почечных канальцев обладает способностью дезаминировать аминокислоты, главным образом глутаминовую, и превращать аминогруппу NH2 в аммиак NH3, который секретируется в канальцы, присоединяет ещё один ион Н+ и превращается в ион аммония NH4+.
Аммоний используется в качестве основания для удаления кислых радикалов, которые выделяются в виде нейтральных аммонийных солей, а Na+ реабсорбируется.
NH3 + H+ → NH4+
NaCl + NH4+ → NH4Cl + Na+
Таким образом, нейтрализуются сильные нелетучие кислоты.
Концентрация аммония регулируется преимущественно почками и колеблется в зависимости от состояния кислотно-щелочного равновесия организма.
Итак, как видно из схемы на рисунке 20, рН крови, поступающей в почку и оттекающей от нее 7,4, рН первичной мочи 7,4, а вот рН окончательной мочи может изменяться от 4,5 до 8,4 в зависимости от характера пищи и образа жизни.
При различного рода нарушениях кислотно-основного состояния (дыхательном или метаболическом ацидозах или алкалозах) почки и лёгкие помогают в той или иной мере компенсировать возникшие отклонения рН.