Цель работы: определить массу кислот и солей в анализируемом растворе (г):
– проба А – щавелевая кислота;
– проба Б – фосфорная кислота;
– проба В – смесь серной и фосфорной кислот;
– проба Г – смесь H3PO4 и NaH2PO4.
Сущность работы. Сильные кислоты и слабые кислоты с рKа < 8–9 можно определять методом прямого титрования стандартным раствором щелочи.
Щавелевая кислота является слабой органической кислотой, имеющей рKа ,1 = 1,25 и рKа ,2 = 4,27. Поскольку рK 2 – рK 1 < 4, то она титруется сразу по двум ступеням:
Н2С2О4 + 2NaOH = Na2С2О4 + 2Н2O (f экв(Н2С2О4) = 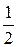 ).
).
При титровании щавелевой кислоты точка эквивалентности находится в щелочной среде, поэтому для фиксирования конечной точки титрования надо применять индикатор фенолфталеин (рТ = 9).
Фосфорная кислота является трехосновной, при этом
рKа , 2 – рKа , 1 > 4 и рKа , 3 – рKа , 2 > 4, поэтому H3PO4 титруется ступенчато. Однако рKа , 3 > 9, поэтому третий скачок на кривой титрования отсутствует.
Фосфорная кислота оттитровывается с метиловым оранжевым по первой ступени:
H3PO4 + NaOH = NaH2PO4 + H2O Þ f экв(H3PO4) = 1
а с фенолфталеином – по двум ступеням:
H3PO4 + 2NaOH = Na2HPO4 + 2H2O Þ f экв(H3PO4) = 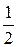
Смесь кислот H2SO4 и H3PO4. Раздельное определение компонентов этой смеси основано на титровании щелочью с применением двух индикаторов.
Одну аликвоту анализируемого раствора титруют с индикатором метиловым оранжевым, при этом оттитровывается сильная кислота H2SO4, а также H3PO4 по первой ступени:
H2SO4 + 2NaOH = Na2SO4 + 2H2O
H3PO4 + NaOH = NaH2PO4 + H2O
Вторую аликвоту титруют с индикатором фенолфталеином, при этом оттитровывается сильная кислота H2SO4, а также H3PO4 по двум ступеням:
H2SO4 + 2NaOH = Na2SO4 + 2H2O
H3PO4 + 2NaOH = Na2НPO4 + 2H2O
Смесь H3PO4 и NaH2PO4. Раздельное определение компонентов этой смеси основано на титровании щелочью с применением двух индикаторов.
Одну аликвоту анализируемого раствора титруют с индикатором метиловым оранжевым, при этом оттитровывается H3PO4 по первой ступени:
H3PO4 + NaOH = NaH2PO4 + H2O
Вторую аликвоту титруют с индикатором фенолфталеином, при этом оттитровывается H3PO4 по двум ступеням и соль NaH2PO4 по одной ступени:
H3PO4 + 2NaOH = Na2HPO4 + 2H2O
NaH2PO4 + NaOH = Na2НРO4 + H2O
Оборудование и реактивы: мерная колба, пипетка, бюретка, конические колбы, стандартный раствор щелочи, индикаторы метиловый оранжевый и фенолфталеин.
Выполнение работы. В мерную колбу получают у лаборантов анализируемый раствор, доводят дистиллированной водой до метки и тщательно перемешивают.
Проба А. Щавелевая кислота. Пипеткой переносят аликвотную часть раствора в коническую колбу. Далее добавляют 1–2 капли фенолфталеина и проводят титрование стандартным раствором щелочи. Титрование прекращают, как только появится неисчезающая розовая окраска раствора. Титрование повторяют не менее 3 раз при условии, что D V ≤ 0,1 мл. По результатам титрования рассчитывают массу кислоты Н2С2O4 × 2H2O в анализируемом растворе (г).
Проба Б. Фосфорная кислота. Пипеткой переносят аликвотную часть раствора в коническую колбу. Далее добавляют 1–2 капли выбранного индикатора – метилового оранжевого или фенолфталеина и проводят титрование стандартным раствором. Титрование с метиловым оранжевым прекращают, как только произойдет резкое изменение окраски раствора, а с фенолфталеином – когда появится неисчезающая розовая окраска. Титрование повторяют не менее 3 раз при условии, что D V ≤ 0,1 мл. По результатам титрования рассчитывают массу кислоты H3PO4 в анализируемом растворе (г).
Пробы В, Г. Смеси H2SO4 и H3PO4, H3PO4 и NaH2PO4. Пипеткой переносят аликвотную часть раствора в коническую колбу, добавляют 1–2 капли индикатора метилового оранжевого и проводят титрование приготовленным раствором щелочи с точно известной концентрацией. Титрование прекращают, как только произойдет резкое изменение окраски раствора. Титрование повторяют не менее 3 раз при условии, что D V ≤ 0,1 мл.
Пипеткой переносят другую аликвотную часть раствора в чистую коническую колбу, добавляют 1–2 капли индикатора фенолфталеина и проводят титрование приготовленным раствором щелочи с точно известной концентрацией. Титрование прекращают, как только появится неисчезающая розовая окраска. Титрование повторяют не менее 3 раз при условии, что D V ≤ 0,1 мл.
По результатам титрования рассчитывают объем щелочи, пошедший на реакцию с каждым из компонентов смеси, а затем их массы в анализируемом растворе (г).
| & | М (Н2С2О4 · 2Н2O) = 126,066 г/моль | М (H2SO4) = 98,08 г/моль |
| М (Н3РO4) = 97,995 г/моль | М (NaH2PO4) = 119,977 г/моль | |
| : | 1. С использованием ПО «Расчет кривых кислотно-основного титрования » провести компьютерный расчет кривых титрования: · Н2С2О4 щелочью (при анализе пробы А), · Н3РO4 щелочью (при анализе проб Б, Г), · Н3РO4 и H2SO4 щелочью (при анализе пробы В) с использованием кнопки Добавить для сравнения и переходом к сводному графику на листе Моделирование. Объяснить вид полученных кривых и обосновать использование индикаторов метилового оранжевого и фенолфталеина, в т. ч. при титровании смесей веществ. 2. С использованием ПО «Практикум по АХ и ФХМА »: – оценить неопределенность измерений; – провести Q -тест и статистическую обработку результатов анализа, если имеется 4 и более результатов параллельных измерений. |