Из курса химии за 8й класс мы знаем, что для измерения количеств веществ, участвующих в химических реакциях, была выбрана особая еденица – моль. Чтобы отмерять один моль вещества, нужно взять столько граммов его, какова относительная молекулярная масса его.
Например, 1моль воды (H2O) равен 18 граммам (1+1+16=18), моль кислорода (O2) – 32 грамма, а моль железа (Fe) – 56 грамм.Но что особенно для нас важно, установлено, что 1 моль любого вещества всегда содержит одинаковое число молекул.
Моль – это такое количество вещества, в котором содержится 6´1023 молекул этого вещества.
В честь итальянского ученого А. Авогадро это число (N)называется постоянной Авогадро или числом Авогадро.
Из формулы 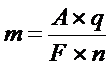 следует, что если q=F, то
следует, что если q=F, то 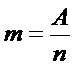 . Это значит что при прхождении через электролит заряда равного 96400 кулонам, выделится
. Это значит что при прхождении через электролит заряда равного 96400 кулонам, выделится  граммов любого вещества. Иначе говоря, для выделения одного моля одновалентного вещества через электролит должен протечь заряд q=F кулонов. Но мы знаем, что в любом моле вещества содержится одно и то же число его молекул – N=6x1023. Это позволяет нам вычислить заряд одного иона одновалентного вещества – элементарный электрический заряд – заряд одного (!) электрона:
граммов любого вещества. Иначе говоря, для выделения одного моля одновалентного вещества через электролит должен протечь заряд q=F кулонов. Но мы знаем, что в любом моле вещества содержится одно и то же число его молекул – N=6x1023. Это позволяет нам вычислить заряд одного иона одновалентного вещества – элементарный электрический заряд – заряд одного (!) электрона:
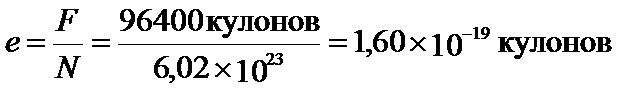
Применение электролиза
Электролитический метод получения чистых металлов (рафинирование, аффинаж). Электролиз, сопровождающийся растворением анода
Хорошим примером является электролитическое очищение (рафинирование) меди. Полученная непосредственно из руды медь отливается в виде пластин и помещается в качестве анода в раствор CuSO4. Подбирая напряжение на электродах ванны (0,20-0,25в), можно добиться, чтобы на катоде выделялась только металлическая медь. При этом посторонние примеси либо переходят в раствор (без выделения на катоде), либо выпадают на дно ванны в виде осадка («анодный шлам»). Катионы вещества анода соединяются с анионом SO42-, а на катоде при этом напряжении выделяется только металлическая медь. Анод как бы «растворяется». Такая очистка позволяет добится чистоты 99,99% («четыре девятки»). Аналогично (аффинаж) очищают и драгоценные металлы (золото Au, серебро Ag).
В настоящее время весь алюминий (Al) добывается электролитически (из расплава бокситов).
Гальванотехника
Гальванотехника – область прикладной электрохимии, занимающаяся процессами нанесения металлических покрытий на поверхность как металлических, так и неметаллических изделий при прохождении постоянного электрического тока через растворы их солей. Гальванотехника пожразделяется на гальваностегию и гальванопластику.
Посредством электролиза можно покрыть металлические предметы слоем другого металла. Этот процесс называется гальваностегией. Особое техническое значение имеют покрытия трудноокисляемыми металлами, в частности никелирование и хромирование, а также серебрение и золочение, часто применяемые для защиты металлов от коррозии. Для получения нужных покрытий предмет тщательно очищяют, хорошо обезжиривают и помещают как катод в электролитическую ванну, содержащую соль того металла, которым желают покрыть предмет. Для более равномерного покрытия полезно применять две пластины в качестве анода, помещая предмет между ними.

Также посредством электролиза можно не только покрыть предметы слоем того или иного металла, но и изготовить их рельефные металлические копии (например, монет, медалей). Этот процесс был изобретен русским физиком и электротехником, членом Российской Академии наук Борисом Семеновичем Якоби (1801-1874) в сороковых годах XIXвека и называется гальванопластикой. Для изготовления рельефной копии предмета сначала делают слепок из какого-либо пластичного материала, например из воска. Этот слепок натирают графитом и погружают в электролитическую ванну в качестве катода, где на нём и осаждается слой металла. Это применяется в полиграфии при изготовлении печатных форм.
Кроме указанных выше, электролиз нашел применение и в других областях:
ü получение оксидных защитных пленок на металлах (анодирование);
ü электрохимическая обработка поверхности металлического изделия (полировка);
ü электрохимическое окрашивание металлов (например, меди, латуни, цинка, хрома и др.);
ü очистка воды – удаление из нее растворимых примесей. В результате получается так называемая мягкая вода (по своим свойствам приближающаяся к дистиллированной);
ü электрохимическая заточка режущих инструментов (например, хирургических ножей, бритв и т.д.).
Список использованной литературы:
1. Гуревич А. Е. «Физика. Электромагнитные явления. 8 класс» Москва, Издательский дом «Дрофа». 1999 год.
2. Габриэлян О. С. «Химия. 8 класс» Москва, Издательский дом «Дрофа». 1997 год.
3. «Элементарный учебник физики под редакцией академика Г. С. Ландсберга - ТомII – электричество и магнетизм». Москва, «Наука» 1972 год.
4. Eric M. Rogers. «Physics for the Inquiring Mind (the methods, nature and phylosophyof physical science)».«PrinsetonUniversitypress» 1966. ТомIII – электричество и магнетизм. Перевод Москва, «Мир» 1971 год.
5. А. Н. Ремизов «Курс физики, электроники и кибернетики для медицинских институтов». Москва, «Высшая школа» 1982 год.