Часть V
«Витамины»
Минск МГЭУ
Теоретическая часть
Витамины
Витамины (от латинского «Vita» – жизнь) – низкомолекулярные органические соединения различной химической природы, необходимые для осуществления жизненно важных биохимических и физиологических процессов в живых организмах. Организм человека и животных не синтезирует витамины или синтезирует в недостаточном количестве, поэтому он должен получать их в готовом виде с пищей. Витамины обладают исключительно высокой биологической активностью и требуются организму в очень небольших количествах – от нескольких мкг до нескольких мг в день.
Витамины, участвующие в биохимических процессах, являются предшественниками коферментов (витамин В1) или собственно коферментами (липоамид). Некоторые витамины обеспечивают осуществление физиологических процессов, например: витамин А2 участвует в процессе зрительного восприятия; витамин А3 – в процессе дифференцировки клеток; витамин D – в процессе формирования костной ткани; витамин Е – антиоксидант.
Наряду с витаминами, необходимость которых для человека и животных бесспорно установлена, в пище содержатся биологически активные вещества, которые по своим функциям ближе не к витаминам, а к другим незаменимым пищевым веществам. Эти вещества называют витаминоподобными. К ним обычно относят биофлавоноиды, холин, инозит, оротовую, пангамовую и пара-аминобензойную кислоты, полиненасыщенные жирные кислоты и др.
Соединения, которые не являются витаминами, но могут служить предшественниками их образования в организме, называются провитаминами. К ним относятся, например, каротины, расщепляющиеся в организме с образованием витамина А, и некоторые стерины (эргостерин, 7-дегидрохолестерин и др.), превращающиеся в витамин D.
Некоторые аналоги и производные витаминов способны занимать место витамина в активном центре фермента, однако при этом не способны выполнять коферментную функцию, что ведет к снижению активности данного фермента и развитию соответствующей витаминной недостаточности. Такие соединения называются антивитаминами. Так, например, производные 4-гидроксикумарина (дикумарин и др.), преду-преждающие возникновение тромбов, – антагонисты витамина К. Суль-фаниламидные препараты, оказывающие бактериостатическое действие,– антагонисты пара-аминобензойной кислоты; аминоптерин и метотрексат (противоопухолевые препараты) – антагонисты фолиевой кислоты. К антивитаминам относятся также вещества, связывающие или разрушающие витамины, например ферменты тиаминаза I и II, инактивирующие тиамин; белок яйца авидин, связывающий биотин.
Ряд витаминов представлен не одним, а несколькими соединениями, обладающими сходной биологической активностью (витамеры), например, витамин В6 включает пиридоксин, пиридоксаль и пиридоксамин. Для бозна-чения подобных групп родственных соединений используют слово «витамин» с буквенными обозначениями (витамин А, витамин Е и т.д.).
Для индивидуальных соединений, обладающих витаминной активностью, рекомендуется использовать рациональные названия, отражающие их химическую природу, например рибофлавин (витамин В2), никотинамид и никотиновая кислота (витамин РР), ретинол (витамин А1).
Витамины классифицируют по их растворимости, а именно различают водорастворимые (гидрофильные) и жирорастворимые (липофильные) вита-мины. С момента открытия первых витаминов и до настоящего времени используется буквенная классификация.
Основной специфической функцией водорастворимых витаминов в организме является образование коферментов. Из жирорастворимых витаминов лишь витамины К и А2 осуществляют коферментную функцию, а остальные участвуют не в ферментативных реакциях, а в различных физиологических процессах.
Знание функций витаминов позволяет понять причину возникновения различных патологических состояний, связанных с нарушением ме-таболизма веществ. Общим положением является то, что дефицит того или иного витамина приводит к снижению активности соответствующего фермента и, следовательно, к торможению ферментативной реакции. Поскольку организм является сбалансированной саморегулирующейся системой, изменение метаболизма какого-либо вещества влечет за собой изменение обмена и других метаболитов. Наблюдаемые изменения организма в целом проявляются не сразу, поскольку организм в начальном этапе дефицита какого-либо витамина компенсирует возникшее отклонение, изменяя метаболизм других веществ так, чтобы снизить отрицательное влияние дефицита витамина (состояние гиповитаминоза). Если дефицит витамина устранен, организм возвращается в нормальное состояние. В том случае, если дефицит витамина большой и длится длительное время, возникает авитаминоз, и когда компенсаторные ресурсы организма исчерпаны наступает летальный исход.
I. Химическое строение и биохимические свойства жирорастворимых витаминов
1.1. Витамин А (ретинол)
Антиксерофтальмический
Жирорастворимый витамин А представляет собой циклический непредельный одноатомный спирт, состоящий из ретинолового кольца и боковой цепи из 2-х остатков изопрена и первичной спиртовой группы.
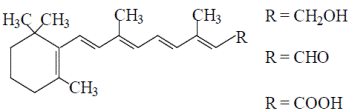
Спиртовая форма витамина А, ретинола, в организме окисляется до ретиналя (R=CHO) и ретиноевой кислоты (R=COOH)
Биохимическая функция в организме
Витамин А может образовываться в слизистой кишечника и печени из провитаминов — α-, β- и γ- каротинов под воздействием каротиноксигеназы. Наибольшей активностью обладает β- каротин (из него образуются две молекулы ретинола, из других — по одной).
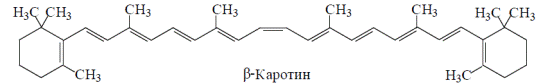
В организме ретинол превращается в ретиналь и ретиноевую кислоту, участвующие в регуляции ряда функций:
1. Ретинол является структурным компонентом клеточных мембран;
2. Регулирует рост и дифференцировку клеток эмбриона и молодого организма, а также деление и дифференцировку быстро проли-ферируюших тканей, в первую очередь, эпителиальных, хряща и костной ткани. Он контролирует синтез белков цитоскелета, реакции распада и синтеза гликопротеинов. Синтез последних осуществляется в аппарате Гольджи. Недостаток витамина А приводит к нарушению синтеза гликопротеинов (точнее, реакций гликозилирования, т. е. присоединения углеводного компонента к белку), что проявляется потерей защитных свойств слизистых оболочек.
3. Является важнейшим компонентом антиоксидантной защиты организма.
4. Витамин А и ретиноиды стимулируют реакции клеточного иммунитета, в частности, увеличивают активность Т-киллеров.
5. Витамин А является антиканцерогеном, так как при его недостатке в организме увеличивается заболеваемость раком легкого и раком других локализаций.
6. Участвует в фотохимическом акте зрения.
Участие витамина А в процессе зрения
Светочувствительный аппарат глаза - сетчатка. Падающий на сетчатку свет адсорбируется и трансформируется пигментами сетчатки в другую форму энергии. У человека сетчатка содержит 2 типа рецепторных клеток: палочки и колбочки. Первые реагируют на слабое (сумеречное) освещение, а колбочки - на хорошее освещение (дневное зрение). Палочки содержат зрительный пигмент родопсин, а колбочки - йодопсин. Оба пигмента - сложные белки, отличающиеся своей белковой частью. В качестве кофермента оба белка содержат 11-цисретиналь, альдегидное производное витамина А.

Рис.1 Схема зрительного цикла: 1 - цис-ретиналь в темноте соединяется с белком опсином, образуя родопсин; 2 - под действием кванта света происходит фотоизомеризация 11-цисретинапя в транс-ретиналь; 3 - транс-ретиналь-опсин распадается на транс-ретиналь и опсин; 4 - поскольку пигменты встроены в мембраны светочувствительных клеток сетчатки, это приводит к местной деполяризации мембраны и возникновению нервного импульса, распространяющегося по нервному волокну; 5 - заключительный этап этого процесса - регенерация исходного пигмента. Это происходит при участии ретиналь-изомеразы.
1.2. Витамин Е (токоферол)
Антистерильный
По химической природе витамин Е представляет собой группу родственных соединений — токоферолов, молекулы которых состоят из двух компонентов: кольца, являющегося производным бензохинона, и изопреноидной боковой цепи. Кроме токоферолов к группе витамина Е относятся α-, β-, γ- и δ- токотриенолы — аналоги соответствующих токоферолов, которые отличаются от последних наличием двойных связей в боковой цепи. Наибольшую биологическую активность проявляет α-токоферол (от греч. tokos — потомство, phero — несу).

Токоферолы синтезируются только в растениях.
Биохимическая функция в организме
Витамин Е является универсальным протектором клеточных мембран от окислительного повреждения. Он занимает такое положение в мембране, которое препятствует контакту кислорода с ненасыщенными липидами мембран (образование гидрофобных комплексов). Это защищает биомембраны от их перекисной деструкции. Антиоксидантные свойства токоферола обусловлены также способностью подвижного гидроксила хроманового ядра его молекулы непосредственно взаимодействовать со свободными радикалами кислорода (О 2 •, НО• НО•), свободными радикалами ненасыщенных жирных кислот (RO•, RO 2 •) и перекисями жирных кислот. Мембраностабилизируюшее действие витамина проявляется и в его свойстве предохранять от окисления SH-группы мембранных белков. Его антиоксидантное действие заключается также в способности защищать от окисления двойные связи в молекулах каротина и витамина А. Витамин Е (совместно с аскорбатом) способствует включению селена в состав активного центра глутатионпероксидазы, тем самым он активизирует ферментативную антиоксидантную защиту (глутатионпероксидаза обезвреживает гидропероксиды липидов).
Токоферол является не только антиоксидантом, но и актигипоксантом, что объясняется его способностью стабилизировать митохондриальную мембрану и экономить потребление кислорода клетками. Следует отметить, что из всех клеточных органелл митохондрии наиболее чувствительны к повреждению, так как в них содержится больше всего легко окисляющихся ненасыщенных липидов. Вследствие мембраностабилизируюшего эффекта витамина Е в митохондриях увеличивается сопряженность окислительного фосфорилирования, образование АТФ и креатинфосфата. Важно также отметить, что витамин контролирует биосинтез убихинона — компонента дыхательной цепи и главного антиоксиданта митохондрий.
Токоферол контролирует синтез нуклеиновых кислот (на уровне транскрипции), а также гема, микросомных иитохромов и других гемсодержаших белков.
Витамин Е обладает способностью угнетать активность фосфолипазы А2 лизосом, разрушающей фосфолипиды мембран. Повреждение мембран лизосом приводит к выходу в цитозоль протеолитических ферментов, которые и повреждают клетку.
Витамин Е является эффективным иммуномодулятором, способствующим укреплению иммунозащитных сил организма.
1.3. Витамин Д (кальциферол)
антирахитический
Кальциферолы - группа химически родственных соединений, относящихся к производным стеринов. Наиболее биологически активные витамины - D2 и D3. Витамин D2 (эргокальциферол), производное эргостерина - растительного стероида, встречающегося в некоторых грибах, дрожжах и растительных маслах.

При облучении пищевых продуктов УФО из эргостерина получается витамин D2, используемый в лечебных целях. Витамин D3, имеющийся у человека и животных, - холекальциферол, образующийся в коже человека из 7-дегидрохолестерина под действием УФ-лучей.
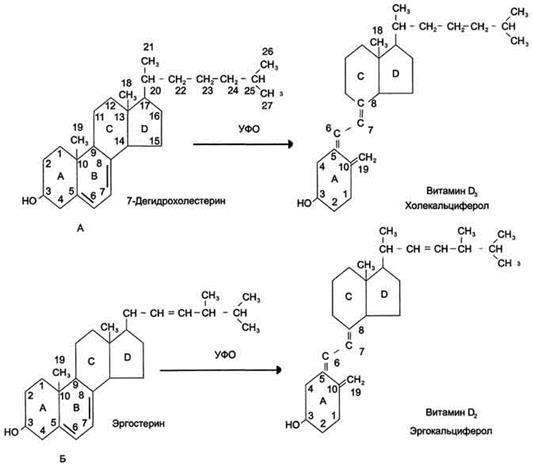
Рис.2 Схема синтеза витаминов D2и D3. Провитамины D2 и D3 - стерины, у которых в кольце В две двойные связи. При воздействии света в процессе фотохимической реакции происходит расщепление кольца В. А - 7-дегидрохолестерин, провитамин D3, (синтезируется из холестерина); Б - эргостерин - провитамин D2.
Биохимическая функция в организме
В организме человека витамин D 3 гидроксилируется в положениях 25 и 1 и превращается в биологически активное соединение 1,25-дигидроксихолекальциферол (кальцитриол).

Кальцитриол выполняет гормональную функцию, участвуя в регуляции обмена Са2+ и фосфатов, стимулируя всасывание Са2+ в кишечнике и кальцификацию костной ткани, реабсорбцию Са2+ и фосфатов в почках. При низкой концентрации Са2+ или высокой концентрации D 3 он стимулирует мобилизацию Са2+ из костей.
Кальцитриол принимает участие в регуляции роста и дифференцировке клеток костного мозга. Он обладает антиоксидантным и антиканцерогенным действием.
1.4. Витамин К (нафтохиноны)
антигеморрагический
Витамин К по химической природе представляет производное нафтохинонов. Существует в нескольких формах в растениях как филлохинон (К1), в клетках кишечной флоры как менахинон (К2). Они различаются строением и количеством изопреновых единиц в боковой цепи.

Синтезированы аналоги витамина К — менадион (витамин К3, лишенный боковой цепи) и его водорастворимый аналог викасол, последний широко применяется в медицинской практике.
В тканях образуется активная форма витамина — менахинон-4 (содержит четыре изопреноидные единицы).
Биохимическая функция в организме
Витамин К является коферментом γ-глутаматкарбоксилазы, карбокси-лирующей глутаминовую кислоту с образованием γ-карбоксиглутаминовой кислоты. γ-глутаматкарбоксилаза участвует в активации факторов свёртывания крови: протромбина (фактор II), проконвертина (фактор VII), фактора Кристмаса (фактор IX) и фактора Стюарта (фактор X). Эти белковые факторы синтезируются как неактивные предшественники. Один из этапов активации их - карбоксилирование по остаткам глутаминовой кислоты с образованием γ -карбоксиглутаминовой кислоты, необходимой для связывания ионов кальция.
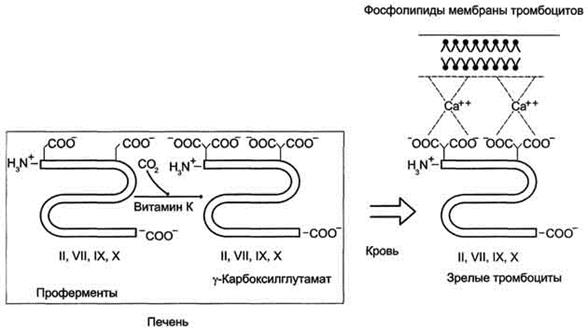
Рис.3. Роль витамина К в свёртывании крови.
II. Химическое строение и биологическая роль водорастворимых витаминов
2.1. Витамин B1 (тиамин)
антиневритный
Тиамин по химической природе представляет производное тиазола и пиримидина, соединенных метиленовым мостиком.
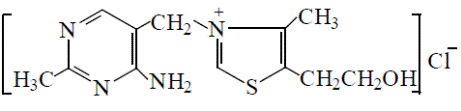
Витамин В 1, присутствует в различных органах и тканях как в форме свободного тиамина, так и его фосфорных зфиров: тиаминмонофосфата (ТМФ), тиаминдифосфата (ТДФ, синонимы: тиаминпирофосфат, ТПФ) и тиаминтрифосфата (ТТФ).
Основной коферментной формой (60—80 % от общего внутриклеточного) является ТПФ.
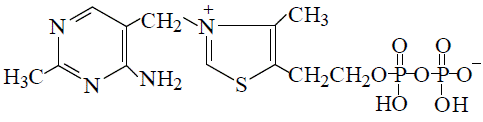
Биохимическая функция в организме
Участие ТПФ в реакции прямого декарбоксилирования пировиноградной кислоты (ПВК).
При декарбоксилировании ПВК с помощью пируватдекарбоксилазы бразует-ся ацетальдегид, который под воздействием алкогольдегидрогеназы превра-щается в этанол. ТПФ является незаменимым кофактором пируватдекарбо-ксилазы.
Участие ТПФ в реакциях окислительного декарбоксилирования.
Окислительное декарбоксилирование пируватакатализирует пируват-дегидрогеназа. В состав пируватдегидрогеназного комплекса входит несколько структурно связанных ферментных белков и коферментов. ТПФ катализирует начальную реакцию декарбокси-лирования ПВК.
Окислительное декарбоксилирование ПВК является одной из ключевых реакций в обмене углеводов. В результате этой реакции ПВК, образовавшаяся при окислении глюкозы, включается в главный метаболический путь клетки — цикл Кребса, где окисляется до углекислоты и воды с выделением энергии. Таким образом, благодаря реакции окислительного декарбоксилирования ПВК создаются условия для полного окисления углеводов и утилизации всей заключенной в них энергии. Кроме того, образующаяся при действии ПДГ-комплекса активная форма уксусной кислоты служит источником для синтеза многих биологических продуктов: жирных кислот, холестерина, стероидных гормонов, ацетоновых тел и других.
Окислительное дскарбоксилирование а-кетоглутатарата катализирует а-кетоглутаратдегидрогеназа. Этот фермент является составной частью цикла Кребса. Строение и механизм действия а -кетоглугаратдегидрогеназного комплекса схожи с пируватдегидрогеназой, т. е. ТПФ также катализирует начальный этап превращения кетокислоты. Таким образом, от степени обеспеченности клетки ТПФ зависит бесперебойная работа этого цикла.
Помимо окислительных превращений пирувата и а -кетоглутарата, ТПФ принимает участие в окислительном декарбоксилировании кетокислот с разветвленным углеродным скелетом (продукты дезаминирования валина, изолейцина и лейцина). Эти реакции играют важную роль в процессе утилизации аминокислот и, следовательно, белков клеткой.
ТПФ — кофермент транскетолазы.
Транскетолаза — фермент пентозофосфатного пути окисления углеводов
Физиологическая роль этого пути заключается в том, что он является основ
ным поставщиком NADFH•H+ и рибозо-5-фосфата. Транскетолаза переносит
двууглеродные фрагменты от ксилулозо-5-фосфата к рибозо-5-фосфату, что
приводит к образованию триозофосфата (3-фосфоглицеринового альдегида)
и С 7 сахара (седогептулозо-7-фосфата). ТПФ необходим для стабили-зации
карбаниона, образующегося при расщеплении связи С 2 -С 3 ксилулозо-5-
фосфата.
Участие в синтезе ацетилхолина.
ТПФ катализирует в пируватдегидрогеназной реакции образование ацетил-КоА — субстрата ацетилирования холина.
Помимо участия в ферментативных реакциях, тиамин может выполнять и некоферментные функции. Полагают, что тиамин участвует в кроветворении, на что указывает наличие врожденных тиаминзависимых анемий, поддающихся лечению высокими дозами этого витамина, а также в стероидогенезе.
2.2. Витамин B 2 (рибофлавин)
Витамин роста
Витамин В 2 отличается от других витаминов желтым цветом (iflavus — желтый). Однако, в отличие от окисленной желтой, восстановленная форма витамина бесцветна.
Молекула рибофлавина по химической природе представляет собой производное изоаллоксазина, связанного с пятиатомным спиртом рибитолом. Термином флавины обозначаются многие производные изоаллоксазина, обладающие В 2 -витаминной активностью.

Биосинтез флавинов осуществляется растительными и многими бактериальными клетками, а также плесневыми грибками и дрожжами. Благодаря микробному биосинтезу рибофлавина в желудочно-кишечном тракте жвачные животные не нуждаются в этом витамине. У других животных и человека синтезирующихся в кишечнике флавинов недостаточно для предупреждения гиповитаминоза. В пище витамин В 2 находится преимущественно в составе своих коферментных форм – FMN (флавинмоно-нуклеотида) и FAD (флавинадениндинуклеотида).
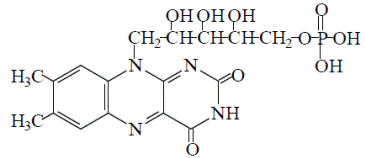

Биохимическая функция в организме
Основное значение витамина В 2 состоит в том, что он входит в состав флавиновых коферментов — FMN и FAD. Роль этих коферментов заключается в следующем:
FMN и FAD — коферменты оксидаз, переносящих электроны и Н+ с окисляемого субстрата на кислород. Таковыми являются ферменты, участвующие в распаде аминокислот (оксидазы D- и L-аминокислот), нуклеотидов (ксантиноксидаза), биогенных аминов (моно- и диаминоксидазы) и другие.
FMN и FAD — промежуточные переносчики электронов и протонов в дыхательной цепи: FМN входит в состав I-го комплекса цепи тканевого дыхания, FAD — в состав II-го комплекса.
FAD — кофермент пируват- и α-кетоглутаратдегидрогеназных комплексов (наряду с ТПФ и другими коферментами FAD осуществляет окислительное дскарбоксилированис соответствующих кетокислот), а также единственный кофермеит сукцинатдегидрогеназы (фермента цикла Кребса). Таким образом, рибофлавин принимает активное участие в работе главного метаболического пути клетки.
FAD — участник реакций окисления жирных кислот в митохондриях (он является коферментом ацил-КоА-дегидрогеназы).
2.3. Витамин B 3 (пантотеновая кислота).
Витамин В 3, широко распространен в природе, отсюда и его название — пантотеновая кислота (от panthos — повсюду). Пантотеновая кислота состоит из остатков D-2,4-дигидрокси-3,3-диметилмасляной кислоты и β-аланина, соединённых между собой амидной связью:

Коферментными формами витамина В 3, образующимися в цитоплазме клеток, являются 4′-фосфопантетеин и KoA-SH.

В кишечнике человека пантотеновая кислота в небольших количествах продуцируется кишечной палочкой. Пантотеновая кислота - универсальный витамин, в ней или её производных нуждаются человек, животные, растения и микроорганизмы.
Биохимическая функция в организме
Значение пантотеновой кислоты определяется исключительно важной ролью ее коферментных форм в ключевых реакциях метаболизма. Производные витамина, такие как S-сульфопантетеин, способны поддерживать рост бифидо-бактерий — важного компонента биоценоза кишечника.
4′-фосфопантетеин является активной субъединицей ацилпереносящего белка (АПБ) синтазы жирных кислот — представителя класса так называемых фосфопантетеинпротеинов.
Ацетил-КоА является субстратом для синтеза жирных кислот, холестерина и стероидных гормонов, ацетоновых тел, ацетилхолина, ацетилгюкозаминов. С него начинаются реакции главного метаболического пути клетки — цикла Кребса.
Ацетил-КоА принимает участие в реакциях обезвреживания (ацетилирование биогенных аминов и чужеродных соединений).
Ацетил-КоА участвует в активировании жирных кислот с образованием ацил-КоА. Ацил-КоА используется для синтеза липидов; для транспорта жирных кислот в митохондрии.
2.4. Витамин B5 (РР никотиновая кислота, никотинамид)
антипеллагрический
Никотиновая кислота является пиридин-3-карбоновой кислотой, никотинамид — ее амидом. Оба соединения в организме легко превращаются друг в друга и поэтому обладают одинаковой витаминной активностью.
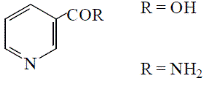
В тканях оба соединения преимущественно используются для синтеза коферментных форм — NAD и NADP.
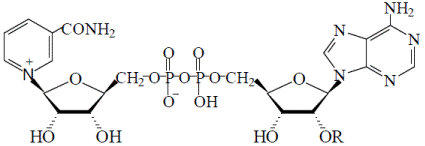
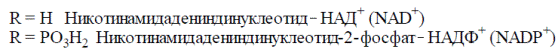
Биохимическая функция в организме
Почти весь имеющийся в клетках и жидких средах организма витамин РР представлен в виде никотинамида, включенного в состав коферментов — NAD и NADP.
NAD+ — кофермент дегидрогеназ, участвующий в реакциях окисления глюкозы, жирных кислот, глицерина, аминокислот, является коферментом дегидрогеназ цикла Кребса (исключая сукцинатдегидрогеназу). В этих реакциях кофермент выполняет функцию промежуточного акцептора электронов и протонов.
NAD+ — переносчик протонов и электронов в дыхательной цепи митохондрий (от окисляемого субстрата к первому комплексу цепи тканевого дыхания).
NAD+ — субстрат ДНК-лигазной реакции при синтезе и репарации ДНК, а также субстрат для синтеза поли-АДФ-рибозы в поли- (АДФ) -рибозилировании белков хроматина.
NADPH•H+ — донор водорода в реакциях синтеза жирных кислот, холестерина, стероидных гормонов и некоторых других соединений.
NADPH•H+ — компонент монооксигеназной цепи микросомного окисления, выполняющей функцию дстоксикации антибиотиков и других чужеродных веществ.
NAD+ и NADPH•H+ являются аллостерическими регуляторами ферментов энергетического обмена, в частности, ферментов цикла Кребса, а также реакций глюконеогенеза.
Никотинамид и N-метилникотинамид (метаболит никотинамида) являются участниками процесса метилирования т-РНК и белков.
2.5. Витамин B6 (пиридоксин, пиридоксаль,
пиридоксамин)
антидерматитный
Витамин В 6 включает группу трех природных производных пиридина, обладающих одинаковой витаминной активностью: пиридоксина, пиридоксаля, пиридоксамина, отличающихся друг от друга наличием соответственно спиртовой, альдегидной или аминогруппы.
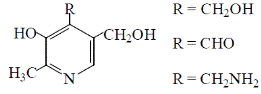
Коферментные функции выполняет фосфорилированное производное пиридоксина: пиридоксальфосфат.
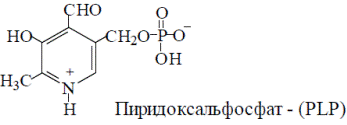
Биохимическая функция в организме
Витамин В 6 часто называют «королем обмена аминокислот»; вместе с тем его коферментные формы участвуют в реакциях, катализируемых почти всеми классами ферментов.
Коферментные формы витамина В6 входят в состав следующих ферментов:
аминотраисфераз аминокислот, катализирующих обратимый перенос NH 2 -группы от аминокислоты на α -кетокислоту, при этом образуются новые α -кетокислоты и заменимые аминокислоты;
декарбоксилаз аминокислот, отщепляющих карбоксильную группу аминокислот, что приводит к образованию биогенных аминов (гистамина, серотонина, ГАМК и других), а также моноаминоксидаз, гистаминазы (диаминооксидаза) и аминотрансферазы ГАМК, обезвреживающих (окисляющих) биогенные амины;
изомераз аминокислот, с помощью которых организм разрушает D-аминокислоты (в состав тканевых белков млекопитающих входят L-аминокислоты);
синтазы δ- аминолевуленовой кислоты, участвующей в биосинтезе гема гемоглобина и других гемсодержащих белков; ферментов, обеспечивающих синтез витамина РР из триптофана; цистеина из серина и гомоцистеина;
фермента, участвующего в реакциях биосинтеза сфинголипидов (из серина и пальмитил-КоА).
Таким образом, витамин В 6 характеризуется исключительно широким спектром биологического действия. Он принимает участие в регуляции белкового, углеводного и липидного обмена, биосинтезе гема и биогенных аминов, гормонов щитовидной железы и других биологически активных соединений. Помимо каталитического действия, пиридоксальфосфат участвует в процессе активного транспорта некоторых аминокислот через клеточные мембраны, ему присуща функция регулятора конформационного состояния гликогенфосфорилазы — главного регулируемого фермента, осуществляющего распад гликогена.
2.6. Витамин В 9 (Фолиевая кислота, витамин Вc)
антианемический
Фолиевая кислота (лат. folium — лист) состоит из трёх структурных единиц: остатка птеридина, парааминобензойной и глутаминовой кислот.
. Витамином В c это соединение назвали из-за его способности излечивать анемию у цыплят (от англ. chicken — цыпленок).
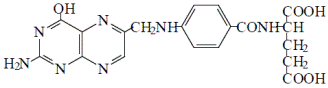
В организме человека птеридиновое кольцо не синтезируется, поэтому удовлетворение потребности в фолиевой кислоте полностью зависит от его поступления с пищей.
Витамин В 9, всасываясь в тонком кишечнике, восстанавливается в энтероцитах до активной формы - тетрагидрофолиевой кислоты (ТГФК) и N5-метил-ТГФК.
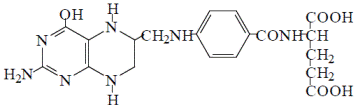
Биохимическая функция в организме
Коферментная форма фолиевой кислоты — ТГФК — необходима для мобилизации и использования в реакциях метаболизма одноуглеродных функциональных групп: метильной (-СН 3), метиленовой (-СН 2 -), метенильной (-СН=), формальной (-СНО) и формиминогруппы (CH=NH). Присоединение этих групп к 5-му или 10-му атому азота ТГФК осуществляется ферментативно.
Важнейшими реакциями с участием одноуглеродных фрагментов, связанных с ТГФК, являются:
1. 5,10-метенил-ТГФК и 10-формил ТГФК служат донорами соответствующих одноуглеродных радикалов при синтезе пуриновых нуклеотидов;
2. 5-метил-ТГФК вместе с витамином В12 участвуют в переносе метильной группы в реакциях синтеза дТМФ и метионина;
3. ТГФК вовлекается в метаболизм аминокислот: серина, глицина и метионина.
2.7. Витамин В12 (Кобаламин)
антианемический
Структура витамина В 12 отличается от строения всех других витаминов своей сложностью и наличием в его молекуле иона металла — кобальта. Кобальт связан координационной связью с четырьмя атомами азота, входящими в состав порфириноподобной структуры (называемой корриновым ядром), и с атомом азота 5,6-диметилбензимидазола. Кобальтсодержащсе ядро молекулы представляет собой плоскостную структуру с перпендикулярно расположенным к ней нуклеотидом. Последний, помимо 5,6-диметилбензимидазола, содержит рибозу и фосфорную кислоту (циановая группа, связанная с кобальтом, присутствует только в очищенных препаратах витамина, в клетке она замешается водой или гидроксильной группой). Из-за присутствия в молекуле витамина кобальта и амидного азота это соединение получило название кобаламин.

Биохимическая функция в организме
Витамин В12 служит источником образования двух коферментов: метилкобаламина в цитоплазме и дезоксиаденозилкобаламина в митохондриях.
Метилкобаламин - кофермент, участвующий в образовании метионина из гомоцистеина. Кроме того, он принимает участие в превращениях производных фолиевой кислоты, необходимых для синтеза нуклеотидов - предшественников ДНК и РНК.
Дезоксиаденозилкобаламин в качестве кофермента участвует в метаболизме жирных кислот с нечётным числом углеродных атомов и аминокислот с разветвлённой углеводородной цепью.
2.8. Витамин Н (биотин)
антисеборейный
В основе строения биотина лежит тиофеновое кольцо, к которому присоединена молекула мочевины, а боковая цепь представлена валерьяновой кислотой.

N1-имидазольного кольца является местом карбоксилирования. Связываясь с ионом гидрокарбоната (НС03 -), биотин становится коферментом, называемым карбоксибиотином.
Биотин способен образовывать с авидином — гликопротеином белка куриного яйца — прочный комплекс, который не может расщепляться пищеварительными ферментами. Поэтому при частом употреблении сырых яиц прекращается всасывание присутствующего в пище биотина. Способность молекул авидина и биотина специфически связываться друг с другом используется в некоторых методах очистки в биотехнологии.
Биохимическая функция в организме
Витамин Н способствует усвоению тканями ионов бикарбоната и активирует реакции карбоксилирования и транскарбоксилирования в составе следующих карбоксибиотинил-ферментов:
1. Пируваткарбоксилазы — фермента, катализирующего АТФ-зависимое образование оксалоацетата из пирувата и НС03 -.

Пируваткарбоксилаза является тетрамерным белком, несущим четыре молекулы биотина, каждая из которых связана с остатком лизина апофермента. Пируваткарбоксилазная реакция является наиболее важной анаплеротической реакцией, особенно в печени и почках (к анаплеротическим относятся возмещающие, пополняющие, реакции). Так, пируваткарбоксилаза восполняет запас оксалоацетата, необходимый для функционирования цикла Кребса. Пируваткарбоксилаза является важным митохонлриальным ферментом глюконеогенеза (новообразования глюкозы).
2. Ацетил-КоА-карбоксилазы — первого фермента в реакциях
биосинтеза жирных кислот. Активная форма энзима представляет собой множество длинных мономерных нитей. При ферментативном катализе отдается карбоксильная группа бикарбоната ацетил-коэнзиму А с образованием малонил-КоА:
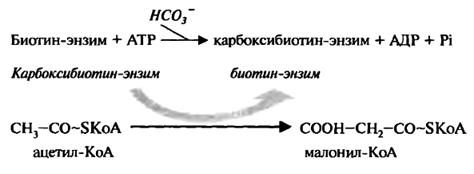
3. Пропионил-КоА-карбоксилазы — фермента, участвующего в окислении жирных кислот с нечетным числом атомов углерода. При этом происходит стереоспецифический перенос активированной карбоксильной группы от карбоксибиотина к пропионил-КоА с образованием метил малонил-КоА:
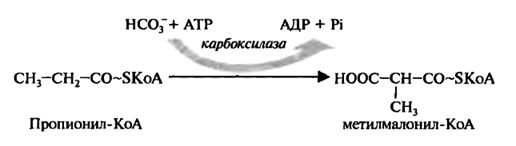
Следует отметить, что ион бикарбоната может утилизироваться клеткой без участия биотина, как, например, это имеет место в карбомоилфосфатсинтетазной реакции при синтезе пиримидинов:

4. Бета-метилкротоноил-КоА-карбоксилазы — фермента, участвующего в реакциях окислительного распада лейцина.
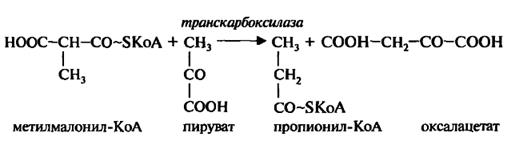
5. Метилмалонил-ЩУК-транскарбоксилазы — фермента, катализи-рующего реакцию транскарбоксилирования, а именно, обратимое превращение пирувата и оксалацетата (другие транскарбоксилазные реакции также протекают с участием биотина):
2.9. Витамин Р (биофлавоноиды)
Капилляроукрепляющий
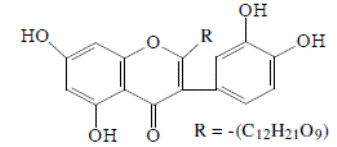
Биофлавоноиды – разнообразная группа растительных полифенольных соединений, в основе структуры которых лежит дифенилпропановый углеродный скелет.
Биохимическая функция в организме
Биофлавоноиды могут использоваться для построения биологически важных соединений в клетке, в частности убихинона. Витамин Р способствует стабилизации межклеточного матрикса соединительной ткани и уменьшению проницаемости капилляров.
Рутин и квертецин — полифенолы, обладающие Р- витаминной активностью, являются эффективными антиоксидантами.
Флавоноиды (катехины) зеленого чая способны оказывать выраженное цитопротекторное действие, в основе которого лежит их свойство перехватывать свободные радикалы кислорода. В отличие от витамина Е, биофлавоноиды кроме прямого антирадикального действия могут также связывать ионы металлов с переменной валентностью, ингибируя тем самым процесс ПОЛ (перекисного окисления липидов) биомембран. Наиболее эффективными ловушками супероксидного радикала кислорода (с которого начинается процесс ПОЛ) являются железокомплексы флавоноидов: например, комплекс рутина с Fe2+ почти в 5 раз активнее самого рутина.
2.10. Витамин С (аскорбиновая кислота)
антискорбутный
Аскорбиновая кислота - лактон кисло