1. В методах окислительно-восстановительного титрования чаще всего используют реакции:
A. Межатомного окисления-восстановления
B. Самоокисления-самовосстановления
C. Межмолекулярного и межионного окисления-восстановления
D. Внутримолекулярного окисления-восстановления
E. Реакции, происходящие с переносом электронов
2. Подберите расчетные формулы для соответствующих расчетов при титровании Fе(II) раствором KMnO4:
Потенциал системы до начала титрования
А. Е0МnO4-/Mn2++  lg
lg 
B. Е0Fe3+/Fe2+  lg
lg 
С.

D. 
3. Подберите расчетные формулы для соответствующих расчетов при титровании Fe(II) раствором KMnO4: потенциал системы в точке эквивалентности
А. Е0МnO4-/Mn2++  lg
lg 
В. Е0Fe3+/Fe2+  lg
lg 
С.

D. 
4. Подберите расчетные формулы для соответствующих расчетов при титровании Fe(II) раствором KMnO4: потенциал системы после точки эквивалентности
А. Е0МnO4-/Mn2++  lg
lg 
B. Е0Fe3+/Fe2+  lg
lg 
C.

D. 
5. Подберите расчетные формулы для соответствующих расчетов при титровании Fe(II) раствором KMnO4: константа равновесия реакции
А. Е0МnO4-/Mn2++  lg
lg 
B. Е0Fe3+/Fe2+  lg
lg 
С.

Д. 
6. Подберите расчётные формулы для соответствующих расчётов при титровании Fe(II) раствором KMnO4: потенциал системы в начале скачка титрования
А. Е0МnO4-/Mn2++  lg
lg 
B. Е0Fe3+/Fe2+  lg
lg 
С.

D. 
7. Найдите для каждого из указанных ниже титрантов характеристику его устойчивости и др. cвойства. Раствор калия дихромата
A. Устойчив несколько лет, не изменяется при нагревании до 100 гр., окислительные свойства зависят от [Н+] и природы кислоты.
B. Неустойчив, разложение ускоряется на свету, при нагревании, под действием кислот и оснований, титр устанавливается не сразу.
C. Устойчив продолжительное время и инертен по отношению к хлороводородной кислоте.
D. Мало устойчив из-за летучести растворенного вещества и окисления кислородом воздуха, особенно на свету.
E. Устойчив неограниченно долго, вещество легко очищается перекристаллизацией.
8. Найдите для каждого из указанных ниже титрантов характеристику его устойчивости и др. свойства. Раствор церия (IV) сульфата в 1н. серной кислоте.
A. Устойчив несколько лет, неизменяется при нагревании до 100 гр., окислительные свойства зависят от [Н+] и природы кислоты.
B. Неустойчив, разложение ускоряется на свету, при нагревании, под действием кислот и оснований, титр устанавливается не сразу.
C. Устойчив продолжительное время и инертен по отношению к хлороводородной кислоте.
D. Мало устойчив из-за летучести растворенного вещества и окисления кислородом воздуха, особенно на свету.
E. Устойчив неограниченно долго, вещество легко очищается перекристаллизацией.
9. Найдите для каждого из указанных ниже титрантов характеристику его устойчивости и др. cвойства. Раствор калия перманганата
A. Устойчив несколько лет, неизменяется при нагревании до 100 гр., окислительные свойства зависят от [Н+] и природы кислоты.
B. Неустойчив, разложение ускоряется на свету, при нагревании, под действием кислот и оснований, титр устанавливается не сразу.
C. Устойчив продолжительное время и инертен по отношению к хлороводородной кислоте.
D. Мало устойчив из-за летучести растворенного вещества и окисления кислородом воздуха, особенно на свету.
E. Устойчив неограниченно долго, вещество легко очищается перекристаллизацией.
10. Найдите для каждого из указанных ниже титрантов характеристику его устойчивости и др. свойства. Раствор йода
A. Устойчив несколько лет, неизменяется при нагревании до 100 гр., окислительные свойства зависят от [Н+] и природы кислоты.
B. Неустойчив, разложение ускоряется на свету, при нагревании, под действием кислот и оснований, титр устанавливается не сразу
C. Устойчив продолжительное время и инертен по отношению к хлороводородной кислоте.
D. Мало устойчив из-за летучести растворенного вещества и окисления кислородом воздуха, особенно на свету.
E. Устойчив неограниченно долго, вещество легко очищается перекристаллизацией.
11. Найдите для каждого из указанных ниже титрантов характеристику его устойчивости и др. свойстав. Раствор калия бромата
A. Устойчив несколько лет, неизменяется при нагревании до 100 гр, окислительные свойства зависят от [Н+] и природы кислоты.
B. Неустойчив, разложение ускоряется на свету, при нагревании, под действием кислот и оснований, титр устанавливается не сразу.
C. Устойчив продолжительное время и инертен по отношению к хлороводородной кислоте.
D. Мало устойчив из-за летучести растворенного вещества и окисления кислородом воздуха, особенно на свету.
E. Устойчив неограниченно долго, вещество легко очищается перекристаллизацией.
12. Какими методами можно определить антипирин
A. Йодометрия
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое
13. Какими методами можно определить пероксид водорода
A. Иодометрия
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое
14. Какими методами можно определить калия арсенит
A. Йодометрия
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое
15. Какими методами можно определить магния сульфат
A. Йодометрия
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое
16. Какими методами можно определить новокаин
A. Йодометрия
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое
17. Выберите один или несколько правильных ответов для фиксирования конечной точки титрования в редокс-методах.
A. Редокс-индикаторы
B. Специфические индикаторы
C. Инструментальные методы
D. Безиндикатрное титрование окрашенными титрантами
E. Добавление органических растворителей.
18. Какая из приведенных ниже полуреакций восстановления калия перманганата наиболее широко используется в количественном анализе:
A) MnO4-+4H+3e-  MnO2 + 2H2O E0=+1,69 MnO2 + 2H2O E0=+1,69
|
B) MnO4-+8H+4e-  Mn2+ + 4H2O E0=+1,51 Mn2+ + 4H2O E0=+1,51
|
C) MnO4- +2Н2О+3е-  MnO2 + 4ОН- E0=+0,60 MnO2 + 4ОН- E0=+0,60
|
D) MnO4-+e  MnO42- + 2H2O E0=+0,58 MnO42- + 2H2O E0=+0,58
|
Е) MnO4- +3Н2О+3е-  MnО(OН)2 + 4ОН- E0=+0,60 MnО(OН)2 + 4ОН- E0=+0,60
|
19. Подберите соответствующие индикаторы для фиксирования точки эквивалентности в перманганатометрии.
A. Раствор крахмала
B. Безиндикаторный
C. Тропеолин 00
D. Метиловый оранжевый
E. Дифениламин
20. Подберите соответствующие индикаторы для фиксирования точки эквивалентности в йодометрии.
A. Раствор крахмала
B. Безиндикаторный
C. Тропеолин 00
D. Метиловый оранжевый
E. Дифениламин
21. Подберите соответствующие индикаторы для фиксирования точки эквивалентности в дихроматометрии.
A. Раствор крахмала
B. Безиндикаторный
C. Тропеолин 00
D. Метиловый оранжевый
E. Дифениламин
22. Подберите соответствующие индикаторы для фиксирования точки эквивалентности в броматометрии.
A. Раствор крахмала
B. Безиндикаторный
C. Тропеолин 00
D. Метиловый оранжевый
E. Дифениламин
23. Подберите соответствующие индикаторы для фиксирования точки эквивалентности в нитритометрии.
A. Раствор крахмала
B. Безиндикаторный
C. Тропеолин 00
D. Метиловый оранжевый
E. Дифениламин
24. Укажите продукты, которые образуются при взаимодействии натрия нитрита в кислой среде с такими веществами: Ar-NH2
A. Нитрозоамин
B. Нитрозоариленамин
C. Соль диазония
D. Нитрозоантипирин
E. Азид
25. Укажите продукты, которые образуются при взаимодействии натрия нитрита в кислой среде с такими веществами: R2-NH
A. Нитрозоамин
B. Нитрозоариленамин
C. Соль диазония
D. Нитрозоантипирин
E. Азид
26. Укажите продукты, которые образуются при взаимодействии натрия нитрита в кислой среде с такими веществами: Ar-N=(R)2
A. Нитрозоамин
B. Нитрозоариленамин
C. Соль диазония
D. Нитрозоантипирин
E. Азид
27. Укажите продукты, которые образуются при взаимодействии натрия нитрита в кислой среде с такими веществами:
R-CO-NH-NH2
A. Нитрозоамин
B. Нитрозоариленамин
C. Соль диазония
D. Нитрозоантипирин
E. Азид
28. Укажите, какие вещества образуются при взаимодействии нитрита натрия с таким веществом

A. Нитрозоамин
B. Нитрозоариленамин
C. Соль диазония
D. Нитрозоантипирин
E. Азид
29. Какими способами можно приготовить титрованные растворы тиосульфата натрия
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое
D. Ни то, ни другое
30. Какими способами можно приготовить титрованные растворы йода
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое
D. Ни то, ни другое
31. Какими способами можно приготовить титрованные растворы йода хлорида
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое
D. Ни то, ни другое
33. Какими способами можно приготовить титрованные растворы аммония трисульфатоцеррата (IV)
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое
D. Ни то, ни другое
34. Выберите один или несколько правильных ответов.
Cодержание пероксида водорода в растворе можно определять следующими методами:
A. Перманганатометрии
B. Броматометрии
C. Йодометрии
D. Цериметрии
E. Дихроматометрии
35. Выберите один или несколько правильных ответов.
В титриметрическом анализе можно использовать редоксреакции, которые:
A. Протекают стехиометрически, быстро и до конца
B. Имеют константу равновесия >=108
C. Позволяют фиксировать точку эквивалентности
D. Идут с образованием бесцветных продуктов
E. Сопровождаются видимыми изменениями
36. Реакциями окисления-восстановления называют реакции, идущие:
A. С изменением валентности элементов
B. С отдачей электронов
C. С повышением степени окисления восстановителя
D. С понижением степени окисления окислителя
E. С изменением степени окисления элементов
37. Подберите подходящий метод определения перекиси водорода, содержащей консерванты:
A. Дихроматометрия
B. Йодометрия
C. Перманганатометрия
D. Нитритометрия
E. Аскорбинометрия
38. Подберите подходящий метод определения Fe(II) в растворе, содержащем HCl:
A. Дихроматометрия
B. Йодометрия
C. Перманганатометрия
D. Нитритометрия
E. Аскорбинометрия
39. Подберите подходящий метод определения Ca2+
A. Дихроматометрия
B. Йодометрия
C. Перманганатометрия
D. Нитритометрия
E. Аскорбинометрия
40. Подберите подходящий метод определения C6H5-NH2
A. Дихроматометрия
B. Йодометрия
C. Перманганатометрия
D. Нитритометрия
E. Аскорбинометрия
41. Подберите подходящий метод определения Na2S2O3
A. Дихроматометрия
B. Йодометрия
C. Перманганатометрия
D. Нитритометрия
E. Аскорбинометрия
42. Какие титранты можно стандартизировать по мышьяковистому ангидриду:
A. Р-р калия перманганата
B. Р-р йода
C. И то, и другое
D. Ни то, ни другое
43. Какие титранты можно стандартизировать по первичному стандарту - железо металлическое:
A. Р-р калия перманганата
B. Р-р йода
C. И то, и другое
D. Ни то, ни другое
44. Какие титранты можно стандартизировать по первичному стандарту - соль мора:
A. Р-р калия перманганата
B. Р-р йода
C. И то, и другое
D. Ни то, ни другое
45. Какие титранты можно стандартизировать по первичному стандарту - гидразинсульфату:
A. Р-р калия перманганата
B. Р-р йода
C. И то, и другое
D. Ни то, ни другое
46. Какие титранты можно стандартизировать по первичному стандарту - калия дихромату:
A. Р-р калия перманганата
B. Р-р йода
C. И то, и другое
D. Ни то, ни другое
47. Выберите один или несколько правильных ответов.
Редоксиндикаторы должны отвечать следующим требованиям:
A. Быть ярко окрашенными
B. Менять окраску при окислении или восстановлении
C. Окисление или восстановление индикатора должно происходить быстро
D. Окраска индикатора должна изменяться при определённом значении потенциала
E. Процесс изменения окраски индикатора должен быть обратим
48. Выберите один или несколько правильных ответов.
Достоинствами цериметрии являются:
A. Сернокислые растворы церия (IV) чрезвычайно устойчивы
B. Восстановители можно определять в присутствии хлорид-ионов.
C. Редокспотенциал пары Ce4+/Ce3+ можно изменять в интервале1,28-1,60 в
D. Определение проводят только в сильнокислых растворах
E. Высокая стоимость соединений церия
49. На величину скачка титрования на кривой титрования в редоксметодах наиболее существенное влияние оказывает:
A. Редокс-потенциал окислителя
B. Редокс-потенциал восстановителя
C. Разность потенциалов окислителя и восстановителя
D. Изменение концентраций окислителя и восстановителя
E. Изменение концентрации ионов водорода
50. Укажите, в каких методах окислительно-восстановительного титрования используют для фиксирования конечной точки титрования добавление органического растворителя для извлечения избытка титранта
A. Перманганатометрия
B. Йодометрия
C. Цериметрия
D. Броматометрия
E. Нитритометрия
51. Укажите, в каких методах окислительно-восстановительного титрования, для фиксирования конечной точки титрования применяют внешние индикаторов
A. Нитритометрия
B. Перманганатометрия
C. Йодометрия
D. Цериметрия
E. Броматометрия
52. Укажите, в каких методах окислительно-восстановительного титрования используют для фиксирования конечной точки титрования специфический индикатор-крахмал
A. Нитритометрия
B. Перманганатометрия
C. Йодометрия
D. Цериметрия
E. Броматометрия
53. Укажите, в каких методах окислительно-восстановительного титрования используют для фиксирования конечной точки титрования безындикаторное титрование
A. Нитритометрия
B. Перманганатометрия
C. Йодометрия
D. Цериметрия
E. Броматометрия
54. Укажите, какие свойства проявляет йод (в роли какого реагента выступает) в следующей реакции: I2 + H2S ----> 2HI + S
A. Окислитель
B. Восстановитель
C. Электрофильный р-нт
D. Окислитель и восст-ль
E. Индифферентное вещество
55. Укажите, какие свойства проявляет йод (в роли какого реагента выступает) в следующей реакции: I2+5Cl2+H2O---->2HIO3+10HClO
A. Восстановитель
B. Электрофильный р-нт
C. Окислитель и восст-ль
D. Индифферентное вещество
E. Окислитель
56. Укажите, какие свойства проявляет йод (в роли какого реагента выступает) в следующей реакции: I2+NaOH---->NaOI+NaI+H2O
A. Окислитель
B. Восстановитель
C. Электрофильный р-нт
D. Окислитель и восст-ль
E. Индифферентное вещество
57. Укажите, какие свойства проявляет йод (в роли какого реагента выступает) в следующей реакции: I2 + I- ------>(I3)-
A. Окислитель
B. Восстановитель
C. Электрофильный реагент
D. Окислитель и восстановитель
E. Индифферентное вещество
58. Укажите, какие свойства проявляет йод (в роли какого реагента выступает) в следующей реакции:
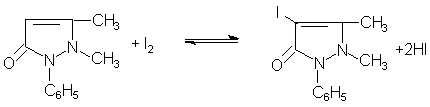
A. Окислитель
B. Восстановитель
C. Электрофильный реагент
D. Окислитель и восстановитель
E. Индифферентное вещество
59. Какими методами можно определять калия бромат
A. Йодометрия
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое
60. Какими методами можно определять 8-оксихинолин
A. Йодометрия
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое
61. Введите один или несколько правильных ответов
Mетод бромометрии применяют для определения:
A. Восстановителей
B. Минеральных кислот
C. Первичных ароматических аминов и фенолов
D. Третичных алифатических аминов
E. Окислителей
62. Введите один или несколько правильных ответов
При проведении йодометрических определений необходимо соблюдать условия:
A. Титрование проводят на холоду
B. Среда нейтральная или слабо щелочная
C. Избыток калия йодида при определении окислителей
D. При обратном и заместительном титровании определение проводят в склянках с притертыми пробками
E. Раствор крахмала добавляют в титруемую смесь отсутствии йода или незначительном количестве его
A.
63. При титровании Fe(II) раствором калия дихромата расчеты потенциала системы для построения кривой титрования в момент, когда добавлено
50% титранта, производят по формулам:
А. Е=Е0Fe3+/Fe2+ 
B. E= 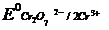 +
+ 
C. Е=Е0Fe3+/Fe2+
D. (6E0Cr2O72-/2Cr3++ E0Fe3+/Fe2+)/7
E. ЭДС= 
64. При титровании Fe(II) раствором калия дихромата расчеты потенциала системы для построения кривой титрования в момент, когда добавлено 90% титранта, производят по формулам:
А. Е=Е0Fe3+/Fe2+ 
B. E= 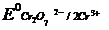 +
+ 
C. Е=Е0Fe3+/Fe2+
D. (6E0Cr2O72-/2Cr3++ E0Fe3+/Fe2+)/7
E. ЭДС= 
65. При титровании Fe(II) раствором калия дихромата расчеты потенциала системы для построения кривой титрования в момент начала скачка
титрования производят по формулам:
А. Е=Е0Fe3+/Fe2+ 
B. E= 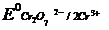 +
+ 
C. Е=Е0Fe3+/Fe2+
D. (6E0Cr2O72-/2Cr3++ E0Fe3+/Fe2+)/7
E. ЭДС= 
66. При титровании Fe(II) раствором калия дихромата расчеты потенциала системы для построения кривой титрования в момент точки эквивалентности производят по формулам:
А. Е=Е0Fe3+/Fe2+ 
B. E= 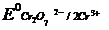 +
+ 
C. Е=Е0Fe3+/Fe2+
D (6E0Cr2O72-/2Cr3++ E0Fe3+/Fe2+)/7
E ЭДС= 
67. При титровании Fe(II) раствором калия дихромата расчеты потенциала системы для построения кривой титрования в момент конца скачка
титрования производят по формулам:
А. Е=Е0Fe3+/Fe2+ 
B. E= 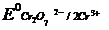

C. Е=Е0Fe3+/Fe2+
D. (6E0Cr2O72-/2Cr3++ E0Fe3+/Fe2+)/7
E ЭДС= 
68. Подберите подходящий метод определения активного хлора в белильной извести
A. Перманганатометрия через стадию образования труднорастворимых оксалатов
B. Иодометрия
C. Броматометрия через 8-оксихинолинаты
D. Дихроматометрия
E. Нитритометрия
69. Подберите подходящий метод определения солей Ca2+ и Ba2+
A. Перманганатометрия через стадию образования труднорастворимых оксалатов
B. Иодометрия
C. Броматометрия через 8-оксихинолинаты
D. Дихроматометрия
E. Нитритометрия
70. Подберите подходящий метод определения солей Mg2+, Al3+ и др
A. Перманганатометрия через стадию образования труднорастворимых оксалатов
B. Иодометрия
C. Броматометрия через 8-оксихинолинаты
D. Дихроматометрия
E. Нитритометрия
71. Подберите подходящий метод определения стрептоцида белого
A. Перманганатометрия через стадию образования труднорастворимых оксалатов
B. Йодометрия
C. Броматометрия через 8-оксихинолинаты
D. Дихроматометрия
E. Нитритометрия
72. По какому способу можно приготовить титрованные растворы калия перманганата
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое
D. Ни то, ни другое
73. По какому способу можно приготовить титрованные растворы калия дихромата
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое
D. Ни то, ни другое
74. По какому способу можно приготовить титрованные растворы калия бромата
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое
D. Ни то, ни другое
75. По какому способу можно приготовить титрованные растворы натрия тиосульфата
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое
D. Ни то, ни другое
76. Выберите один или несколько правильных ответов. Бромирование органических соединений происходит в соответствии с такими правилами:
A. Заместитель 1 рода направляет последующий заместитель в орто- и пара-положения.
B. Если орто-положение занято такими заместителями как карбокси-, сульфогруппа или карбонильная группа, они вытесняются бромом.
C. Наличие в орто-положении таких заместителей, как -CH3,-NO2,-Cl,-Br и др., препятствует вхождению брома в занятые ими положения.
D. Если в орто- и пара-положениях находятся NH2 или -OH -группы, такие производные окисляются до различных продуктов.
E. Если в мета- положении находятся -NH2 или -ОН группы, они не препятствуют бромированию в орто- и пара- положениях.
77. Выберите один или несколько правильных ответов
Недостатками цериметрии можно считать:
A. Зависимость редокс-потенциала системы пары Ce4+/Ce3+ от природы кислоты
B. Высокая стоимость соединений церия(IV)
C. Отсутствие взаимодействия с хлорид-ионами
D. Титрование только в сильно-кислых средах
E. Более сильные окислительные свойства, чем у перманганата калия
78. Какая окислительно-восстановительная пара содержит наиболее сильный восстановитель?
| A) Fe3+/Fe2+ E0=+0.77 |
| B) Sn4+/Sn2+ E0=+0.15 |
| C) I2/2I- E0=+0.54 |
| D) S4O62-/2S2O32- E0=+0.09 |
| E) VO2+/VO2+ E0=+0.99 |
79. Укажите каким редокс-методом можно определить количественное содержание меди сульфата?
A. Нитритометрия
B. Бромометрия
C. Перманганатометрия
D. Броматометрия
E. Йодометрия
80. Укажите каким редокс-методом можно определить количественное содержание активного хлора в хлорамине?
A. Нитритометрия
B. Бромометрия
C. Перманганатометрия
D. Броматометрия
E. Йодометрия
81. Укажите каким редокс-методом можно определить количественное содержание фенола?
A. Нитритометрия
B. Бромометрия
C. Перманганатометрия
D. Броматометрия
E. Йодометрия
82. Укажите каким редокс-методом можно определить количественное содержание сульфаниловой кислоты?
A. Нитритометрия
B. Бромометрия
C. Перманганатометрия
D. Броматометрия
E. Йодометрия
A.
83. Выберите один или несколько правильных ответов.
К редокс-индикаторам относятся:
A. Метиловый оранжевый
B. Ферроин
C. Крахмал
D. *Дифениламинсульфокислота
E. Калия перманганат
84. Выберите один или несколько правильных ответов
Преимуществами йодометрии являются:
A. Летучесть йода
B. Повышение титра раствора йода при хранении за счет окисления йодид-иона
C. Определение можно проводить только в нейтральной или слабо щелочной средах
D. Определение проводят на холоду
E. Высокая точность метода за счет чувствительного индикатора - Крахмала
85. В какой из редокс-пар окисленная форма является наиболее сильным окислителем?
| А) Сl2/Cl- E0=+1,36 |
| B) Cr2O72-/2Cr3+ E0=+1,33 |
| C) MnO4-/Mn2+ E0=+1,51 |
| D) MnO4-/MnО2 E0=+0,60 |
| Е) MnO4-/MnO42- E0=+0,56- |
86. Какими методами редокс-метрии определяют содержание сильных кислот в растворе
A. Перманганатометрия
B. Йодометрия
C. Нитритометрия
D. Аскорбинометрия
E. Титанометрия
87. Какими методами редокс-метрии определяют содержание воды в органических соединениях?
A. Перманганатометрия
B. Йодометрия
C. Нитритометрия
D. Аскорбинометрия
E. Титанометрия
88. Какими методами редокс-метрии определяют содержание новокаина
A. Перманганатометрии
B. Йодометрии
C. Нитритометрии
D. Аскорбинометрии
E. Титанометрии
89. Какими методами редокс-метрии определяют содержание формальдегида в формалине?
A. Перманганатометрия
B. *Йодометрия
C. Нитритометрия
D. Аскорбинометрия
E. Титанометрия
90. Какими методами редокс-метрии определяют содержание сульфаниловой кислоты?
A. Перманганатометрия
B. Йодометрия
C. Нитритометрия
D. Аскорбинометрия
E. Титанометрия
91. Подберите первичные стандарты для стандартизации раствора перманганата калия
A. Мышьяковистый ангидрид
B. Соль мора
C. И то, и другое
D. Ни то, ни другое
92. Подберите первичные стандарты для стандартизации раствора йода
A. Мышьяковистый ангидрид
B. Соль мора
C. И то, и другое
D. Ни то, ни другое
93. Подберите первичные стандарты для стандартизации раствора тиосульфата натрия
A. Мышьяковистый ангидрид
B. Соль мора
C. И то, и другое
D. Ни то, ни другое
94. Подберите первичные стандарты для стандартизации раствора церия сульфата
A. Мышьяковистый ангидрид
B. Соль мора
C. И то, и другое
D. Ни то, ни другое
95. Подберите первичные стандарты для стандартизации раствора нитрита натрия
A. Мышьяковистый ангидрид
B. Соль мора
C. И то, и другое
D. Ни то, ни другое
96. Подберите подходящий способ титрования при определении восстановителей методом йодометрии
A. Способ прямого титрования
B. Способ обратного титрования
C. И то, и другое
D. Ни то, ни другое
97. Подберите подходящий способ титрования для определения кальция перманганатометрически
A. Способ прямого титрования
B. Способ обратного титрования
C. И то, и другое
D. Ни то, ни другое
98. Подберите подходящий способ титрования для определения окислителей йодометрически
A. Способ прямого титрования
B. Способ обратного титрования
C. И то, и другое
D. Ни то, ни другое
99. Подберите подходящий способ титрования для определения окислителей перманганатометрически
A. Способ прямого титрования
B. Способ обратного титрования
C. И то, и другое
D. Ни то, ни другое
100. Выберите один или несколько правильных ответов.
Щавелевую кислоту или оксалаты применяют в качестве первичного стандарта для следующих титрантов:
A. Раствор бромата калия
B. Раствор перманганата калия
C. Раствор сульфата церия
D. Раствор йода
E. Раствор тиосульфата натрия
Осадительное и комплексометрическое титровани е
1. Осадительное титрование - это:
A. метод анализа, основанный на реакции образования труднорастворимых соединений
B. метод анализа, основанный на измерении объема титранта-осадителя, затраченного на количественное осаждение определяемого компонента
C. метод анализа, основанный на измерении объема титранта, затраченного на количественное взаимодействие с определяемым компонентом
D. метод анализа, основанный на точном измерении массы определяемого вещества в виде осадка
2. Кривая осадительного титрования - это:
A. графическая зависимость концентрации ионов водорода от объема титранта
B. графическая зависимость изменения растворимости при титровании
C. графическая зависимость изменения концентрации определяемого иона в процессе титрования от объема титранта
D. графическая зависимость величины редокс-потенциала от объема титранта
E. графическая зависимость изменения концентрации титранта от объема определяемого иона в процессе титрования
3. Выберите один или несколько правильных ответов
На величину скачка титрования в осадительном титровании влияют
A. растворимость осаждаемого соединения
B. концентрация титруемого растворов
C. концентрация стандартного растворов
D. температура
E. катализатор
4. Точка конца титрования в осадительном титровании фиксируется
A. визуально, с помощью рН-индикаторов
B. визуально, с помощью редокс-индикаторов
C. визуально, с помощью осадительных индикаторов
D. только инструментальными методами
E. всеми перечисленными способами
5. Вещества можно оттитровать методом осадительного титрования (продукт реакции бинарный труднорастворимый электролит), если:
А.растворимость осадка 10-4
В. ПР осадка 10-5
С. ПР осадка 10-7
Д. ПР осадка < 10-10
С. ПР осадка 10-8
6. Титрованный раствор нитрата серебра готовят по способу:
A. установленного титра
B. приготовленного титра
C. и то, и другое
D. ни то, ни другое
7. Титрованный раствор тиоцианата аммония готовят по способу:
A. установленного титра
B. приготовленного титра
C. и то, и другое
D. ни то, ни другое
8. В качестве первичных стандартов в аргентометрии используют:
A. натрия хлорид
B. калия хлорид
C. и то, и другое
D. ни то, ни другое
9. В методе аргентометрии для фиксирования точки конца титрования используют индикаторы
A. осадительные
B. адсорбционные
C. металлохромные
D. все названные
E. ни один из названных.
10. Определение по методу Мора проводят в области рН:
A. 1,5 - 10,5
B. 2 - 8
C. 0 - 14
D. 6,5 - 10,3
E. 6,5 - 7,5
11. В качестве индикатора при определении по Мору применяют:
A. железо-аммонийные квасцы
B. хромат калия
C. дифенилкарбазон
D. эозин
E. натрия нитропруссид
12. Методом Мора количественно определяют:
A. Cl-, Вr-, I-, SCN-
B. Br-, I-
C. Cl-, Br-
Д. Cl-, Br-, I-
13. Галогениды определяют по методу Фольгарда способом:
|
| Поделиться: |
Поиск по сайту
Все права принадлежать их авторам. Данный сайт не претендует на авторства, а предоставляет бесплатное использование.
Дата создания страницы: 2017-12-12 Нарушение авторских прав и Нарушение персональных данных