Дубильные вещества (танины, таниды)- растительные высокомолекулярные фенольные соединения (мол. масса от 1000 до 20000), обладающие вяжущим вкусом, способные связывать белки кожи («Дубить» невыделанную шкуру, кожу), осаждать алкалоиды. Дубильные вещества с мол. массой от 300 до 1000 не способны к дублению, но они обладают вяжущими свойствами, поэтому их часто называют «пищевыми танинами» или «чайным танином». Способность дубильных веществ «дубить» невыделанную шкуру, превращая ее в кожу, основана на их взаимодействия с белком кожи- коллагеном, - приводящим к образованию структур, устойчивых к процессам гниения. Термин «дубильные вещества» был впервые использован в 1790 году французским исследователем Сегеном для обозначения присутствующих в экстрактах некоторых растений веществ, способных осуществлять процесс дубления.
Классификация ДВ
1. Классификация Г.Проктера (1894 г).: ДВ в зависимости от природы продуктов их разложения при 180-200°С (без доступа воздуха) разделяют на 2 группы:
| 1) пирогалловые (гидролизуемые ДВ). | 
|
| пирогаллол | |
| 2) пирокатехиновые (конденсированные ДВ). | 
|
| пирокатехин |
2. Классификация Фрейденберга:
1) гидролизуемые ДВ (расщепляются в условиях кислотного или ферментного гидролиза на простейшие составные части, в том числе галловую кислоту):
а) галлотанины- эфиры галловой кислоты и сахаров.
б) несахаридные эфиры фенолкарбоновых кислот
в) эллаготанины- эфиры эллаговой кислоты и сахаров.
2) конденсированные ДВ (не распадаются под действием кислот, образуя при этом продукты конденсации- флобафены):
а) производные флаванов
б) производные флавандиолов
в) производные оксистильбенов
Гидролизуемые дубильные вещества.
К гидролизуемой группе ДВ относят соединения, которые при обработке разбавленными кислотами (в условиях кислотного гидролиза) распадаются с образованием более простых соединений фенольной (чаще всего галловой кислоты) и нефенольной природы (как правило глюкозы или другого моносахарида).
В зависимости от строения образующихся при полном гидролизе первичных фенольных соединений различают:
Галлотанины (галловые дубильные вещества) - сложные эфиры галловой или дигалловой кислоты с глюкозой, причем к молекуле глюкозы может присоединиться разное количество (до 5) молекул галловой (или м-дигалловой) кислоты.
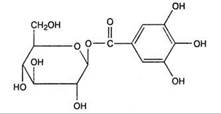
| β-D-глюкогаллин (моногаллоильный эфир). Источник: галлы(наросты на L сумаха полукрылатого (китайский танин), ветках дуба лузитанского (турецкий танин), L сумаха дубильного и скумпии копсестра. |
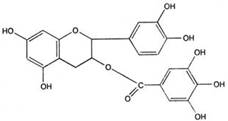
Несахарные эфиры галловой кислоты - эфиры галловой кислоты, например, 3-О-галлоилхинная кислота (теогаллин).

| 
|
| Теогаллин (зеленный чай). | Катехингаллат |

| таратанин |
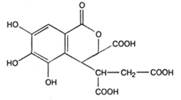
Эллаговые ДВ, или эллаготанины, при гидролизе отщепляют в качестве фенольных остатков эллаговую кислоту, которая образуется в растениях из гексагидроксидифеновой кислоты- продукта окисления галловой кислоты. в качестве сахаристого остатка в эллаговых ДВ также чаще всего встречается глюкоза.

| 
|
| Кислота гексагидроксидифеновая | Кислота хебуловая |

| 
|
| Эллаговая кислота | Корилагин |
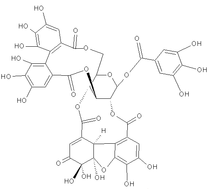
| Хебулаговая кислота |
Сырье: тропические растения- плоды, терминалия хебула, цезальпинии дубильной, корка гранатника.
Конденсированные ДВ.
Конденсированные ДВ в основном представлены полимерами катехина (флаван-3-ол) или лейкоантроцианидина (флаван-3,4-диол) или сополимерами этих двух типов флаваноидных соединений.
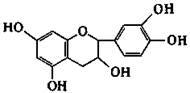
| 
|
| Катехин | Лейкоантоцианидин |

| 
|
| Резвератол (3,5,4´- тригидроксистильбен) | Хлорогеновая кислота |

| Иногда к ДВ относят моно- и дикофеилхинные кислоты (например, хлорогеная кислота). К этой же группе относят розмариновую кислоту. Сырье: зверобой, черника, чай китайский. |
| Розмариновая кислота |
ДВ широко распространены в природе. Наиболее распространены ДВ в представителях двудольных растений, где они накапливаются в максимальных количествах (Rosaceae, Tamaricaceae, Polygonaceae, Salicaceae, Myrtaceae, Fabaceae, Plumbaginaceae, Geraniaceae, Asteraceae).
У однодольных ДВ встречаются лишь в некоторых семействах. Многие хвойные накапливают большое количество ДВ. Эти вещества встречаются в папоротниках, хвощах, плаунах и мхах. Наиболее высокое содержание (до 50-70 %) ДВ отмечено в патологических образованиях- в турецких и китайских галлах.
ДВ накапливаются в разных частях растений. Чаще всего они содержатся в коре ствола, затем в коре корней и корневищах, в стеблях и листьях (у травянистых растений), а также в оболочке плодов.
Содержание ДВ изменяется в зависимости от периода вегетации растения (min- весной, в период отрастания растения.max- в фазе бутонизации- начале цветения. К концу вегетации количество ДВ в корнях постепенно убывает. Фаза вегетации влияет не только на количество, но и на качественный состав ДВ).
ДВ преимущественно локализованы в вакуоли растительной клетки отделены от цитоплазмы белково-липидной мембраной- тонопластом, который регулирует участие вакуолярных веществ в метаболизме клетки. Поскольку ДВ находятся в растворенном состоянии, их обнаруживают с помощью гистохимических реакций. С помощью таких реакций можно установить, что большинство ДВ листьев находятся в обкладочных клетках, окружающих жилки. В стеблях, стволах и корневищах ДВ локализуются в паренхимных клетках сердцевинных лучей, коры, вкраплены в древесину и флоэму (в клетки паренхимы); в механической ткани ДВ отсутствуют. В случае повреждения живой клетки изменяется внутриклеточное давление, и наступает разрыв тонопласта. ДВ вытесняются в ципотлазму, где, подвергаясь ферментативному окислению, превращаются в коричневые и красные аморфные вещества, называемые флабофенами. В отличие от исходных танинов флабофены нерастворимы в холодной воле, но растворяются в горячей, окрашивая настои и отвары в красно-бурый цвет.
ДВ в растительном организме выполняют определенные физиологические функции:
1. одна из форм запасных веществ;
2. принимают участие в построение древесины;
3. препятствую гниению древесины;
4. защитные вещества против вредителей и возбудителей заболеваний.
Физико-химические свойства ДВ.
Средняя мол. масса порядка 1000-5000 (до 20000), представляют собой, как правило, аморфные соединения, образующие при растворении в воде коллоидные растворы.
Таниды растворимы в органических растворителях: ацетоне, этиловом спирте, смеси этилового спирта и этилового эфира, в этиловом эфире; частично: тилацетате, пиридине; нерастворимы в хлороформе, петролейном эфире, бензоле и сероуглероде.
Оптически активные соединения, обладают вяжущим вкусом, легко окисляются на воздухе, приобретая коричневую или темную окраску.
Катехины - кристаллические вещества, хорошо растворимые в воде и органических растворителях (спирт, ацетон и др.). легко окисляются при нагревании, на свету, особенно в щелочной среде и при действии окисляющих ферментов (пероксидазы).
Лейкоантоцианидины - аморфные вещества, окисляются легче чем катехины; растворимы в воде, этаноле, ацетоне, хуже в этилацетате, нерастворимы в этиловом эфире. Max поглощение в УФ-спектре270-280 нм. При нагревании с разбавленными кислотами дают ярко окрашенные антоцианы.
Методы выделения и идентификации.
При выделении из РС получают фракции ДВ. Для этого используют экстракцию растительного материала органическими растворителями: обрабатывают сырье петролейным эфиром, бензолом или смесью бензол:хлороформ (1:1) для удаления основной массы хлорофилла, терпеноидов и липидов, затем экстрагируют этиловым эфиром, который извлекает некоторые фенольные соединения, в том числе оксикоричные кислоты и катехин; после этого проводят экстракцию этилацетатом, в результате которой в экстракт переходят цианидины, эфиры оксикоричной кислоты и др. в завершении растительный материал экстрагируют метиловым или этиловым спиртом, при этом в раствор переходят ДВ и др. фенольные соединения.
Для получения суммы ДВ используют РС, которое вначале экстрагируют горячей водой, а затем охлажденный водный экстракт обрабатывают последовательно вышеперечисленными растворителями.
Широко распространено выделение ДВ осаждением из водных или спиртово-водных растворов солями свинца. Полученные осадки затем обрабатывают разбавленной серной кислотой.
В промышленных условиях ДВ извлекают из сырья горячей водой в батарее диффузоров (перколяторов) по принципу противотока.
Суммарные извлечения ДВ разделяют на индивидуальные компоненты с помощью хроматографических методов (катехинов, лейкоантоцианидинов):
1. адсорбционная хроматография на колонках целлюлозы, полиамида
2. ионнообменная
3. распределительная хроматография на колонках силикогеля
4. противоточное распределение
5. гельфильтрация на колонках Сефадекса Г-50, Г-100 и др.
Идентификация индивидуальных компонентов ДВ основана на:
1. хроматографический механизм (хроматографируя на бумаге и тонкослойная)
2. спектральных исследованиях
3. качественных реакциях
| Реакции осаждения. Образование осадка с | Аналитический сигнал |
| 1. растворами желатина | образуется муть, исчезающая при добавлении избытка реактива |
| 2. растворами алкалоидов | |
| 3. растворами солей тяжелых металлов |
Для доказательства наличия в растениях гидролизуемых или конденсируемых ДВ используются цветные реакции, позволяющие различать эти группы:
| гидролизуемые | конденсированные |
| 1. Реакция с раствором железоаммониевых квасцов (или хлорида окисного железа). | |
| черно-синее окрашивание или осадок | черно-зеленое окрашивание |
| 2. Реакция с диазореактивом (диазобензолсульфокислота, диазотированная сульфаниловая кислота). Развивается различная окраска. | |
| 3. Реакция с формальдегидом в присутствии хлороводородной кислоты. | |
| Фильтрат+ железоаммониевые квасцы + ацетат свинца- синее или фиолетовое окрашивание. | Образуется осадок. |
| 4. с нитрозометилуретпном. | |
| Фильтрат+ железоаммониевые квасцы + ацетат свинца- фиолетовое окрашивание. | Образуется осадок. |
| 5. бромная вода | |
| Образуется осадок. | |
| 6. Уксусная кислота+ ацетат свинца | |
| Образуется осадок. | Фильтрат+ железоаммониевые квасцы- раствор окрашивается в черно-зеленый цвет |
| 7. NaNO2 + HCl | |
| Коричневое окрашивание | |
| 8. Ванилин + HCl(конц) | |
| Красное окрашивание (катехины) |
4. изучение продуктов расщепления
5. УФ-, ИК- и ПСР- спектроскопии.
Для изучения структуры ДВ используется гидролиз (ферментативный- танназы), щелочное распределение с последующим анализом полученных продуктов- фенольных фрагментов и других компонентов молекулы.
Хроматограммы ДВ просматривают в УФ-свете и отмечают характер флуоресценции зон адсорбции. Некоторые производные катехинов имеют слабую голубую флуоресценцию, усиливающуюся после обработки хроматограмм парами аммиака.
Для обнаружения катехинов, лейкоантоцианидов и их производных на хроматограммах используют 1% ванилин в HCl(конц). Лейкоантоцианидины можно отличить от катехтнов при выдерживании хроматограммы в парах HCl с последующим нагреванием при 105°С в течение 2 мин. при этом лейкоантоцианидины переходят в антоцианидины (розовый, красно-фиолетовый цвет), а катехины остаются бесцветными или желтеют.
Методы количественного определения ДВ в РС.
1. весовой метод (ВЕМ) (официальный в дубильно-экстрактовой промышленности): в водных вытяжках из растительного материала вначале определяют общее количество растворимых веществ (сухой остаток) путем высушивания определенного объема вытяжки до постоянной массы. Затем из вытяжки удаляют ДВ, обрабатывая ее обезжиренным кожным порошком (Гольев порошок), после отделения осадка в фильтрате вновь устанавливают количество сухого остатка. Разность в массе сухого остатка до и после обработки вытяжки кожным порошком показывает количество подлинных танидов.
2. титриметрический метод Левенталя-Курсанова (фармакопейный (ГФ СССР XI издание)): определяют путем окисления их перманганатом калия в сильноразбавленных растворах в присутствии индигосульфокислоты.
3. спектрофотометрическое: на реакциях с солями Fe(III), фосфорновольфрамовой кислотой.
4. нефелометрические, хроматоспектрофотометрические методы: в научных исследованиях.
Медико-биологическое значение ЛРС.
Препараты ДВ применяются в качестве вяжущих и противовоспалительных средствах. Вяжущее действие ДВ основано на их способности связываться с белками сс образованием плотных альбуминатов. При нанесении на слизистые оболочки или раневую поверхность ДВ вызывают частичное свертывание белков слизи или раневого экссудата и приводят к образованию пленки, защищающей от раздражения чувствительные нервные окончания тканей. Уменьшение при этом болевых ощущений, местное сужение сосудов, ограничение секреций, а также непосредственное уплотнение клеточных мембран приводят к уменьшению воспалительной реакции. ДВ благодаря способности образовывать осадки с алкалоидами, гликазидами и солями тяжелых металлов в качестве противоядий при пероральном отравлении этими веществами.
| ЛРС | Лекарственное сырье | Применение |
| Сумах китайский (сумах полукрылатый) | собранные осенью и высушенные галлы китайские («чернильные орешки») | для производства танина и препаратов на его основе |
| Дуб лузитанский (дуб зараженный) | свежесобранные галлы- зеленные, мягкие, сочные, шаровидно-шишковатой формы. | для производства танина и препаратов на его основе |
| Горец змеиный (Polygonum bistorta L.) | Собранные после отцветания, очищенные от корней, остатков листьев и стеблей, отмытые от земли и высушенные корневища | Отвар и др. препараты применяются при острых хронических поносах и др. воспалительных процессах в кишечнике, а также наружно при воспалительных процессах слизистой оболочки полости рта. Сырье входит в состав вяжущих желудочных сборов. |
| Кровохлебка лекарственная (красноголовник) (Sanguisorba officinalis L.) | Собранные осенью, очищенные от остатков надземных частей, отмытые от земли и высушенные корневища и корни | В виде отвара как вяжущее, антисептическое и кровоостанавливающее средство при желудочно-кишечных заболеваниях, маточных, геморроидальных кровотечениях, фибромиоме матки, воспалительных процессах полости рта; при энтероколитах, интоксикационных и гастрогенных поносах; губительно действует на трихомонады, грибки рода Candida и лямблии. |
| Бадан толстолистный (Bergenia crassifolia) | Собранные в июне-июле, освобожденные от земли, корней и надземных частей, разрезанные на куски и высушенные корневища | Отвар применяют при лечении заболеваний желудочно-кишечного тракта, хронических воспалительных процессов полости рта; кровоостанавливающее. Листья: при лечении заболеваний органов системы пищеварения, нормализации обмена веществ. |
| Ольха клейкая (ольха черная) (Alnus glutinosa (L.) Gaerth) | Собранные поздней осенью и зимой, высушенные соплодия ольхи серой. | Вяжущее средство при хронических колитах и энтероколитах, диспепсии. «Альтан» |
| Скумпия коггигрия (скумпия кожевенная) (Cotinus coggygria Scop) | Собранные летом (июнь-август) и высушенные листья | Для производства танина, галловой кислоты, обладающих вяжущими, бактерицидными свойствами; «Флакумин». |
| Сумах дубильный (Rhus coriaria L.) | Собранные летом (июнь-август) и высушенные листья | Для получения медицинского и технического танина. Препараты "Танальбин", "Тансал". |
| Дуб черешчатый (дуб обыкновенный) (Quercus robur L. (syn. Quercus pedunculata Ehrh.)) | Собранная ранней весной кора поросли, тонких стволов и молодых ветвей. | Вяжущее и противовоспалительного средства. Кора, отвар, порошок, сборы. "Витадент". |
| Лапчатка прямостоящая (Potentilla erecta (L.), Hatpe (syn. Potentilla tormentilla Schrank)) | Собранные в фазу цветения и высушенные корневища | Отвар и настойки как вяжущее и противовоспалительное средство. Сырье входит в состав вяжущих сборов. |
| Лапчатка серебристая | Собранная в период цветения и высушенная трава | Противовоспалительное, вяжущее, противоожоговое средство. Сырье входит в состав сбора М.Н. Здренко. «Холафлукс» содержит экстракт травы лапчатки гусиной |
| Черника обыкновенная (Vaccinium myrtillus L.) | Зрелые и высушенные плоды, а также собранные до окончания плодоношения и высушенные верхушки побегов | Вяжущее (плоды) и гипогликемическое (побеги) средство, обладающее противовоспалительными свойствами. Плоды в пачках, отвар, сбор "Арфазетин" и «Мирфазин» (побеги черники). |
| Черемуха обыкновенная (Padus avium Mill. (Padus racemosa G.)) | Собранные в период полного созревания и высушивания плоды дикорастущих и культивируемых кустарников или деревьев. | Вяжущие и противовоспалительные средства. Плоды, отвар, сборы. |