Ковалентная химическая связь»
Дата проведения: 11.11.2021.
Цель: углубить и расширить знания о причинах возникновения ковалентной химической связи.
Развивающая цель: развивать представления о ковалентной полярной и неполярной химической связи.
Воспитательная цель: продолжить формирование интереса к предмету и химического видения мира, воспитывать самостоятельность, умение сотрудничать с учителем и другими учащимися
Тип урока: урок формирования новых знаний.
Ход урока:
1. Организационный момент
2. Актуализация знаний (проверь себя)
1. Назовите максимальное количество электронов на внешнем энергетическом электронном уровне у неметаллов.
2. Какие типы химической связи вы еще помните?
3.Что такое ион?
4. Какую связь называют ионной?
5. Записать схему образования ионной связи оксида натрия
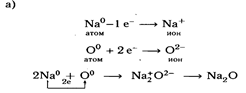
Запись в тетрадях
3. Изучение нового материала
Сегодня мы продолжаем изучение типов химической связи.
Как мы назовем взаимодействие атомов элементов-неметаллов между собой?
Запишите в тетрадях тему урока «Ковалентная химическая связь»
Мы уже рассмотрели, как взаимодействуют атомы элементов-металлов с атомами элементов-неметаллов: одни отдают свои внешние электроны и превращаются при этом в положительные ионы, другие принимают электроны и превращаются при этом в отрицательные ионы. Ионы притягиваются друг к другу, образуя ионные соединения.
А как осуществляется связь между атомами элементов-неметаллов, которые имеют сходную тенденцию к присоединению электронов мы рассмотрим Предлагаю посмотреть видео:. https://yandex.fr/video/preview/?filmId=15914889286561977291&from=tabbar&parent-reqid=1636477562244176-546554147061285467-man1-2717-240-man-l7-balancer-8080-BAL
4. Закрепление: Выполнение теста.
В аммиаке и хлориде бария химическая связь соответственно
1) ионная и ковалентная полярная
2) ковалентная полярная и ионная
3) ковалентная неполярная и металлическая
4) ковалентная неполярная и ионная
В каком ряду все вещества имеют ковалентную полярную связь?
1) HCl NaCl Cl2
2) O2 H2O CO2
3) H2O NH3 CH4
4) NaBr HBr CO
3.Соединениями с ковалентной полярной и ковалентной неполярной связью являются соответственно:
1)вода и сероводород
2)бромид калия и азот
3)аммиак и водород
4)кислород и метан
Ковалентная неполярная связь характерна для
1) С12 2) SO3 3) СО 4) SiO2
Веществом с ковалентной полярной связью является
1) С12 2) NaBr 3) H2S 4) MgCl2
Вещество с ковалентной неполярной связью имеет формулу
1) NH3 2) Сu 3) H2S 4) I2
7.Веществами с неполярной ковалентной связью являются
1) вода и алмаз
2) водород и хлор
3) медь и азот
4) бром и метан
Тремя общими электронными парами образована ковалентная связь в молекуле
1) азота
2) сероводорода
3) метана
4) хлора
Между атомами с одинаковой относительной электроотрицательностью образуется химическая связь
1) ионная
2) ковалентная полярная
3) ковалентная неполярная
4) водородная
Подумайте какие и где вещества с ковалентной неполярной связью мы с вами применяем (используем) в жизни, в быту?
1. кислород – мы им дышим;
2. азот – используется в морозильных камерах и как удобрение;
3. йод – незаменим в домашней аптечке. Наш регион беден эти природным элементом, поэтому его добавляют в продукты (соль, сметана, хлеб). Им богаты морепродукты;
4. хлор – хлорируем воду, обеззараживая ее;
5. фтор – в зубной пасте, в качестве отбеливающего средства.
Запишем домашнее задание: пересказ параграфа 4, стр. 29 – 33; По желанию подготовить сообщение или презентацию о типах кристаллических решеток.
Выучить определения:
Химическая связь – это такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы.
Ковалентная химическая связь – это связь, возникающая между атомами за счёт общих электронных пар.
Электроотрицательность – это способность атомов химических элементов оттягивать на себя общие электронные пары, находящиеся в совместном владении
Неполярная – ковалентная химическая связь, образующаяся между атомами с одинаковой электроотрицательностью.
Полярная – ковалентная химическая связь, образующаяся между атомами с разной электроотрицательностью.
Молекула углекислого газа неполярная, так как имеет линейное строение
Кристаллическая решётка веществ с ковалентной химической связью: атомная и молекулярная. Атомная – очень прочная (графит, алмаз), молекулярная – газы, легколетучие жидкости, твёрдые легкоплавкие вещества (хлор, вода, йод, углекислый газ – «сухой лёд»). Молекулярная кристаллическая решётка непрочная, так как внутримолекулярные связи прочные, межмолекулярное взаимодействие слабое.