Тема: «Физика атомного ядра»
Нуклонная модель ядра Гейзенберга-Иваненко. Заряд ядра. Массовое число ядра. Изотопы.
В 1911 году Резерфорд произвел опыт по «рассеиванию альфа и бета частиц».
Резерфорд сделал вывод, что масса атома сосредоточена в центре атома в небольшом объеме и имеет положительный заряд.
Таким образом, Резерфорд открыл атомное ядро, с этого момента и ведёт начало ядерная физика, изучающая строение и свойства атомных ядер. В ядре атома сосредоточена почти вся масса атома. Диаметр ядра не превышает 10-14–10-15 м.
После обнаружения стабильных изотопов элементов, ядру самого лёгкого атома была отведена роль структурной частицы всех ядер. С 1920 года ядро атома водорода имеет официальный термин — протон, в 1932 году Джеймсом Чедвиком была открыта новая электрически нейтральная частица, названная нейтроном. В том же году Иваненко и, независимо, Гейзенберг выдвинули гипотезу о протон-нейтронной структуре ядра. В дальнейшем, с развитием ядерной физики и её приложений, эта гипотеза была полностью подтверждена.
По этой теории все ядра состоят из двух видов частиц — протонов и нейтронов.
Протоны и нейтроны называются нуклонами.
Общее число нуклонов в ядре называется массовым числом и обозначается буквой А.
Массовое число А численно равно массе ядра, выраженной в атомных единицах массы и округленной до целых чисел.
Атомная единица массы (1 а. е. м.) равна 1/12 части массы атома углерода, внесистемная единица массы, применяемая для масс молекул, атомов, атомных ядер и элементарных частиц.
Число протонов соответствует порядковому (атомному) номеру элемента.
Разница между массовым и зарядовым числом равна числу нейтронов.
Любой химический элемент периодической таблицы Д.И. Менделеева можно представить формулой: 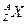
A – массовое число, Z – зарядовое число. Массовое число равно сумме протонов и нейтронов. Зарядовое число – это атомный номер, который равен числу протонов в ядре.
В ядрах одного и того же химического элемента число нейтронов может быть различным, а число протонов всегда одно и то же. Такие ядра называются изотопами.
Энергия связи нуклонов в ядре. Ядерные силы
Силы, которые скрепляют отдельные протоны и нейтроны в ядре называются ядерными, а соответствующее взаимодействие сильным. Оно на много порядков величин превышает гравитационное притяжение между протонами и нейтронами в ядре и доминирует над электромагнитными силами кулоновского отталкивания одноименно заряженных протонов внутри ядра.
Важнейшей особенностью ядерных сил является короткий радиус их действия. Они действуют только внутри атомного ядра. Законы ядерных взаимодействий — это законы квантовой физики, и они носят совершенно другой характер, чем уже известные нам гравитационные взаимодействия.
Отметим два свойства ядерных сил:
1) На расстоянии между нуклонами внутри ядра порядка 1 фм и больше силы носят характер притяжения,
характер притяжения, но при сближении протонов или нейтронов на расстоянии меньше 1 фм возникают силы отталкивания. Это препятствует сжатию ядер до еще меньших размеров.
2) Экспериментально доказано, что ядерные силы между двумя протонами, двумя нейтронами и протоном и нейтроном практически одинаковы. Это свойство называют зарядовой независимостью ядерных сил.
Минимальная энергия, необходимая для расщепления ядра на отдельные нуклоны, называется энергией связи ядра.
Энергию связи любого ядра можно определить с помощью формулы Эйнштейна, которая устанавливает взаимосвязь между массой и энергией:
Есв.= Δmс2=(Zmp+Nmn-Mя)с2
где Δm — дефект массы, с — скорость света в вакууме.
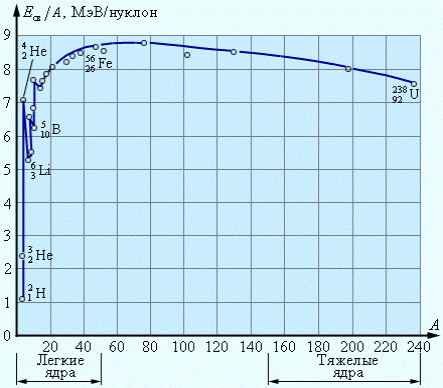
Устойчивость ядер характеризует физическая величина, называемая удельной энергией связи. Она равна энергии связи, которая приходится только на одну ядерную частицу (протон или нейтрон):
Еуд.=Есв/А
По графику зависимости удельной энергии связи от массового числа элементов можно заметить, что для легких ядер энергия связи очень мала. Удельная энергия связи имеет наибольшее значение для ядер атомов, расположенных в средней части периодической системы элементов с массовыми числами от 28 до 138. С дальнейшим ростом массового числа энергия связи убывает.