Задача 11-1. 
1. Рассчитаем количественное соотношение атомов углерода, водорода и азота в пиридине: оно равно n(C): n(H): n(N) = (75,9/12): (6,3/1): (17,8/14) = 6,325: 6,3: 1,27 = 4,98: 4,96: 1 ≈ 5: 5: 1, то есть количественная формула пиридина – C5H5N. 1 балл
2. Используя условие ароматичности, можно установить структурную формулу пиридина:  . Действительно, данная формула удовлетворяет всем требованиям: эта молекула плоская, т.к. в ней содержатся 3 кратные связи, вращение вокруг которых невозможно 2 балла в этой молекуле всего один цикл 1 балл все связи сопряжены (кратные связи чередуются с одинарными) 1 балл система содержит 6π-электронов (по 2 от каждой кратной связи; n=1) 2 балла
. Действительно, данная формула удовлетворяет всем требованиям: эта молекула плоская, т.к. в ней содержатся 3 кратные связи, вращение вокруг которых невозможно 2 балла в этой молекуле всего один цикл 1 балл все связи сопряжены (кратные связи чередуются с одинарными) 1 балл система содержит 6π-электронов (по 2 от каждой кратной связи; n=1) 2 балла
3. Исходя из похожих рассуждений, установим, что циклопентадиен и циклооктатетраен неароматичны (т.к. число π-электронов не равно 4n+2), а тиофен отвечает всем требованиям ароматичности. 3*1 балл =3 балла
Всего 10 баллов
Задача 11-2.
1. Формула винной килоты – НООС-СН(ОН)-СН(ОН)-СООН, следовательно, формула её кислой соли имеет вид ХООС-СН(ОН)-СН(ОН)-СООН.
1 балл
2. По условию, массовая доля углерода в этом соединении равна ω(С) = 25,53%, т.е. ω(С) = 48/16*6+12*4+1*5+Ar(Х) =0,2553 Отсюда, Х – калий.
0,5 баллов
Формула винного камня – КООС-СН(ОН)-СН(ОН)-СООН, его нынешнее название – гидротартрат калия.
1 балл
3. Поташ К2СО3. 0,5 баллов
4.Калий – серебристый, лёгкий, мягкий металл с низкой температурой плавления. При горении калия на воздухе образуется надпероксид калия: К + О2 → КО2. Соединения калия окрашивают пламя спиртовки в фиолетовый цвет. 1 балл
5. Реакция 1
КООС-СН(ОН)-СН(ОН)-СООН + NaOH → КООС-СН(ОН)-СН(ОН)-СООNa + Н2О
1 балл
Реакция 2 –
Cu2+ + 2OH- + 2C4O6H42- → 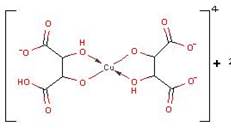
2 балла
Реакция 3 –

2 балла
6. Хелатные.
1 балл
Всего 10 баллов
Задача 11-3.
1. «Семёрка металлов древности» – это Pb, Fe, Au, Ag, Hg, Cu, Sn. Сульфаты не всех металлов растворимы в воде, т.е. не подвергаются электролизу в растворе. 2 балла
С помощью уравнения Фарадея определим возможное значения молярных массы солей:
m = (M*I*t)/(n*F), откуда M = (m*n*F)/(I*t) = (0,0893*96500*n)/(15*3600*2) = 0,0798n
1 балл
При n=1 М=79,8г/моль При n=2 М=159,6г/моль, что соответствует сульфату меди CuSO4. При n=3 M=239,4г/моль, ни один из указанных сульфатов не подходит. Таким образом, металл Х– медь. 2 балла
2. Малахит (СuOH)2CO3, халькопирит или медный колчедан СuFeS2, халькозин или медный блеск Cu2S.
2*0,5= 1 балл
Реакция 1: Сu + 2H2SO4 (конц.) → CuSO4 + SO2 + H2O. Образуются сульфат меди(II) (А), оксид серы(IV) и вода. 0,5 балла
Реакция 2: СuSO4 + 2NaOH → Cu(OH)2 ↓ + Na2SO4. Получается гидроксид меди(II) (Б) сине-голубого цвета и сульфат натрия. 0,5 балла
Реакция 3: СН2О + Сu(OH)2 → HCOOH + 2CuOH +H2O (при нагревании). Продукты: HCOOH – муравьиная кислота (В); CuOH - гидроксид меди(I) (Г) жёлтого цвета, 1 балл который далее распадается на оксид меди (I) красного цвета и воду: 2CuOH → Cu2O + H2O. Этим и объясняется постепенное изменение окраски раствора.
2 балла
Всего 10 баллов
Задача 11-4. 
1. Реакции:
С2Н6 + Сl2 → C2H5Cl (на свету) + HCl 0,5 балла
C2H5Cl + NaCN → C2H5CN + NaCl 0,5 балла
C2H5CN + 2H2O → C2H5COOH + NH3 (в присутствии серной кислоты) 0,5 балла
C2H5Cl + Mg → C2H5MgCl 0,5 балла
C2H5MgCl + CO2(сухой лёд) → C2H5COOMgCl 0,5 балла
C2H5COOMgCl + H2O → C2H5COOH + Mg(OH)Cl 0,5 балла
C2H5COOH + 2Cl2 → CH3CCl2COOH + 2HCl (катализатор – PCl5) 1 балл
CH3CCl2COOH → CH3CHCl2 + CO2 (при нагревании) 1 балл
CH3CHCl2 + 2H2 → C2H6 +2HCl (на никелевом катализаторе) 1 балл
Таким образом, А – C2H5Cl; Б – C2H5CN; В – C2H5COOH; Г – C2H5MgCl; Д – C2H5COOMgCl; Е – CH3CCl2COOH; Ж – CH3CHCl2.
2. Подтверждение дополнительными данными:
Соединение Г действительно содержит 24/(2*12+5*1+24+35,5) = 0,271, т.е. 27,1% Mg по массе; 1 балл в реакции 3НСООН + 2КMnO4 → 2 MnO2 + 3СО2 + 2KOH + 2H2O (при нагревании) выделяется углекислый газ СО2, следовательно, сухой лёд имеет состав СО2. 2 балла
3. Французский химик Виктор Гриньяр. 1 балл
Всего 10 баллов