Алкенами, этиленовыми углеводородами или олефинами (маслообразующими) называют углеводороды, в состав молекул которых входят как минимум два углеродных атома, соединенные друг с другом двумя связями. Эти атомы находятся в состоянии sp2-гибридизации.
Алкены образуют гомологический ряд с общей формулой СnН2n.
Первым членом гомологического ряда является этилен имеющий молекулярную формулу С2Н4 и структурную формулу СН2=СН2. В силу особенности sp2-гибридизации молекула этилена имеет плоскостное строение. Наличие π-связи исключает возможность свободного вращения вокруг углерод-углеродной связи. Поэтому связи атомов углерода, затраченные на соединение с другими атомами или группами жестко расположены в одной плоскости под углом 1200 друг к другу. Жесткое строение системы двойной связи в молекулах алкенов вызывает определенные особенности в их строении.
Строение молекул алкенов предполагает существование двух видов изомерии:
1. изомерия положения двойной связи. Например:

2. Геометрическая или цис –, транс -изомерия
Геометрическими изомерами называются пространственные или стереоизомеры различающиеся положением заместителей относительно двойной связи. В силу отсутствия возможности вращения вокруг двойной связи - заместители могут располагаться либо по одну сторону двойной связи, либо по разные стороны. Например:

2. Номенклатура, Е, Z-номенклатура.
Для алкенов также действуют три номенклатуры: тривиальная, рациональная и систематическая.
Тривиальные названия:

По рациональной номенклатуре алкан рассматривается как производное этилена. При этом если заместители присоединены к разным углеродным атомам двойной связи, то олефин называют симметричным и обозначают символом «симм- », если заместители присоединены к одному углеродному атому двойной связи, то олефин называют несимметричным и обозначают символом «несимм -». Например:
 Названия олефинов по систематической номенклатуре образуют из названия алкана, имеющего аналогичное строение, заменяя суффикс «ан» на «ен». За главную цепь принимают самую длинную цепь, содержащую двойную связь. Нумерацию углеродных атомов начинают с того конца цепи, к которому ближе двойная связь. Например:
Названия олефинов по систематической номенклатуре образуют из названия алкана, имеющего аналогичное строение, заменяя суффикс «ан» на «ен». За главную цепь принимают самую длинную цепь, содержащую двойную связь. Нумерацию углеродных атомов начинают с того конца цепи, к которому ближе двойная связь. Например:

Порядок:
- выбрать самую длинную (главную) цепь, содержащую двойную связь;
- определиться со старшинством групп;
- пронумеровать главную цепь, придавая двойной связи наименьший из номеров локантов;
- перечислить префиксы;
- составить полное название соединения.
Например:

Для обозначения геометрических изомеров применяют две номенклатуры:
цис -, транс - и Е-, Z-
В соответствии с цис -, транс -номенклатурой геометрические изомеры, в которых заместители расположены по одну сторону относительно двойной связи называются с цис -изомерами.
Геометрические изомеры, в которых заместители расположены по разные стороны относительно двойной связи, называются транс -изомерами.
Если в качестве заместителей выступают углеводородные радикалы, то преимущество при определении конфигурации алкена имеют радикалы с более длинной углеродной цепью (конфигурация определяется относительно радикала с большей цепью). Например:
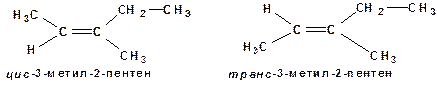
Часто цис -, транс -номенклатура не позволяет однозначно определить геометрические изомеры. Более совершенной в этом отношении является Е-, Z- номенклатура.
Е-Изомеры – это такие геометрические изомеры, в которых старшие заместители у углеродных атомов двойной связи находятся по разные стороны относительно двойной связи (от немецкого слова «entgegen» - напротив).
Z- Изомеры это такие геометрические изомеры, в которых старшие заместители у углеродных атомов двойной связи находятся по одну сторону относительно двойной связи (от немецкого слова «zusamen» - вместе).
Обозначение Е- и Z- ставят перед названием соединения по номенклатуре ИЮПАК и заключают в скобки (обозначение цис - и транс- в скобки не заключается). Например:
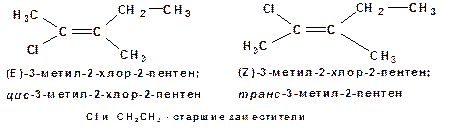
Старшинство заместителей определяется атомным номером элемента, атом которого связан с атомом углерода двойной связи, а при одном и том же элементе – атомными номерами элементов, следующих по цепи заместителя. Ряд заместителей в порядке возрастания старшинства:
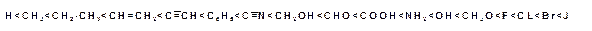
Способы получения.
Промышленные способы.
1. Первые четыре члена ряда олефинов получают в промышленности крекингом нефтяных дистиллятов.
2. Некоторые олефины, например 1-бутен и 2-бутен, а также пентены нормального и изомерного строения, получают дегидрогенизацией соответствующих предельных углеводородов. Процесс ведут с использованием гетерогенного катализатора на основе триоксида хрома и при температуре до 4500С:

Лабораторные способы.
Наиболее распространенными лабораторными способами получения олефинов являются дегидратация спиртов (отщепление воды от спиртов) и дегидрогалогенирование галогенпроизводных алканов (отщепление галогенводородов от галогеналканов). Обе эти реакции подчиняются правилу Зайцева:
При дегидратации спиртов и дегидрогалогенировании галогеналканов протон отщепляется преимущественно от наименее гидрогенизированного (имеющего меньшее число атомов водорода) атома углерода (1875г.).
Такое направление протекания этих реакций элиминирования объясняют повышенной термодинамической стабильностью образующегося олефина. Чем больше заместителей, тем больше возможностей для сверхсопряжения. Тем выше степень делокализации электронов, находящихся на π-связи. Соответственно выше термодинамическая стабильность. Стереоселективность определяется большей устойчивостью транс -изомера.
1. Дегидратация спиртов (элиминирование).
Отщепление воды от спирта проводят в газовой и жидкой фазах. В обоих случаях реакцию проводят при высокой температуре в присутствии водоотнимающего средства. В жидкой фазе используют серную или фосфорную кислоты, а в газовой фазе используют оксид фосфора (V), оксид алюминия, оксид тория или соли алюминия. Например:
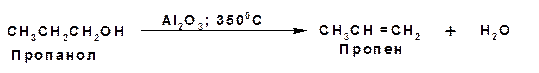
Механизм элиминирования в жидкой фазе включает две стадии. На первой образуется эфир из кислоты и спирта и на второй стадии распад эфира приводит к образованию олефина:

2. Дегидрогалогенироване галогеналканов.
Отщепление галогенводородов от галогеналканов проводят с использованием спиртового раствора едкого калия (КОН), реже используют NaОН:

3. Дегалогенироване вицинальных дигалогеналканов.
Олефины получают путем отщепления галогенов от дигалогенпроизводных с атомами галогена у соседних (или вицинальных) углеродных атомов. Элиминирование проводят в спиртовом или уксуснокислом растворе действием цинковой пыли:
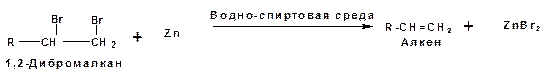
4. Гидрирование ацетиленовых углеводородов и алкадиенов.
В некоторых случая по ходу синтеза легче получить ацетиленовый углеводород, чем алкен. Ацетиленовые углеводороды сравнительно легко превращаются в алкены частичным гидрированием. Водород к π-электронной системе без катализатора не присоединяется. В случае получения алкенов из алкинов используют два варианта каталитической реакции: в газовой фазе на катализаторах гидрирования (платина, палладий, никель)отравленных свинцом (PbO) и в жидкой фазе натрием в жидком аммиаке. При этом образуются алкены различной конфигурации:
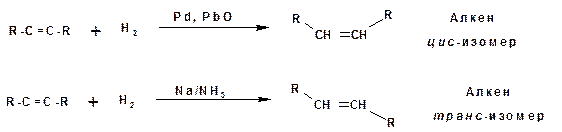
Гидрирование 1,3-диенов приводит к образованию смеси, изомерных по положению двойной связи, алкенов:

Физические свойства.
При нормальных условиях первые четыре члена гомологического ряда этиленовых углеводородов – газы. Олефины с числом углеродных атомов от 5-ти до 17–ти - жидкости. Далее идут твердые тела.
Олефины с нормальной цепью углеродных атомов кипят при более высокой температуре, чем их изомеры с развевленной цепью. Терминальные олефины (с концевой двойной связью) кипят при более низкой температуре, чем их изомеры с расположением двойной связи внутри цепи. транс -Изомеры плавятся при более высокой температуре, чем цис -изомеры. цис -Изомеры обычно кипят при более высокой температуре, чем транс -изомеры.
Плотность олефинов меньше единицы, но больше, чем плотность соотвествующих парафинов. В гоологическом ряду плотность увеличивается.
Растворимость олефинов в воде мала, но выше, чем у парафинов.
Химические свойства.
Главным структурным элементом, определяющим химические свойства олефинов, является двойная связь, включающая одну σ- и одну π-связь. Утомы углерода двойной связи пребывают в состоянии sp2-гибридизации. Сравнение статических факторов, в частности длины и энергии связи показывает, что двойная связь короче и прочнее ординарной связи:

Энергия двойной связи 607.1 кДж/моль, что больше энергии ординарной связи – 349,6 кДж/моль. Однако две ординарные связи по энергии превосходят одну двойную связь на 92.1 кДж/моль. Поэтому двойная связь легко переходит в две ординарные σ-связи путем присоединения по месту двойной связи двух атомов или атомных групп.
Из этого следует, что для олефинов наиболее характерны реакции присоединения. Но некоторым видам олефинов свойственны реакции замещения. Наиболее легко замещается водород у α-углеродного атома по отношению к двойной связи. Так назыываемое аллильное положение. Образующийся, при гомолитическом разрыве связи радикал способен взаимодействовать с электронами π-связи, что обеспечивает его высокую стабильность и соответственно высокую реакционную способность.
Поскольку π-связь представляет собой облако отрицательного заряда расположенное над и под плоскостью молекулы, то олефины должны быть склонны к взаимодействию с частицами, несущими положительный заряд. Реагентами, несущими положительный заряд являются электрофилы.
5.1. Электрофильное присоединение
Электрофильным присоединением (АdЕ) называют реакции присоединения, в которых в скоростьлимитирующей стадии атакующей частицей является электрофил.
Механизм электрофильного присоединения включает три стадии.
Например, присоединение бромистого водорода к этилену с образованием бромистого этила в среде четыреххлористого углерода:

Механизм:
1. На первой стадии образуется так называемый π-комплекс:
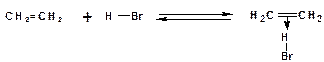
Особенностью π-комплекса является то, что атомы углерода двойной связи находятся в состоянии sp2-гибридизации.
2. Образование промежуточного карбкатиона. Эта стадия является медленной (скоростьлимитирующей):

На этой стадии один из атомов углерода двойной связи переходит в состояние sp3-гибридизации. Другой остается в состоянии sp2-гибридизации и приобретает вакантную р-орбиталь.
3. На третьей стадии бромид-ион, образовавшийся на второй стадии, быстро присоединяется к карбкатиону:

Аналогичный механизм можно привести для реакции электрофильного присоединения брома к этилену с образованием 1,2-дибромэтана в среде четыреххлористого углерода.
1. Образование π-комплекса:

2. Образование циклического бромониевого иона:

Циклический бромониевый ион более стабилен, чем открытый этил-катион. Причина такой стабильности в том, что в циклическом бромониевом ионе все атомы имеют по восемь электронов на внешнем электронном уровне. В то время ка в этил-катионе у атома углерода, несущего положительный заряд имеется только шесть электронов. Образование бромониевого иона связано с гетеролитическим разрывом связи Br- Br и отщеплением бромид-иона.
3. Присоединение бромид-иона к циклическому бромониевому иону:
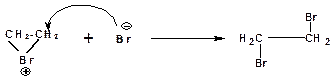
Поскольку одна сторона исходного алкена экранирована в бромониевом ионе положительно заряженным атомом брома, то бромид-ион может атаковать бромониевый ион только с противоположной стороны. При этом трехчленный цикл раскрывается, а бромид-ион образует ковалентную связь с атомом углерода. Продуктом присоединения является вицинальный дибромид.
Доказательством представленного механизма, предусматривающего атаку бромониевого иона бромид-ионом с тыльной стороны, является образование транс -1,2-дибромциклогексана по реакции циклогексена с бромом:

Правило Марковникова.
Взаимодействие галогенводородов с несимметричными алкенам по механизму электрофильного присоединения приводит к образованию продуктов строго определенного строения. Так по реакции 2-метил-2-бутена с бромистым водородом преимущественно образуется 2-бром-2-метилбутан:

Строение, образующегося продукта в случае реакции электрофильного присоединения к несимметричным алкенам подчиняется правилу Марковникова:
При присоединении галогеноводорода к несимметричному алкену протон реагента преимущественно присоединяется к наиболее гидрогенизированному(имеющему большее число атомов водорода) атому углерода (1869г.).
Объяснение данному направлению хода реакции заключается в том, что образующиеся на второй стадии механизма электрофильного присоединения карбкатионы формируют ряд стабильности, аналогичный ряду стабильности радикалов:
Метил-катион <первичный <вторичный <третичный.
В соответствии с рядом стабильности продукт присоединения галогенид-иона к третичному углеродному атому будет более предпочтительным, чем присоединение ко вторичному.
По механизму электрофильного присоединения в соответствии с правилом Марковникова к олефинам присоединяются:
галогенводороды; галогены, вода, гипогалогенитные кислоты:

В случае присоединения гипогалогенитных кислот в роли электрофильной частицы выступает ион галоида (кроме фтора), поскольку электроотрицательность хлора, брома и йода меньше, чем у кислорода.
Радикальные реакции.